Clear Sky Science · pl
Podpisane, zapieczętowane, dostarczone: uogólnialny model dawkowania i metabolizmu żywych bioterapeutyków
Przekształcanie pożytecznych mikrobów w lekarstwo
Wielu ludzi wie, że mikroby w naszych jelitach wpływają na zdrowie, ale znacznie trudniej jest przełożyć te maleńkie towarzysze na precyzyjne, niezawodne lekarstwo. W tym badaniu autorzy rozwiązują bardzo praktyczne pytanie: jeśli połkniemy kapsułkę z zaprojektowanymi „dobrymi bakteriami”, które mają oczyścić szkodliwy związek w jelicie, ile powinniśmy ich zażyć i kiedy? Naukowcy budują ramę matematyczną łączącą to, co dzieje się z jedzeniem w żołądku i jelitach, działania naszych rodzimych mikroorganizmów oraz to, jak dodany szczep probiotyczny może wkroczyć, aby chronić organizm.
Zaburzenie zapachu ciała jako studium przypadku
Badacze koncentrują się na trimetyloaminurii, nazywanej czasem „zespołem zapachu ryby”. W tym schorzeniu mutacje w enzymie wątroby sprawiają, że silnie pachnący związek, trimetyloamina (TMA), nie zostaje odpowiednio zneutralizowany i zamiast tego gromadzi się w pocie, wydychanym powietrzu i moczu. TMA powstaje przede wszystkim w jelicie, gdy bakterie rozkładają składniki odżywcze takie jak cholina, obecne w powszechnych produktach jak jaja czy mięso. Obecne terapie próbują ograniczyć podaż tych składników lub eliminować bakterie jelitowe antybiotykami — strategie trudne do utrzymania i obarczone skutkami ubocznymi. Autorzy badają inną koncepcję: dodać żywy produkt bioterapeutyczny — zmodyfikowaną bakterię przenoszącą enzym zdolny przekształcić TMA w obojętną, bezwonną formę bezpośrednio w jelicie, zanim związek dostanie się do krwiobiegu.
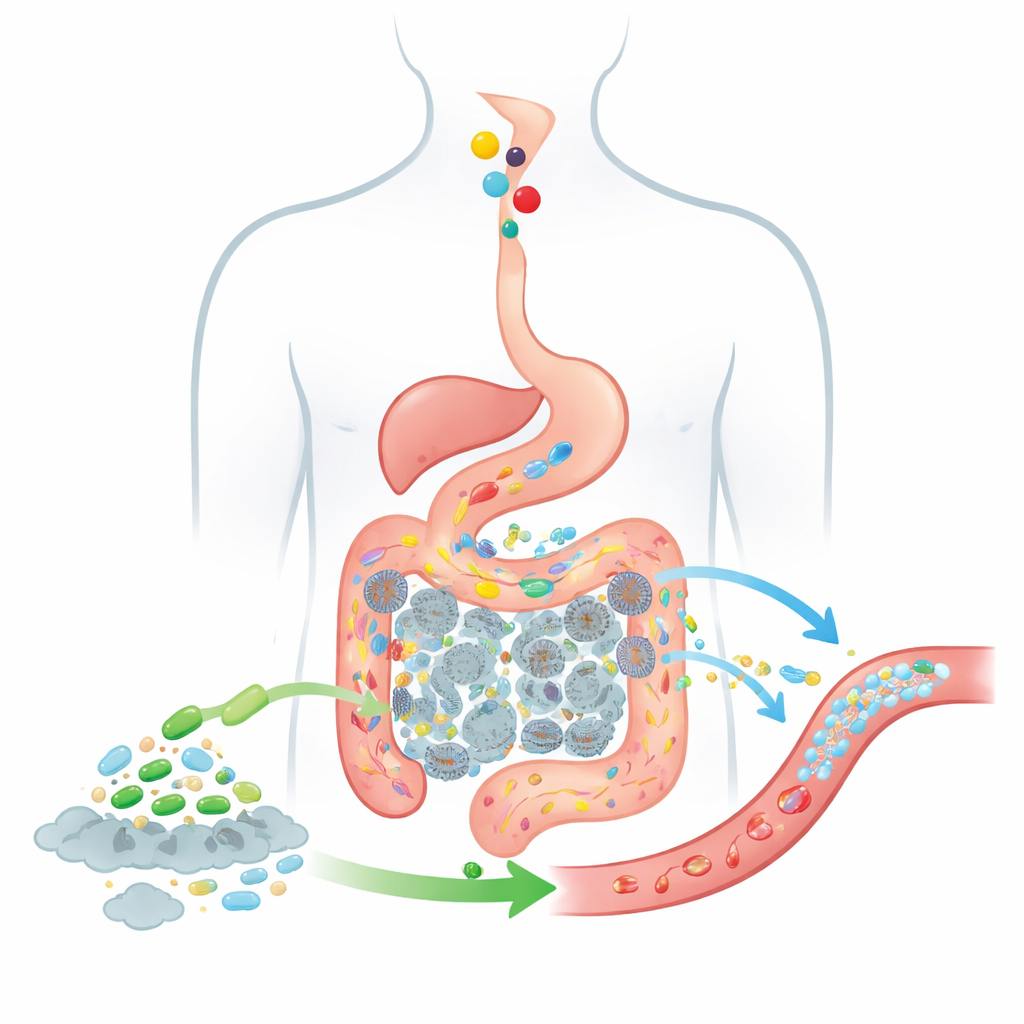
Śledzenie jedzenia i bakterii przez jelita
Aby przewidzieć, jak skuteczne może być takie żywe leczenie, autorzy rozszerzają klasyczny model wchłaniania leków znany jako model CAT, który śledzi, jak połknięte substancje poruszają się od żołądka przez segmenty jelita cienkiego do okrężnicy. Ich zaktualizowany model BCAT dzieli jelito na wiele połączonych „skrzyniek”, z których każda reprezentuje odcinek jelita lub okrężnicy z określoną objętością płynu, typową liczbą bakterii i sposobem wchłaniania. Gdy pokarm przechodzi z jednej skrzynki do następnej, model śledzi, ile jest choliny, ile TMA produkują bakterie jelitowe, jaka część TMA przechodzi do krwi oraz jak dodane komórki probiotyczne przemieszczają się i działają tą samą trasą. W przeciwieństwie do wcześniejszych modeli, ten traktuje populację probiotyczną jako przemieszczającą się, zmieniającą się chmurę komórek, a nie stałe tło, i jawnie uwzględnia okrężnicę, gdzie powstaje zdecydowana większość TMA.
Weryfikacja modelu na danych z życia
Model jest użyteczny tylko wtedy, gdy odpowiada rzeczywistości, więc zespół przetestował BCAT na danych ludzkich. Najpierw sprawdzili, czy model potrafi odtworzyć klasyczne badania żywieniowe z lat 50. až 90., w których ochotnicy jedli określone dawki choliny, a potem analizowano TMA i jego zneutralizowaną formę w moczu. W różnych dawkach i niezależnych badaniach frakcja choliny przekształcanej w trimetyloaminy oscylowała okołodwóch trzecich; BCAT pomyślnie odtworzył ten wzorzec. Następnie zastosowali ramy do innego zmodyfikowanego probiotyku, SYNB1618, zaprojektowanego dla fenyloketonurii. Korzystając z danych z badań klinicznych o tym, ile diagnostycznego produktu rozkładu pojawiło się w moczu uczestników, przewidywania BCAT różniły się tylko o około 5 procent, znacznie przewyższając prostsze, niskorozdzielcze modele.
Ile probiotyku i kiedy go zażyć?
Mając tę walidację, autorzy zastosowali BCAT do trimetyloaminurii. Zadali pytanie: jaka jest najmniejsza dawka probiotyku, która zmniejszy całkowitą ekspozycję na TMA we krwi o 95 procent, co mniej więcej odpowiada naturalnej mocy oczyszczającej zdrowego enzymu wątroby? Gdy probiotyk i posiłek są przyjmowane razem, model sugeruje dawkę około dziesięciu miliardów komórek, podobną do zawartości typowej dostępnej bez recepty kapsułki probiotycznej. Ale ma znaczenie czas podania. Ponieważ rodzimy ekosystem bakteryjny już osiedlił się w całej okrężnicy, a połknięte probiotyki muszą tam dotrzeć ze żołądka, występuje opóźnienie zanim terapia znajdzie się we właściwym miejscu. Symulacje pokazują, że przyjęcie probiotyku około trzy do czterech godzin przed posiłkiem bogatym w cholinę pozwala mu „przybyć wcześniej”, rozprzestrzenić się po okrężnicy i efektywniej przechwytywać TMA. Przy takim harmonogramie wymagana dawka spada w przybliżeniu czterokrotnie, co może zmniejszyć obawy dotyczące bezpieczeństwa bardzo wysokich obciążeń mikrobiologicznych.
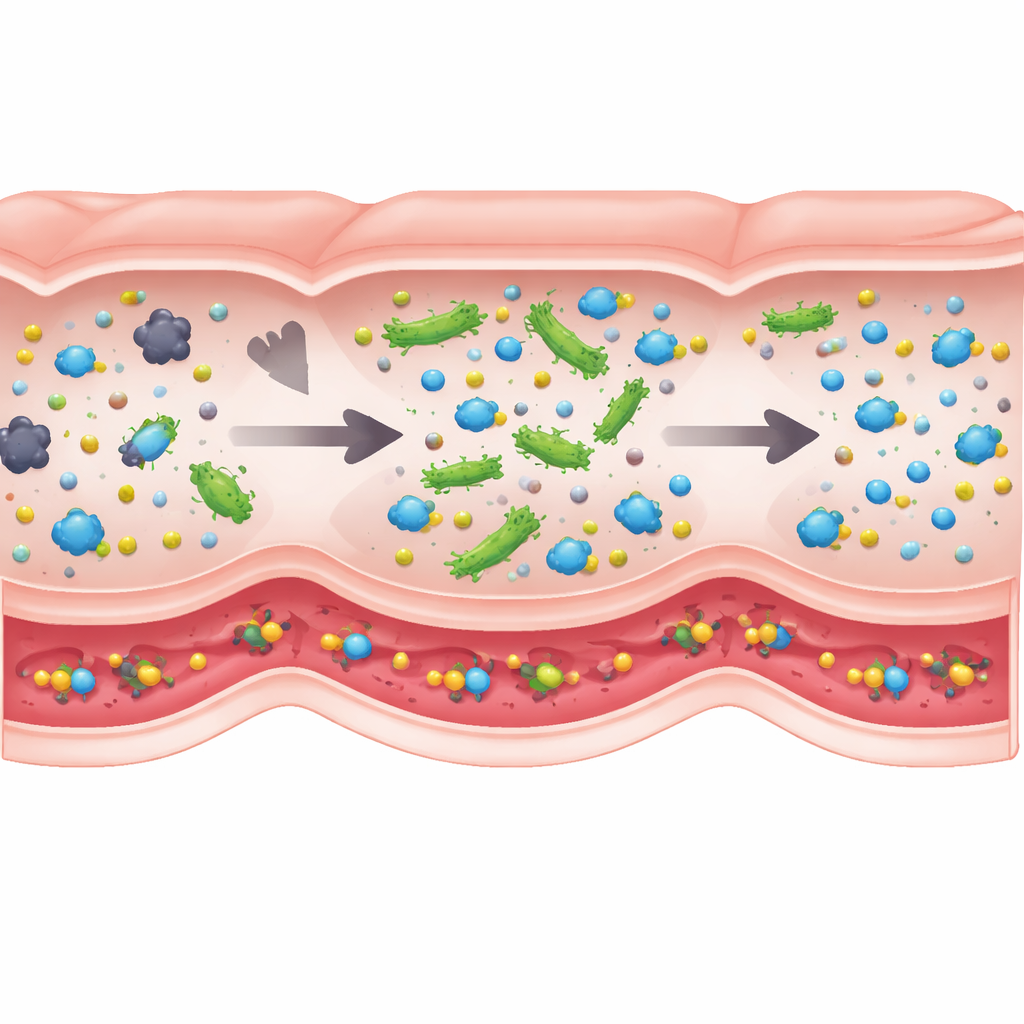
Co ma największe znaczenie „pod maską”
Nie każdy element biologiczny wpływa na wynik w równym stopniu, więc autorzy zastosowali rodzaj globalnej analizy wrażliwości, aby zobaczyć, które składniki modelu faktycznie napędzają sukces. Najważniejszym czynnikiem okazała się ilość aktywnego enzymu, jaką niesie każda komórka probiotyczna. Zmiany w czasie przejścia przez jelita, szybkościach wchłaniania czy nawet w ogólnej gęstości bakterii miały relatywnie niewielki wpływ w realistycznych zakresach. Oznacza to, że przy projektowaniu takich żywych bioterapeutyków inżynieria komórek produkujących więcej kluczowego enzymu może być znacznie ważniejsza niż dopracowywanie tempa ich przemieszczania się przez jelito. Sugeruje to również, że rekomendacje dawkowania z BCAT powinny być stosunkowo odporne na różnice między ludźmi, nawet jeśli ich tempo trawienia i mikrobiomy się różnią.
Od jednego schorzenia do wielu
Ostatecznie ta praca nie tylko daje wskazówki dla rzadkiego i społecznie uciążliwego zaburzenia zapachu. Wprowadza ogólne, adaptowalne ramy do planowania i optymalizacji terapii z wykorzystaniem żywych mikrobów dla każdego stanu, w którym mikrobiom jelitowy przekształca dietetyczne lub pochodzące z organizmu związki w szkodliwe produkty. Łącząc w jedną ilościową wizję pasaż jelitowy, rodzimą chemię mikrobiologiczną i zaprojektowane enzymatyczne oczyszczanie, model BCAT może wskazać realistyczne cele dawkowania i strategie czasowania dużo wcześniej, niż szczep osiągnie próby kliniczne. Dla pacjentów i klinicystów to przybliża perspektywę, że przyszłe leki probiotyczne będą nie tylko przyjazne i brzmiące naturalnie, ale też przewidywalne, regulowalne i oparte na tym samym rygorze planowania, co konwencjonalne leki.
Cytowanie: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Słowa kluczowe: mikrobiom jelitowy, terapia probiotyczna, trimetyloaminuria, modelowanie matematyczne, żywe bioterapeutyki