Clear Sky Science · sv
Undertecknat, förseglat, levererat: en generaliserbar modell för dosering och metabolism av levande bioterapeutika
Att göra hjälpsamma bakterier till medicin
Många vet att mikroberna i vår tarm kan påverka hälsan, men det är långtifrån uppenbart hur man förvandlar dessa små passagerare till precis, pålitlig medicin. Denna studie tar sig an en mycket praktisk fråga: om vi sväljer en kapsel med konstruerade ”goda bakterier” avsedd att ta hand om en skadlig kemikalie i tarmen, hur mycket bör vi ta och när bör vi ta den? Författarna bygger ett matematiskt ramverk som knyter samman vad som händer med födan när den rör sig genom magsäcken och tarmarna, vad våra bofasta mikrober gör med den, och hur ett tillsatt probiotiskt stam kan ingripa för att skydda kroppen.
En kroppsdoftsstörning som testfall
Forskarnas fokus ligger på trimetylaminuri, ibland kallat ”fiskluktssyndromet.” Vid detta tillstånd innebär mutationer i en leverenzym att en starkt luktande förening, trimetylamin (TMA), inte neutraliseras på rätt sätt utan istället byggs upp i svett, utandning och urin. TMA bildas främst i tarmen när bakterier bryter ner näringsämnen som kolin från vanliga livsmedel som ägg och kött. Nuvarande behandlingar försöker svälta systemet på dessa näringsämnen eller döda tarmbakterier med antibiotika — strategier som är svåra att upprätthålla och kan ge biverkningar. Författarna utforskar en annan idé: tillsätta en levande bioterapeutisk produkt — en konstruerad bakterie som bär på ett enzym som kan omvandla TMA till en ofarlig, luktfri form direkt i tarmen innan den hinner gå över i blodet.
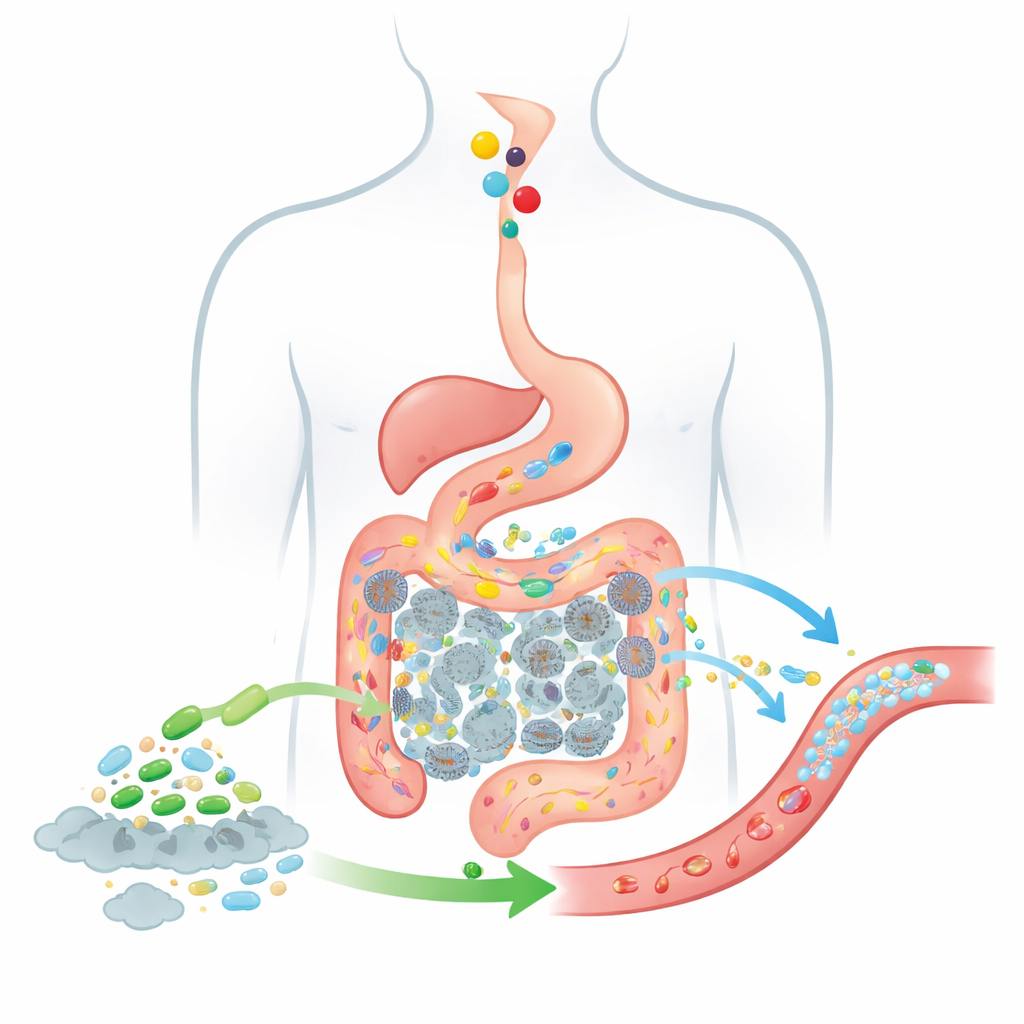
Följa föda och bakterier genom tarmen
För att förutsäga hur väl en sådan levande terapi kan fungera, utökar författarna en klassisk modell för läkemedelsupptag känd som CAT-modellen, som spårar hur inmundigade substanser rör sig från magsäcken genom segment av tunntarmen och in i tjocktarmen. Deras uppdaterade BCAT-modell delar in tarmen i flera sammankopplade ”boxar”, där varje box representerar en tarmsträcka eller kolon med sin egen vätskevolym, typiska bakterieantal och absorptionsbeteende. När födan passerar från en box till nästa håller modellen reda på hur mycket kolin som finns, hur mycket TMA tarmbakterier producerar, hur mycket av det TMA som passerar över i blodet, och hur tillsatta probiotiska celler färdas och verkar längs samma rutt. Till skillnad från tidigare modeller behandlar denna modell den probiotiska populationen som ett rörligt, föränderligt moln av celler snarare än en fast bakgrund, och den inkluderar uttryckligen kolon, där den absoluta majoriteten av TMA bildas.
Kontrollera modellen mot verkliga data
En modell är bara användbar om den stämmer överens med verkligheten, så teamet testade BCAT mot mänskliga data. Först frågade de om modellen kunde återskapa klassiska näringsstudier från 1950- till 1990-talen, där frivilliga åt uppmätta doser kolin och forskare senare samlade in och analyserade TMA och dess neutraliserade form i urin. Över flera dosnivåer och oberoende studier låg andelen kolin som omvandlades till trimetylaminer kring två tredjedelar; BCAT fångade framgångsrikt detta mönster. Därefter tillämpade de ramverket på en annan konstruerad probiotika, SYNB1618, designad för den ärftliga sjukdomen fenylketonuri. Med kliniska data om hur mycket av en diagnostisk nedbrytningsprodukt som dök upp i försöksdeltagarnas urin skilde sig BCAT:s förutsägelser med endast omkring 5 procent, vilket klart överträffade enklare, lågupplösta modeller.
Hur mycket probiotika och när ska man ta den?
Med denna validering i handen lät författarna BCAT undersöka trimetylaminuri. De frågade: Vad är den minsta probiotikados som kan minska total TMA-exponering i blodet med 95 procent, vilket ungefär motsvarar den naturliga nedbrytningskraften hos ett friskt leverenzym? När probiotika och måltid tas samtidigt föreslår modellen en dos kring tio miljarder celler, liknande vad som får plats i en typisk receptfri probiotikakapsel. Men tidpunkten spelar roll. Eftersom bofasta tarmbakterier redan är etablerade genom hela kolon medan insvalda probiotika måste färdas dit från magsäcken, finns det en fördröjning innan terapin befinner sig på rätt plats. Simulationer visar att det att ta probiotikan ungefär tre till fyra timmar före en kolinrik måltid gör att den kan ”ankomma i förväg”, sprida sig genom kolon och avbryta TMA mer effektivt. Med detta schema minskar den erforderliga dosen ungefär fyra gånger, vilket kan minska säkerhetsbekymmer kring mycket höga mikrobmängder.
Vad som betyder mest under ytan
Inte alla biologiska detaljer påverkar utgången lika mycket, så författarna använde en typ av global känslighetsanalys för att se vilka modellingredienser som faktiskt driver framgång. Den tydliga vinnaren var mängden aktivt enzym som varje probiotikacell kan bära. Förändringar i tarmtransittider, absorptionshastigheter eller till och med den totala bakterietätheten hade jämförelsevis små effekter inom realistiska intervall. Det innebär att när man designar sådana levande bioterapeutika kan det vara långt viktigare att konstruera celler som producerar mer av nyckelenzymet än att finjustera hur snabbt de rör sig genom tarmen. Det antyder också att dosrekommendationer från BCAT bör vara ganska robusta över olika personer, även om deras matsmältningshastigheter och mikrobiom varierar.
Från en störning till många
Slutligen erbjuder detta arbete inte bara vägledning för en sällsynt och socialt plågsam luktstörning. Det introducerar ett generellt, anpassningsbart ramverk för planering och optimering av levande mikrobiella terapier för alla tillstånd där tarmmikrobiomet omvandlar diet- eller kroppsfödda föreningar till skadliga biprodukter. Genom att sammanföra tarmtransit, infödd mikrobiell kemi och konstruerad enzymatisk städning i en kvantitativ bild kan BCAT-modellen föreslå realistiska doseringsmål och tidningsstrategier långt innan en stam når kliniska prövningar. För patienter och kliniker innebär detta löftet att framtida probiotikamediciner inte bara kommer att låta vänliga och naturliga, utan också bli förutsägbara, ställbara och grundade i samma typ av noggranna planering som används för konventionella läkemedel.
Citering: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Nyckelord: tarmmikrobiom, probiotisk terapi, trimetylaminuri, matematisk modellering, levande bioterapeutika