Clear Sky Science · ja
署名済み、封印済み、配達済み:生体治療薬の投与量と代謝のための一般化可能なモデル
有益な微生物を医薬品に変える
腸内の微生物が健康に影響を与えることは広く知られていますが、それらの小さな共生者を精密で信頼できる薬に変える方法ははるかに分かりにくいものです。本研究は実践的な問いに取り組みます:有害な化合物を腸内で除去するよう設計された「良い細菌」のカプセルを飲む場合、どれだけ、いつ摂取すべきか?著者らは、胃や腸を通る食物の挙動、常在微生物の作用、そして添加されたプロバイオティクス株がどのように体を守るかを結びつける数理フレームワークを構築します。
嗅覚障害を試験例に
研究者らはトリメチルアミン尿症(しばしば「魚臭症候群」と呼ばれる)に着目します。この疾患では肝臓の酵素の変異により、強い臭いを持つ化合物トリメチルアミン(TMA)が適切に中和されず、汗や呼気、尿に蓄積します。TMAは主に、卵や肉など一般的な食品に含まれるコリンなどの栄養素を腸内細菌が分解する際に生成されます。現在の治療はこれらの栄養素を制限するか、抗生物質で腸内細菌を減らすことを試みますが、持続が難しく副作用を引き起こす可能性があります。著者らは別の発想を検討します:TMAが血流に入る前に腸内で直接無害で無臭の形に変換できる酵素を持つ遺伝子組み換え細菌という生体治療製品を添加する方法です。
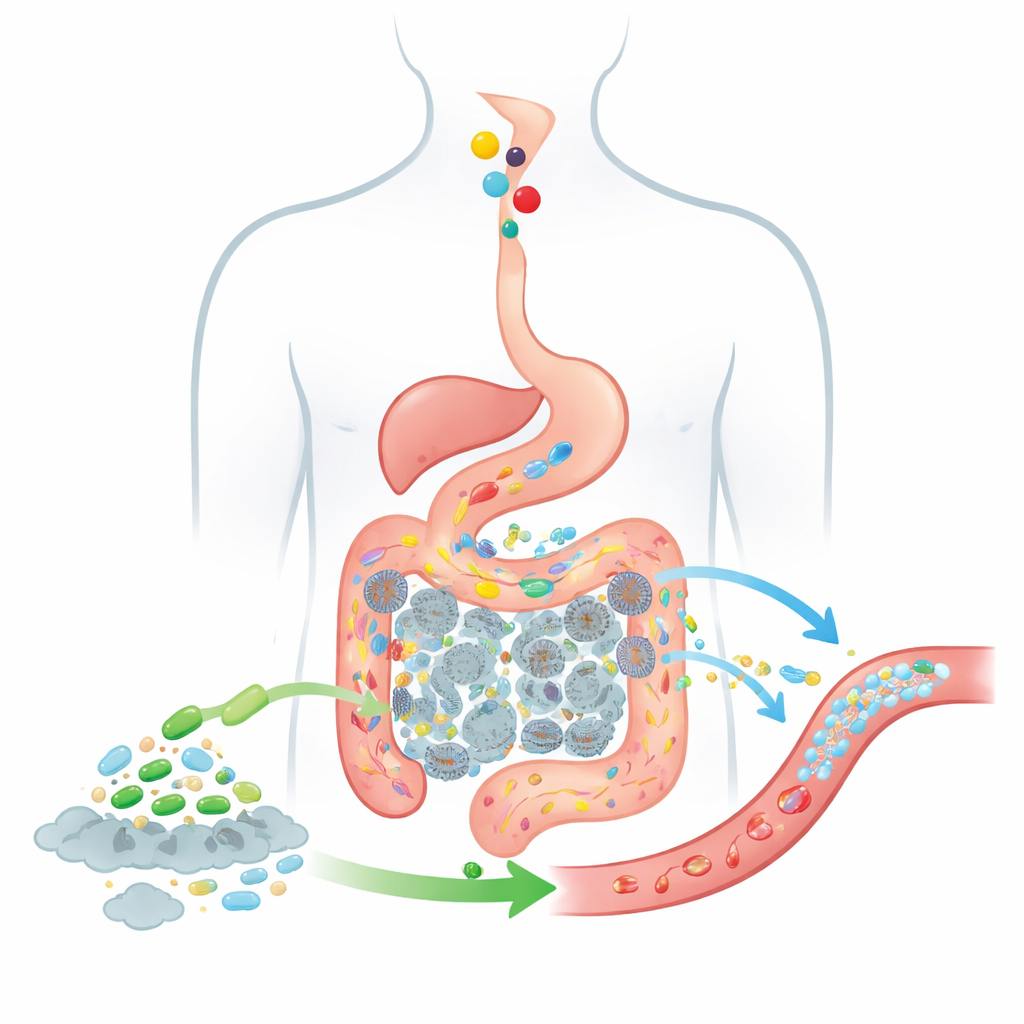
食物と細菌の腸内での追跡
そのような生きた治療がどれほど効果的かを予測するため、著者らは古典的な薬物吸収モデルであるCATモデルを拡張します。このモデルは、飲み込まれた物質が胃から小腸の区画を経て結腸へ移動する様子を追跡します。改良版のBCATモデルは腸を複数の相互接続された「ボックス」に分割し、それぞれのボックスが流体量、典型的な細菌数、吸収の特性を持ちます。食物がボックスから次のボックスへ移る際に、コリンの量、腸内細菌が産生するTMAの量、血中に移行するTMAの量、そして添加されたプロバイオティクス細胞が同じ経路をどのように移動し作用するかをモデルが追跡します。従来のモデルと異なり、本モデルはプロバイオティクス集団を固定的な背景としてではなく、移動し変化する細胞の雲として扱い、TMAの大部分が生成される結腸を明示的に含めています。
実データとの照合
モデルは現実と一致してこそ有用です。そこでチームはBCATを人データで検証しました。まず、1950年代から1990年代の古典的な栄養学的研究を再現できるかを確かめました。被験者が測定された量のコリンを摂取し、その後尿中のTMAとその中和体を収集・解析したこれらの研究で、複数の投与量や独立した研究にわたり、コリンがトリメチルアミン類に変換される割合は約3分の2に近い値を示しました。BCATはこのパターンをうまく再現しました。次に、遺伝性疾患フェニルケトン尿症のために設計された別の遺伝子組み換えプロバイオティクスSYNB1618にフレームワークを適用しました。被験者の尿中に出現した診断的分解産物の量に関する臨床試験データを用いたところ、BCATの予測は約5パーセントの差にとどまり、低解像度の単純なモデルよりもはるかに優れていました。
どれだけのプロバイオティクスをいつ摂るべきか?
この検証を得て、著者らはBCATをトリメチルアミン尿症に適用しました。問いはこうです:健康な肝酵素の自然な除去能力に大まかに匹敵する、血中の総TMA曝露を95%削減できる最小のプロバイオティクス投与量はどれか?プロバイオティクスと食事を同時に摂る場合、モデルは約100億個の細胞量を示唆し、これは市販のプロバイオティクスカプセルに収まる量に近いものです。しかし、タイミングが重要です。常在の腸内細菌はすでに結腸全体に存在している一方で、飲み込んだプロバイオティクスは胃から結腸へ移動する必要があるため、治療が適所に到達するまでに遅れがあります。シミュレーションは、コリンを多く含む食事の約3〜4時間前にプロバイオティクスを摂取すると、それが「早めに到着」して結腸に広がり、TMAをより効果的に捕捉できることを示します。このスケジュールでは必要投与量が約4分の1に減少し、非常に高い微生物負荷に関する安全性の懸念を低減できる可能性があります。
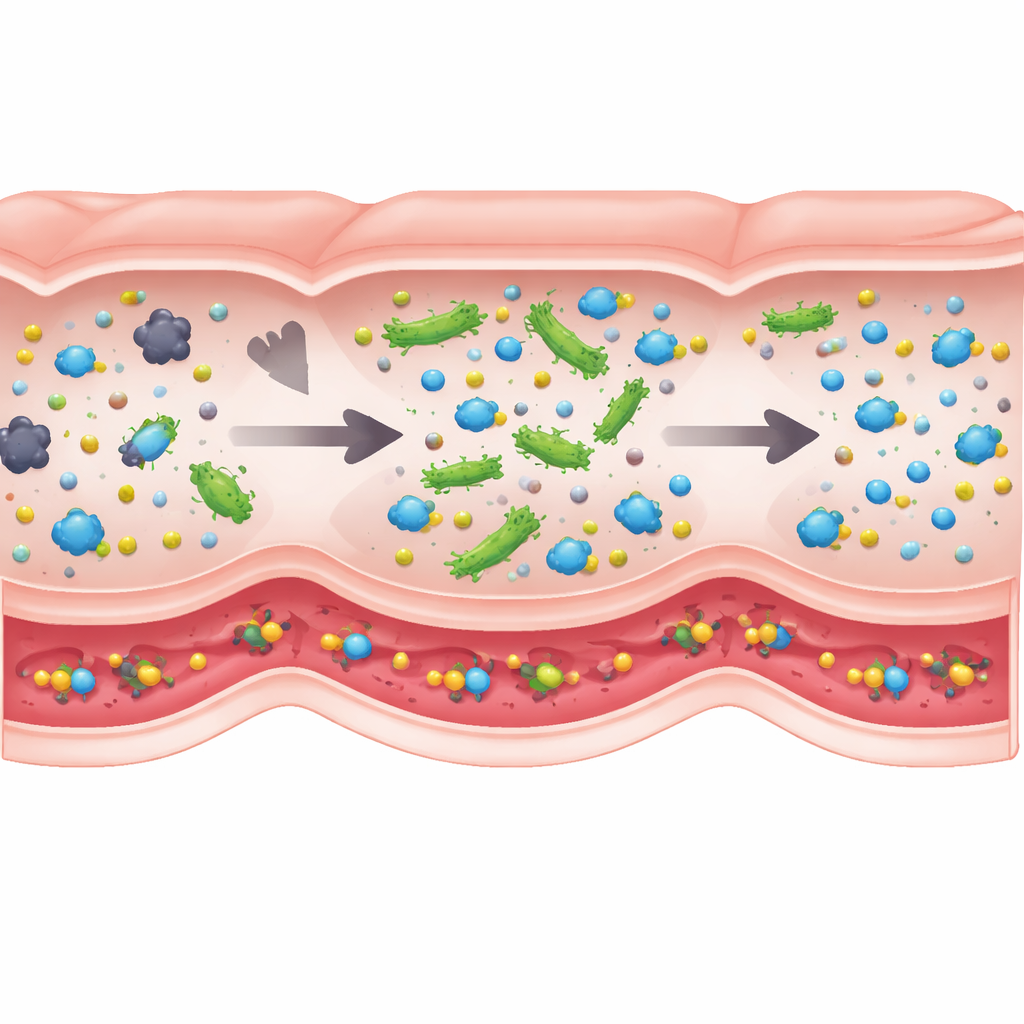
内部で最も重要な要素
すべての生物学的詳細が結果に同じ影響を与えるわけではありません。そこで著者らはグローバル感度解析の一種を用いて、モデルの成功を実際に左右する要素を調べました。明快な勝者は、各プロバイオティクス細胞が運ぶことのできる活性酵素の量でした。腸内通過時間、吸収率、あるいは総細菌密度の変化は、現実的な範囲では比較的小さい影響にとどまりました。これは、こうした生体治療薬を設計する際には、細胞がより多くの主要酵素を産生するように工学的に改変することが、腸内での移動速度の微調整よりもはるかに重要である可能性を示唆します。また、消化速度やマイクロバイオームが人によって異なっても、BCATによる投与勧告はかなり頑健であることを示しています。
一つの疾患から多くの疾患へ
結局のところ、本研究は稀で社会的に困難な臭気障害への指針を提供するだけではありません。腸内マイクロバイオームが食事性または体内由来の化合物を有害な副産物に変えるようなあらゆる状態に対して、ライブ微生物治療を計画・最適化するための一般的で適応可能なフレームワークを提示します。腸の通過、常在微生物の化学反応、設計された酵素による除去を一つの定量的な図に編み合わせることで、BCATモデルは株が臨床試験に到達する前から現実的な投与目標とタイミング戦略を示唆できます。患者と臨床家にとって、将来のプロバイオティクス治療は親しみやすく自然に聞こえるだけでなく、従来薬と同様の厳密な計画に基づいた予測可能で調整可能なものになるという期待をもたらします。
引用: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
キーワード: 腸内マイクロバイオーム, プロバイオティクス療法, トリメチルアミン尿症, 数理モデリング, 生体由来治療薬(ライブバイオセラピューティクス)