Clear Sky Science · fr
Signé, scellé, livré : un modèle généralisable pour le dosage et le métabolisme des biothérapeutiques vivantes
Transformer des microbes utiles en médicaments
Beaucoup savent que les microbes de notre intestin influent sur la santé, mais il est bien moins évident de transformer ces minuscules hôtes en médicaments précis et fiables. Cette étude aborde une question très concrète : si l’on avale une gélule de « bonnes bactéries » génétiquement modifiées destinée à éliminer un composé nocif dans l’intestin, quelle quantité faut-il prendre et à quel moment ? Les auteurs construisent un cadre mathématique qui relie ce qui arrive aux aliments lorsqu’ils traversent l’estomac et les intestins, ce que font nos microbes résidents, et comment une souche probiotique ajoutée peut intervenir pour protéger l’organisme.
Un trouble de l’odeur corporelle comme cas-test
Les chercheurs se concentrent sur la triméthylaminurie, parfois appelée « syndrome de l’odeur de poisson ». Dans cette pathologie, des mutations d’une enzyme hépatique empêchent la neutralisation correcte d’un composé à forte odeur, la triméthylamine (TMA), qui s’accumule alors dans la sueur, l’haleine et l’urine. La TMA est principalement produite dans l’intestin lorsque des bactéries dégradent des nutriments comme la choline, présents dans des aliments courants tels que les œufs et la viande. Les traitements actuels cherchent à priver le système de ces nutriments ou à éliminer les bactéries intestinales par des antibiotiques, des stratégies difficiles à maintenir et susceptibles d’entraîner des effets indésirables. Les auteurs explorent une idée différente : ajouter un produit biothérapeutique vivant — une bactérie ingénierée portant une enzyme capable de convertir la TMA en une forme inoffensive et inodore directement dans l’intestin avant qu’elle n’atteigne la circulation sanguine.
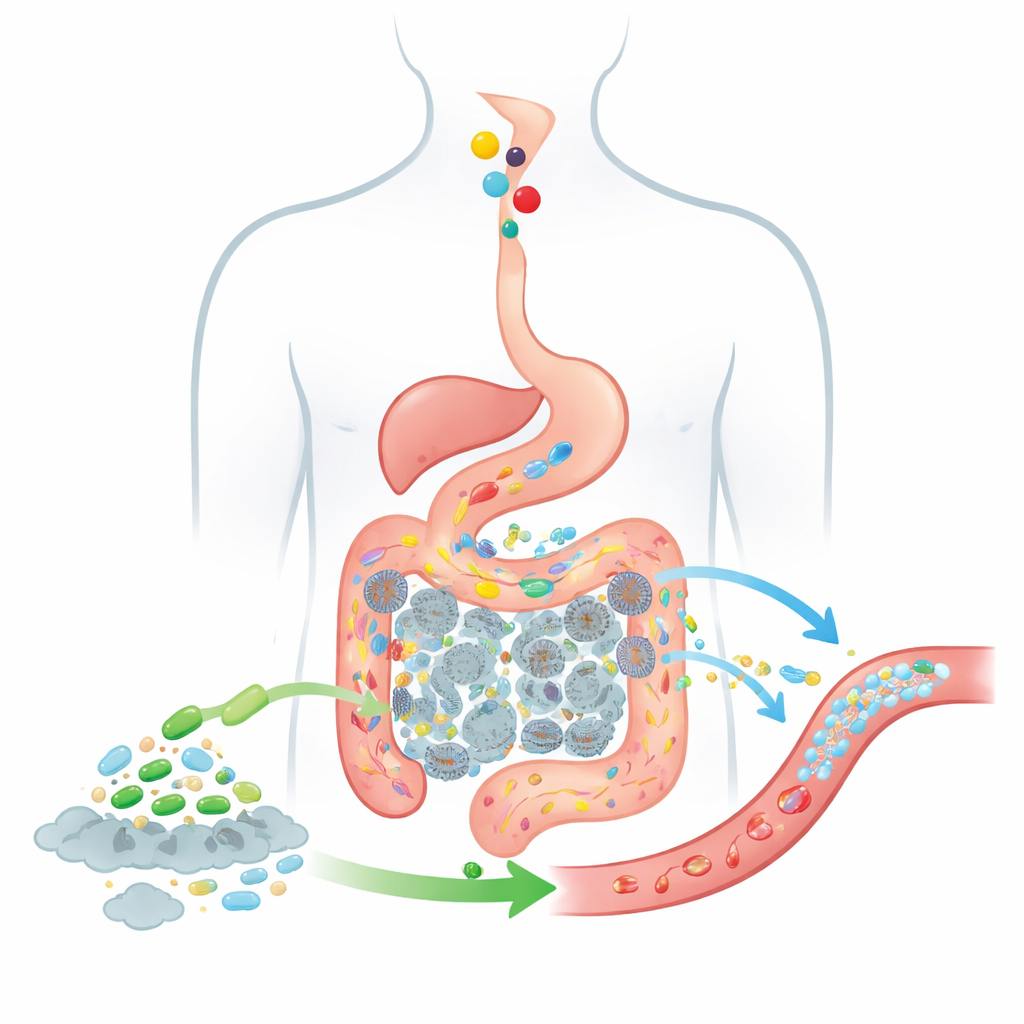
Suivre aliments et bactéries dans l’intestin
Pour prédire l’efficacité d’une telle thérapie vivante, les auteurs étendent un modèle classique d’absorption des médicaments connu sous le nom de modèle CAT, qui suit le déplacement des substances avalées depuis l’estomac à travers des segments de l’intestin grêle jusqu’au côlon. Leur modèle BCAT mis à jour divise l’intestin en plusieurs « boîtes » connectées, chacune représentant un tronçon d’intestin ou du côlon avec son propre volume de fluide, un nombre typique de bactéries et un comportement d’absorption. Lorsque la nourriture passe d’une boîte à l’autre, le modèle suit la quantité de choline présente, la quantité de TMA produite par les bactéries intestinales, la part de cette TMA qui passe dans le sang, et la manière dont les cellules probiotiques ajoutées voyagent et agissent le long du même trajet. Contrairement aux modèles précédents, celui-ci traite la population probiotique comme un nuage mobile et changeant de cellules plutôt que comme un arrière-plan fixe, et il inclut explicitement le côlon, lieu de production de la grande majorité de la TMA.
Vérifier le modèle avec des données du monde réel
Un modèle n’est utile que s’il correspond à la réalité, aussi l’équipe a-t-elle testé BCAT sur des données humaines. D’abord, ils ont vérifié si le modèle pouvait reproduire des études nutritionnelles classiques des années 1950 à 1990, où des volontaires consommaient des doses mesurées de choline et où les chercheurs analysaient ensuite la TMA et sa forme neutralisée dans l’urine. Sur plusieurs niveaux de dose et d’études indépendantes, la fraction de choline convertie en triméthylamines tournait autour des deux tiers ; BCAT a correctement capturé ce schéma. Ensuite, ils ont appliqué le cadre à un probiotique ingénieré différent, SYNB1618, destiné à la maladie héréditaire phénylcétonurie. En utilisant des données d’essais cliniques sur la quantité d’un produit de dégradation diagnostique apparu dans l’urine des sujets, les prédictions de BCAT différaient d’environ 5 % seulement, surpassant largement les modèles plus simples et de faible résolution.
Quelle quantité de probiotique et quand le prendre ?
Avec cette validation en poche, les auteurs ont appliqué BCAT à la triméthylaminurie. Ils se sont demandés : quelle est la plus petite dose probiotique capable de réduire l’exposition totale à la TMA dans le sang de 95 %, soit à peu près l’efficacité nettoyante d’une enzyme hépatique saine ? Lorsque le probiotique et le repas sont pris simultanément, le modèle suggère une dose d’environ dix milliards de cellules, similaire à ce que contient une capsule probiotique vendue sans ordonnance. Mais le moment compte. Parce que les bactéries résidentes sont déjà établies dans tout le côlon tandis que les probiotiques avalés doivent s’y rendre depuis l’estomac, il existe un délai avant que la thérapie n’arrive au bon endroit. Les simulations montrent que prendre le probiotique environ trois à quatre heures avant un repas riche en choline lui permet « d’arriver en avance », de se répandre dans le côlon et d’intercepter la TMA plus efficacement. Avec ce calendrier, la dose requise diminue d’un facteur d’environ quatre, ce qui pourrait réduire les inquiétudes liées à des charges microbiennes très élevées.
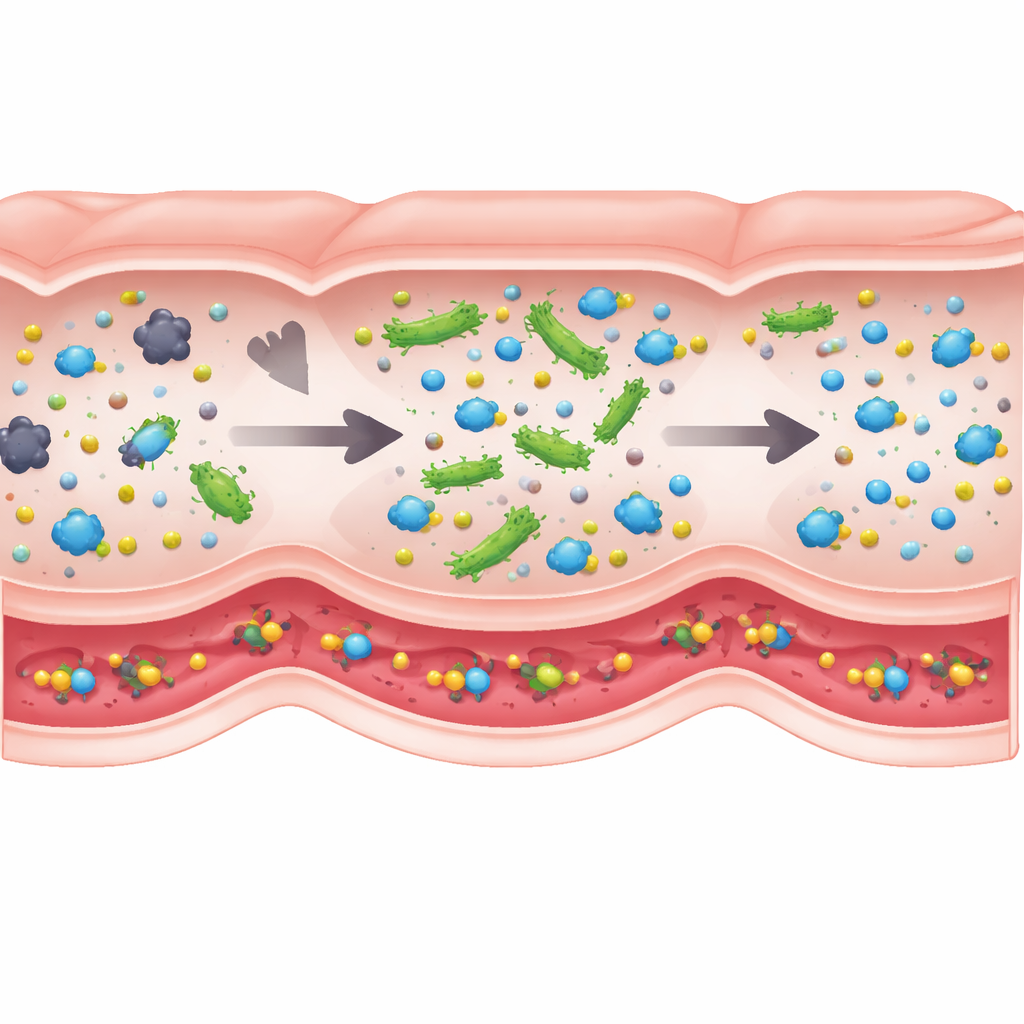
Ce qui compte le plus sous le capot
Tous les détails biologiques n’influencent pas le résultat de la même manière, aussi les auteurs ont-ils utilisé un type d’analyse de sensibilité globale pour déterminer quels ingrédients du modèle conduisent réellement au succès. Le grand gagnant fut la quantité d’enzyme active que chaque cellule probiotique peut porter. Les variations des temps de transit intestinal, des taux d’absorption, ou même de la densité bactérienne globale eurent des effets comparativement faibles dans des plages réalistes. Cela signifie que, lors de la conception de tels biothérapeutiques vivants, l’ingénierie de cellules produisant davantage de l’enzyme clé peut être bien plus importante que l’ajustement fin de leur vitesse de déplacement dans l’intestin. Cela suggère aussi que les recommandations de dosage issues de BCAT devraient être relativement robustes d’une personne à l’autre, malgré la variation de leurs vitesses de digestion et de leurs microbiotes.
D’un trouble à beaucoup d’autres
Au final, ce travail n’offre pas seulement des orientations pour un trouble rare et socialement pénalisant. Il introduit un cadre général et adaptable pour planifier et optimiser des thérapies microbiennes vivantes pour toute condition où le microbiome intestinal transforme des composés alimentaires ou d’origine corporelle en sous-produits nocifs. En rassemblant transit intestinal, chimie microbienne native et nettoyage enzymatique ingénieré en une image quantitative unique, le modèle BCAT peut suggérer des cibles de dosage réalistes et des stratégies temporelles bien avant qu’une souche n’atteigne les essais cliniques. Pour les patients et les cliniciens, cela rapproche la promesse que les futurs médicaments probiotiques seront non seulement naturels et bien acceptés, mais aussi prévisibles, modulables et fondés sur la même planification rigoureuse utilisée pour les médicaments conventionnels.
Citation: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Mots-clés: microbiote intestinal, thérapie probiotique, triméthylaminurie, modélisation mathématique, biothérapeutiques vivantes