Clear Sky Science · de
Unterzeichnet, versiegelt, geliefert: ein verallgemeinerbares Modell für Dosierung und Metabolismus lebender Biotherapeutika
Hilfreiche Keime als Medizin
Viele Menschen wissen, dass die Mikroben in unserem Darm die Gesundheit beeinflussen können, aber es ist weitaus weniger offensichtlich, wie man diese winzigen Mitbewohner in präzise, verlässliche Medizin verwandelt. Diese Studie beschäftigt sich mit einer sehr praktischen Frage: Wenn wir eine Kapsel mit gentechnisch verändertem „guten Bakterium“ schlucken, das eine schädliche Verbindung im Darm abbauen soll, wie viel sollten wir einnehmen und wann? Die Autoren entwickeln einen mathematischen Rahmen, der verbindet, was mit Nahrungsbestandteilen passiert, während sie durch Magen und Darm wandern, was unsere ansässigen Mikroben damit anstellen und wie ein zusätzliches probiotisches Stämmchen eingreifen kann, um den Körper zu schützen.
Eine Körpergeruchs-Störung als Testfall
Die Forscher konzentrieren sich auf Trimethylaminurie, manchmal „Fischgeruchssyndrom“ genannt. Bei dieser Erkrankung führen Mutationen in einem Leberenzym dazu, dass eine stark riechende Verbindung, Trimethylamin (TMA), nicht richtig neutralisiert wird und sich stattdessen in Schweiß, Atem und Urin ansammelt. TMA entsteht hauptsächlich im Darm, wenn Bakterien Nährstoffe wie Cholin aus gängigen Lebensmitteln wie Eiern und Fleisch abbauen. Gegenwärtige Behandlungen versuchen, das System dieser Nährstoffe zu berauben oder die Darmbakterien mit Antibiotika zu zerstören — Strategien, die schwer aufrechtzuerhalten sind und Nebenwirkungen haben können. Die Autoren untersuchen eine andere Idee: ein lebendes Biotherapeutikum hinzufügen — ein gentechnisch verändertes Bakterium, das ein Enzym trägt, das TMA direkt im Darm in eine harmlose, geruchslose Form umwandeln kann, bevor es in den Blutkreislauf gelangt.
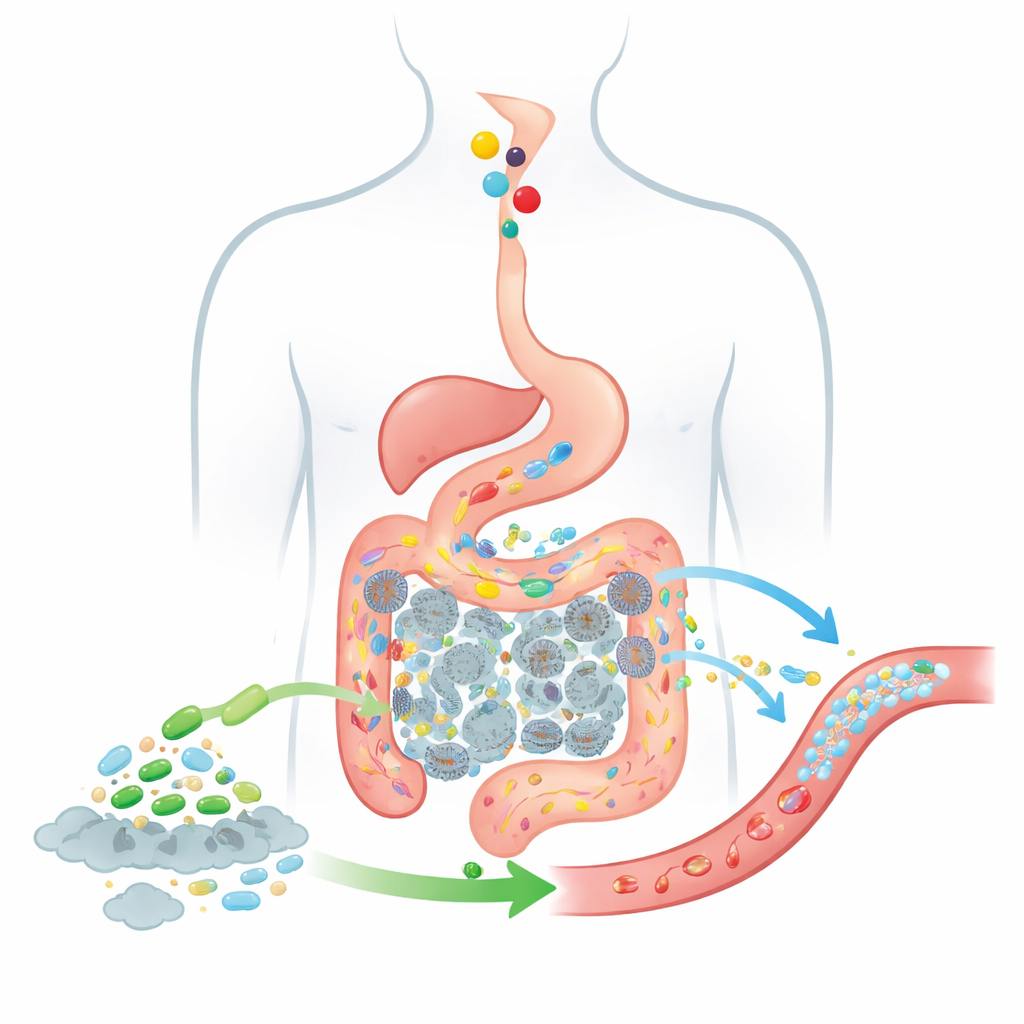
Lebensmittel und Bakterien durch den Darm verfolgen
Um vorherzusagen, wie gut eine solche lebende Therapie wirken könnte, erweitern die Autoren ein klassisches Modell zur Wirkstoffaufnahme, bekannt als CAT-Modell, das verfolgt, wie geschluckte Substanzen vom Magen durch Abschnitte des Dünndarms in den Dickdarm gelangen. Ihr aktualisiertes BCAT-Modell teilt den Darm in mehrere verbundene „Boxen“ auf, von denen jede einen Darmabschnitt oder den Kolon mit eigenem Flüssigkeitsvolumen, typischer bakterieller Anzahl und Absorptionsverhalten repräsentiert. Während die Nahrung von einer Box zur nächsten wandert, verfolgt das Modell, wie viel Cholin vorhanden ist, wie viel TMA Darmbakterien produzieren, welcher Anteil dieses TMA in das Blut übertritt und wie zugefügte probiotische Zellen entlang derselben Strecke reisen und wirken. Anders als frühere Modelle behandelt dieses Modell die probiotische Population als eine sich bewegende, sich verändernde Wolke von Zellen statt als festen Hintergrund, und es beinhaltet explizit den Kolon, in dem der überwiegende Teil des TMA erzeugt wird.
Abgleich des Modells mit realen Daten
Ein Modell ist nur nützlich, wenn es der Realität entspricht, daher testete das Team BCAT anhand menschlicher Daten. Zuerst fragten sie, ob das Modell klassische Ernährungsstudien aus den 1950er- bis 1990er-Jahren reproduzieren konnte, in denen Freiwillige gemessene Dosen Cholin zu sich nahmen und Forscher später TMA und seine neutralisierte Form im Urin analysierten. Über mehrere Dosen und unabhängige Studien hinweg schwankte der Anteil des in Trimethylamine umgewandelten Cholins um etwa zwei Drittel; BCAT erfasste dieses Muster erfolgreich. Anschließend wandten sie das Framework auf ein anderes gentechnisch verändertes Probiotikum, SYNB1618, an, das für die erbliche Erkrankung Phenylketonurie entwickelt wurde. Anhand klinischer Studiendaten darüber, wie viel eines diagnostischen Abbauprodukts im Urin der Probanden auftauchte, wichen die BCAT-Vorhersagen nur um etwa fünf Prozent ab und übertrafen damit deutlich einfachere, niedrig aufgelöste Modelle.
Wie viel Probiotikum und wann einnehmen?
Mit dieser Validierung im Gepäck ließen die Autoren BCAT auf Trimethylaminurie los. Sie fragten: Was ist die kleinste probiotische Dosis, die die gesamte TMA-Exposition im Blut um 95 Prozent senken kann, was ungefähr der natürlichen Reinigungsleistung eines gesunden Leberenzyms entspricht? Wenn Probiotikum und Mahlzeit gleichzeitig eingenommen werden, schlägt das Modell eine Dosis von etwa zehn Milliarden Zellen vor, ähnlich dem Inhalt einer typischen frei verkäuflichen Probiotika-Kapsel. Aber das Timing ist entscheidend. Da die ansässigen Darmbakterien bereits über den Kolon verteilt sind, während geschluckte Probiotika erst vom Magen dorthin gelangen müssen, gibt es eine Verzögerung, bis die Therapie am richtigen Ort ist. Simulationen zeigen, dass die Einnahme des Probiotikums etwa drei bis vier Stunden vor einer cholinreichen Mahlzeit es erlaubt, „früh anzukommen“, sich im Kolon zu verbreiten und TMA effektiver abzufangen. Unter diesem Zeitplan sinkt die erforderliche Dosis um etwa den Faktor vier, was die Sicherheitsbedenken bei sehr hohen mikrobiellen Lasten verringern könnte.
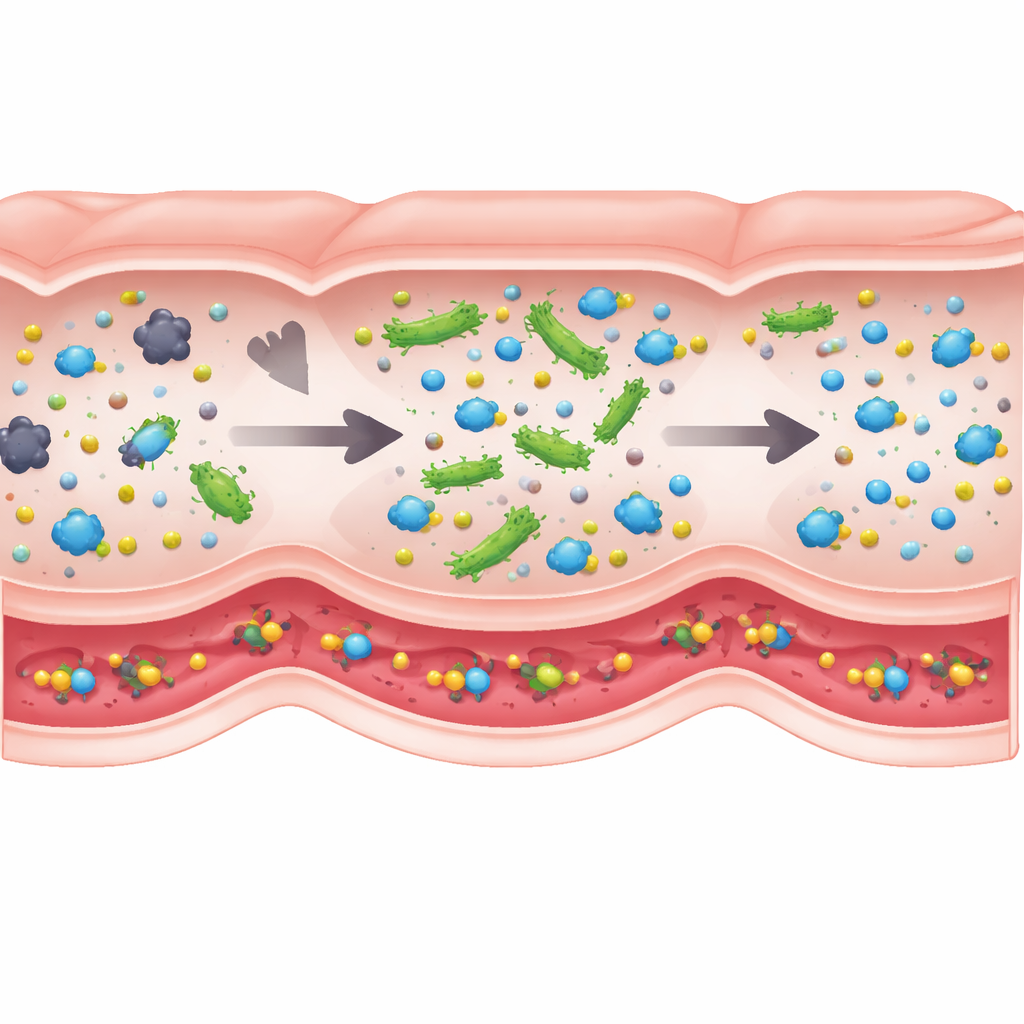
Was unter der Haube am wichtigsten ist
Nicht jedes biologische Detail beeinflusst das Ergebnis gleichermaßen, deshalb nutzten die Autoren eine Form der globalen Sensitivitätsanalyse, um zu sehen, welche Bausteine des Modells den Erfolg tatsächlich antreiben. Der klare Gewinner war die Menge des aktiven Enzyms, die jede probiotische Zelle tragen kann. Änderungen in Darmtransitzeiten, Absorptionsraten oder sogar der allgemeinen Bakteriendichte hatten innerhalb realistischer Bereiche vergleichsweise geringe Effekte. Das bedeutet, dass beim Entwurf solcher lebender Biotherapeutika die Ingenieursarbeit, Zellen zu entwickeln, die mehr des Schlüssel-Enzyms produzieren, weitaus wichtiger sein kann als das Feintuning ihrer Passagegeschwindigkeit durch den Darm. Es legt auch nahe, dass Dosierungsempfehlungen aus BCAT über verschiedene Personen hinweg relativ robust sein sollten, obwohl sich ihre Verdauungsgeschwindigkeiten und Mikrobiome unterscheiden.
Von einer Störung zu vielen
Am Ende bietet diese Arbeit nicht nur Orientierung für eine seltene und sozial belastende Geruchsstörung. Sie führt einen allgemeinen, anpassbaren Rahmen ein, um lebende mikrobiologische Therapien für jede Erkrankung zu planen und zu optimieren, bei der das Darmmikrobiom diätbedingte oder körpereigene Verbindungen in schädliche Nebenprodukte verwandelt. Indem Transit im Darm, die Chemie der einheimischen Mikroben und enzymatische Aufräumarbeit gentechnisch veränderter Zellen zu einem quantitativen Gesamtbild verknüpft werden, kann das BCAT-Modell realistische Dosierungsziele und Zeitstrategien vorschlagen — lange bevor ein Stamm klinische Studien erreicht. Für Patienten und Kliniker bedeutet das die Aussicht, dass zukünftige Probiotika nicht nur freundlich und natürlich klingend, sondern auch vorhersehbar, steuerbar und auf derselben rigorosen Planung beruhend sein werden wie konventionelle Arzneimittel.
Zitation: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Schlüsselwörter: Darmmikrobiom, Probiotische Therapie, Trimethylaminurie, Mathematische Modellierung, Lebende Biotherapeutika