Clear Sky Science · nl
Ondertekend, verzegeld, bezorgd: een generaliseerbaar model voor dosering en metabolisme van levende biotherapeutica
Goede microben omzetten in medicijnen
Veel mensen weten dat de microben in onze darm de gezondheid kunnen beïnvloeden, maar het is veel minder duidelijk hoe je die kleine passagiers kunt omzetten in precieze, betrouwbare medicijnen. Deze studie pakt een heel praktische vraag aan: als we een capsule doorslikken met een gemodificeerde “goede bacterie” die bedoeld is om een schadelijke stof in de darm op te ruimen, hoeveel moeten we er nemen en wanneer moeten we die innemen? De auteurs bouwen een wiskundig raamwerk dat verbindt wat er met voedsel gebeurt terwijl het door maag en darmen beweegt, wat onze residentiële microben ermee doen, en hoe een toegevoegde probiotische stam kan ingrijpen om het lichaam te beschermen.
Een lichaamsgeurstoornis als casus
De onderzoekers richten zich op trimethylaminurie, soms “visgeur-syndroom” genoemd. Bij deze aandoening zorgen mutaties in een leverenzym ervoor dat een sterk ruikende verbinding, trimethylamine (TMA), niet goed geneutraliseerd wordt en zich in plaats daarvan ophoopt in zweet, adem en urine. TMA wordt grotendeels in de darm gemaakt wanneer bacteriën voedingsstoffen zoals choline uit veelvoorkomende voedingsmiddelen als eieren en vlees afbreken. Huidige behandelingen proberen het systeem van deze voedingsstoffen te beroven of de darmbacteriën te doden met antibiotica — strategieën die moeilijk vol te houden zijn en bijwerkingen kunnen geven. De auteurs verkennen een ander idee: voeg een levende biotherapeutische product toe — een gemodificeerde bacterie die een enzym draagt dat TMA in de darm kan omzetten in een onschadelijke, reukloze vorm voordat het de bloedbaan kan bereiken.
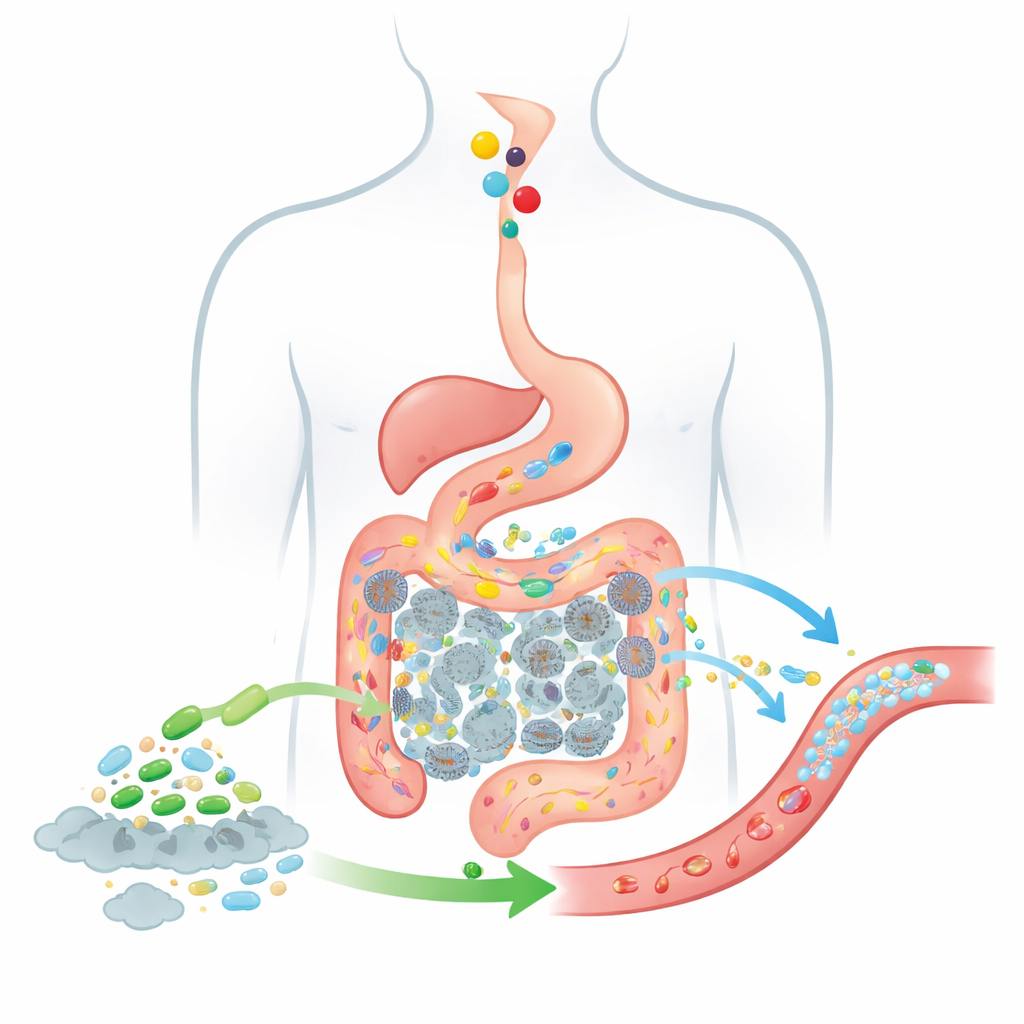
Voedsel en bacteriën volgen door de darm
Om te voorspellen hoe goed zo’n levende therapie zou kunnen werken, breiden de auteurs een klassiek model voor geneesmiddelabsorptie uit, bekend als het CAT-model, dat bijhoudt hoe doorgeslikte stoffen van de maag door segmenten van de dunne darm naar de dikke darm bewegen. Hun bijgewerkte BCAT-model deelt de darm op in meerdere verbonden “boxen”, elk representatief voor een stuk dunne darm of colon met een eigen vloeistofvolume, typische aantallen bacteriën en absorptiegedrag. Terwijl voedsel van de ene box naar de volgende passeert, houdt het model bij hoeveel choline aanwezig is, hoeveel TMA darmbacteriën produceren, hoeveel van dat TMA in het bloed overgaat, en hoe toegevoegde probiotische cellen hetzelfde traject afleggen en handelen. In tegenstelling tot eerdere modellen behandelt dit model de probiotische populatie als een bewegende, veranderende wolk cellen in plaats van als een vaste achtergrond, en het omvat expliciet het colon, waar de overgrote meerderheid van TMA wordt geproduceerd.
Het model toetsen aan real-world data
Een model is alleen nuttig als het overeenkomt met de werkelijkheid, dus het team testte BCAT aan de hand van menselijke gegevens. Eerst vroegen ze of het model klassieke voedingsstudies uit de jaren 1950 tot 1990 kon reproduceren, waarin vrijwilligers gemeten doses choline aten en onderzoekers later TMA en de geneutraliseerde vorm in urine verzamelden en analyseerden. Over meerdere dosisniveaus en onafhankelijke studies zweefde het aandeel choline dat in trimethylamines werd omgezet rond twee derde; BCAT wist dit patroon succesvol te vangen. Vervolgens pasten ze het raamwerk toe op een andere gemodificeerde probiotica, SYNB1618, ontworpen voor de erfelijke ziekte fenylketonurie. Met klinische onderzoeksgegevens over hoeveel van een diagnostisch afbraakproduct in de urine van proefpersonen verscheen, weekten BCAT-voorspellingen slechts ongeveer 5 procent af, wat de prestaties verre overtrof van eenvoudigere, laagresolutie modellen.
Hoeveel probiotica en wanneer innemen?
Met deze validatie in de hand lieten de auteurs BCAT los op trimethylaminurie. Ze vroegen: wat is de kleinste probiotische dosis die de totale TMA-blootstelling in het bloed met 95 procent kan verminderen, wat ruwweg overeenkomt met de natuurlijke opruimkracht van een gezond leverenzym? Wanneer probiotica en maaltijd samen worden ingenomen, suggereert het model een dosis rond tien miljard cellen, vergelijkbaar met wat in een typische vrij verkrijgbare probiotische capsule past. Maar timing doet ertoe. Omdat residentiële darmbacteriën al in het colon gevestigd zijn terwijl doorgeslikte probiotica daarheen moeten reizen vanuit de maag, is er een vertraging voordat de therapie op de juiste plaats is. Simulaties tonen aan dat het innemen van de probiotica ongeveer drie tot vier uur vóór een choline-rijke maaltijd het mogelijk maakt dat ze “vroeg arriveren”, zich door het colon verspreiden en TMA effectiever onderscheppen. Onder dit schema daalt de vereiste dosis ruwweg met een factor vier, wat veiligheidszorgen over zeer hoge microbieële belastingen zou kunnen verminderen.
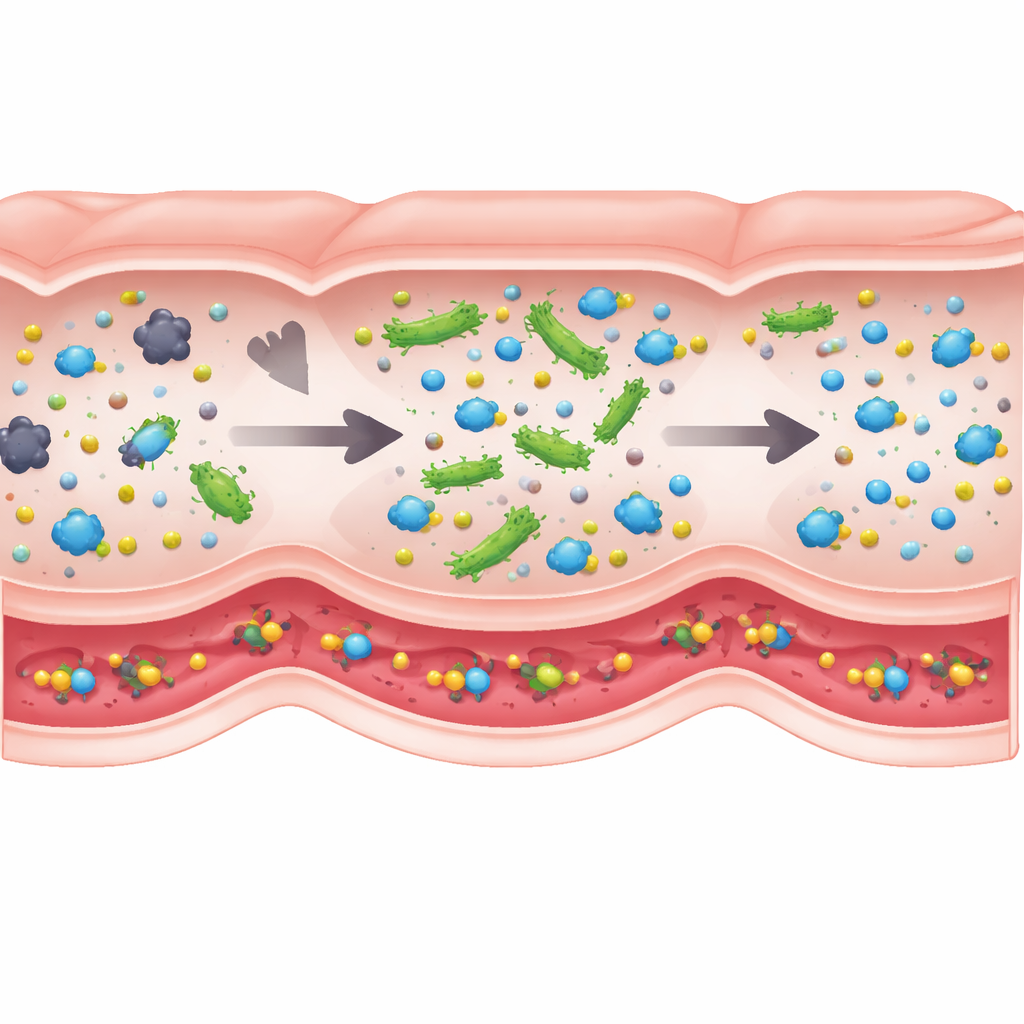
Wat onder de motorkap het meest telt
Niet elk biologisch detail beïnvloedt het resultaat in gelijke mate, dus gebruikten de auteurs een vorm van globale gevoeligheidsanalyse om te zien welke ingrediënten van het model daadwerkelijk succes aansturen. De duidelijke winnaar was de hoeveelheid actief enzym die elke probiotische cel kan dragen. Veranderingen in darmtransittijden, absorptiesnelheden of zelfs de totale bacteriële dichtheid hadden binnen realistische grenzen relatief kleine effecten. Dit betekent dat bij het ontwerpen van dergelijke levende biotherapeutica het engineereren van cellen die meer van het sleutelenzym produceren veel belangrijker kan zijn dan het fijnafstellen van hoe snel ze door de darm bewegen. Het suggereert ook dat dosisaanbevelingen uit BCAT redelijk robuust zouden moeten zijn voor verschillende mensen, ook al variëren hun spijsverteringssnelheden en microbiomen.
Van één aandoening naar vele
Uiteindelijk biedt dit werk niet alleen richtlijnen voor een zeldzame en sociaal belastende geurstoornis. Het introduceert een algemeen, aanpasbaar raamwerk voor het plannen en optimaliseren van levende microbiele therapieën voor elke aandoening waarbij het darmmicrobioom dieet- of lichaamsafgeleide verbindingen omzet in schadelijke bijproducten. Door darmtransit, native microbiële chemie en gemodificeerde enzymatische opruiming samen te brengen in één kwantitatief beeld, kan het BCAT-model realistische doseringsdoelen en timingstrategieën suggereren ver voordat een stam klinische proeven bereikt. Voor patiënten en clinici brengt dit de belofte dichterbij dat toekomstige probiotische medicijnen niet alleen vriendelijk en natuurlijk klinken, maar ook voorspelbaar, afstelbaar en verankerd in hetzelfde soort rigoureuze planning dat voor conventionele geneesmiddelen wordt gebruikt.
Bronvermelding: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Trefwoorden: darmmicrobioom, probiotische therapie, trimethylaminurie, wiskundige modellering, levende biotherapeutica