Clear Sky Science · es
Firmado, sellado, entregado: un modelo generalizable para la dosificación y el metabolismo de bioterapéuticos vivos
Convertir microbios útiles en medicina
Mucha gente sabe que los microbios en nuestro intestino pueden afectar la salud, pero es mucho menos evidente cómo transformar esos pequeños pasajeros en medicamentos precisos y fiables. Este estudio aborda una cuestión muy práctica: si nos tomamos una cápsula de “bacterias buenas” diseñadas para eliminar un compuesto nocivo en el intestino, ¿cuánto debemos tomar y cuándo? Los autores construyen un marco matemático que conecta lo que le ocurre a la comida mientras atraviesa el estómago y el intestino, lo que hacen nuestras bacterias residentes con ella y cómo una cepa probiótica añadida puede intervenir para proteger el organismo.
Un trastorno del olor corporal como caso de prueba
Los investigadores se centran en la trimetilaminuria, a veces llamada “síndrome del olor a pescado”. En esta condición, mutaciones en una enzima hepática hacen que un compuesto de olor fuerte, la trimetilamina (TMA), no se neutralice correctamente y en su lugar se acumule en el sudor, el aliento y la orina. La TMA se produce sobre todo en el intestino cuando las bacterias descomponen nutrientes como la colina, presentes en alimentos comunes como huevos y carne. Los tratamientos actuales tratan de privar al sistema de estos nutrientes o de matar las bacterias intestinales con antibióticos, estrategias difíciles de mantener y que pueden causar efectos secundarios. Los autores exploran una idea distinta: añadir un producto bioterapéutico vivo—una bacteria diseñada que porta una enzima capaz de convertir la TMA en una forma inofensiva y sin olor directamente en el intestino antes de que pase a la sangre.
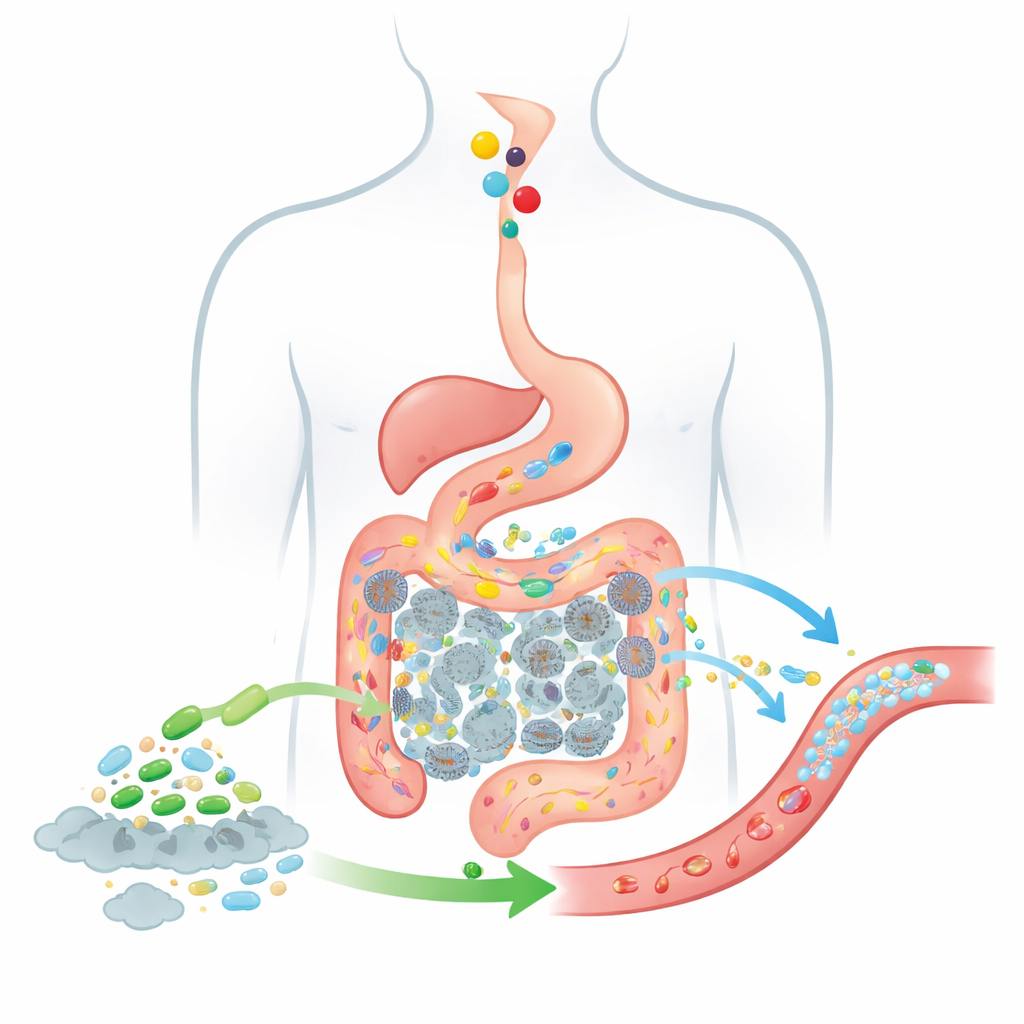
Seguir la comida y las bacterias a través del intestino
Para predecir cuán bien podría funcionar una terapia viva así, los autores amplían un modelo clásico de absorción de fármacos conocido como modelo CAT, que rastrea cómo las sustancias ingeridas se mueven desde el estómago a segmentos del intestino delgado y hasta el colon. Su modelo BCAT actualizado divide el intestino en múltiples “cajas” conectadas, cada una representando un tramo de intestino o colon con su propio volumen de fluido, números típicos de bacterias y comportamiento de absorción. A medida que la comida pasa de una caja a la siguiente, el modelo contabiliza cuánta colina está presente, cuánto TMA producen las bacterias intestinales, qué parte de esa TMA cruza al torrente sanguíneo y cómo viajan y actúan las células probióticas añadidas a lo largo de la misma ruta. A diferencia de modelos anteriores, éste trata a la población probiótica como una nube móvil y cambiante de células en lugar de un trasfondo fijo, e incluye explícitamente el colon, donde se genera la gran mayoría de la TMA.
Comprobar el modelo con datos del mundo real
Un modelo sólo es útil si coincide con la realidad, así que el equipo probó BCAT contra datos humanos. Primero, preguntaron si el modelo podía reproducir estudios clásicos de nutrición desde los años 50 hasta los 90, en los que voluntarios comían dosis medidas de colina y los investigadores recogían y analizaban después la TMA y su forma neutralizada en la orina. A través de varios niveles de dosis y estudios independientes, la fracción de colina transformada en trimetilaminas rondaba aproximadamente dos tercios; BCAT capturó con éxito este patrón. A continuación, aplicaron el marco a otro probiótico diseñado, SYNB1618, desarrollado para la enfermedad hereditaria fenilcetonuria. Usando datos de ensayos clínicos sobre cuánto producto de degradación diagnóstico apareció en la orina de los sujetos, las predicciones de BCAT diferían sólo en torno a un 5 por ciento, superando con creces a modelos más simples y de baja resolución.
¿Cuánto probiótico y cuándo tomarlo?
Con esta validación, los autores aplicaron BCAT a la trimetilaminuria. Preguntaron: ¿Cuál es la dosis mínima de probiótico capaz de reducir la exposición total a TMA en la sangre en un 95 por ciento, aproximándose al poder de limpieza natural de una enzima hepática sana? Cuando el probiótico y la comida se toman juntos, el modelo sugiere una dosis alrededor de diez mil millones de células, similar a la que cabe en una cápsula probiótica de venta libre típica. Pero el momento importa. Dado que las bacterias residentes ya están establecidas a lo largo del colon mientras que los probióticos ingeridos deben viajar desde el estómago, hay un retraso antes de que la terapia esté en el lugar adecuado. Las simulaciones muestran que tomar el probiótico unas tres o cuatro horas antes de una comida rica en colina le permite “llegar antes”, dispersarse por el colon e interceptar la TMA con mayor eficacia. Con este calendario, la dosis requerida se reduce en aproximadamente un factor de cuatro, lo que podría disminuir las preocupaciones de seguridad sobre cargas microbianas muy elevadas.
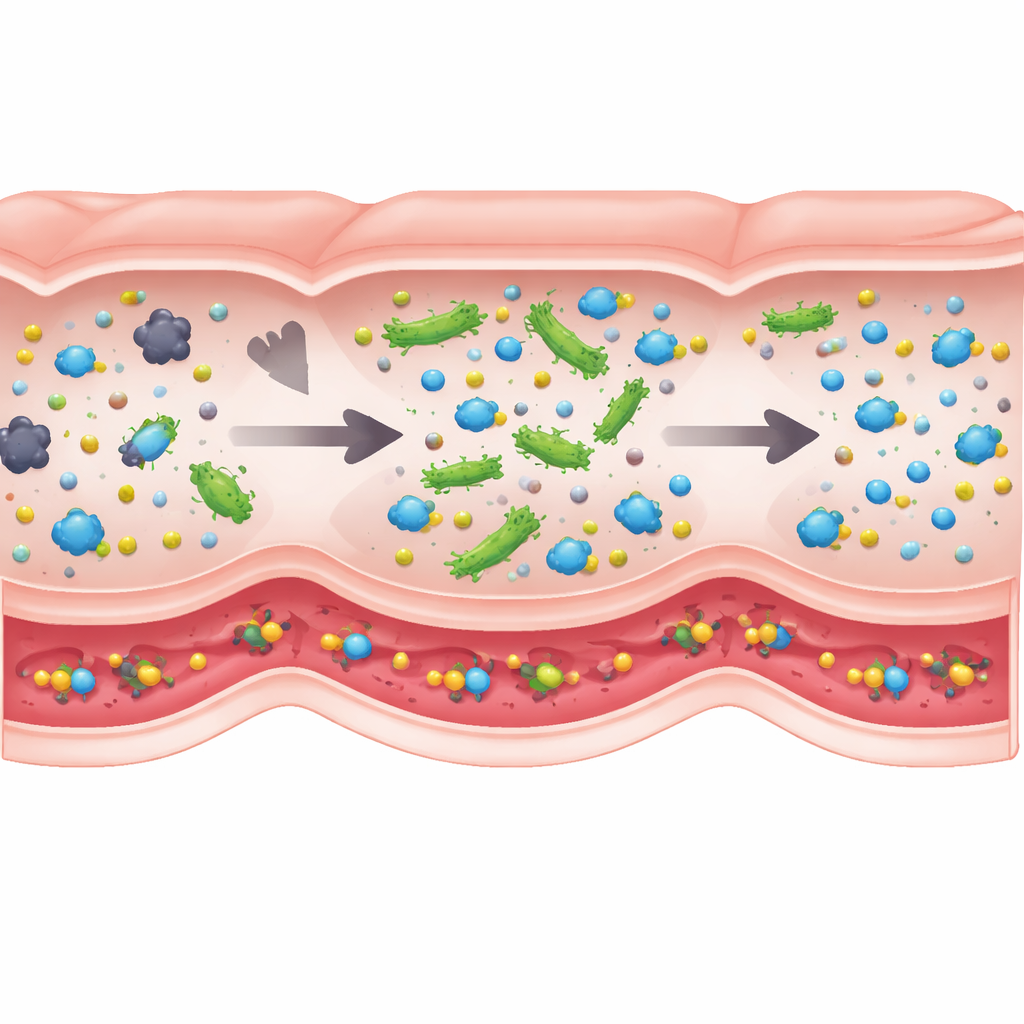
Qué importa más en el interior
No todos los detalles biológicos influyen por igual en el resultado, por lo que los autores emplearon un tipo de análisis de sensibilidad global para ver qué ingredientes del modelo realmente impulsan el éxito. El claro ganador fue la cantidad de enzima activa que puede portar cada célula probiótica. Los cambios en los tiempos de tránsito intestinal, en las tasas de absorción o incluso en la densidad bacteriana total tuvieron efectos comparativamente pequeños dentro de rangos realistas. Esto significa que, al diseñar bioterapéuticos vivos de este tipo, es probable que sea mucho más importante ingenierizar células que produzcan más de la enzima clave que afinar la velocidad a la que se mueven por el intestino. También sugiere que las recomendaciones de dosificación derivadas de BCAT deberían ser bastante robustas entre diferentes personas, aunque varíen en su velocidad de digestión y en sus microbiomas.
De un trastorno a muchos
Al final, este trabajo no sólo ofrece orientación para un trastorno raro y socialmente angustiante del olor. Introduce un marco general y adaptable para planificar y optimizar terapias microbianas vivas para cualquier condición en la que el microbioma intestinal convierta compuestos dietéticos o derivados del propio cuerpo en subproductos dañinos. Al entrelazar el tránsito intestinal, la química microbiana nativa y la limpieza enzimática diseñada en una sola imagen cuantitativa, el modelo BCAT puede sugerir objetivos de dosificación y estrategias de temporalización realistas mucho antes de que una cepa llegue a ensayos clínicos. Para pacientes y clínicos, esto acerca la promesa de que los futuros medicamentos probióticos no sólo suenen amigables y naturales, sino que además sean previsibles, ajustables y fundamentados en el mismo tipo de planificación rigurosa que se usa para los fármacos convencionales.
Cita: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Palabras clave: microbioma intestinal, terapia probiótica, trimetilaminuria, modelado matemático, bioterapéuticos vivos