Clear Sky Science · pt
Assinado, lacrado, entregue: um modelo generalizável para dosagem e metabolismo de bioterapêuticos vivos
Transformando Germes Úteis em Medicina
Muitas pessoas sabem que os microrganismos no nosso intestino podem afetar a saúde, mas é bem menos óbvio como transformar esses pequenos passageiros em medicamentos precisos e confiáveis. Este estudo aborda uma questão muito prática: se engolirmos uma cápsula de “bactérias boas” modificadas para eliminar um químico nocivo no intestino, quanto devemos tomar e quando? Os autores constroem uma estrutura matemática que conecta o que acontece com os alimentos enquanto se movem pelo estômago e intestinos, o que nossos micróbios residentes fazem com eles e como uma cepa probiótica adicionada pode intervir para proteger o corpo.
Um Distúrbio de Odor Corporal como Caso de Teste
Os pesquisadores focam na trimetilaminúria, às vezes chamada de “síndrome do odor de peixe”. Nessa condição, mutações em uma enzima do fígado fazem com que um composto de cheiro forte, a trimetilamina (TMA), não seja neutralizado adequadamente e, em vez disso, se acumule no suor, hálito e urina. A TMA é formada principalmente no intestino quando bactérias degradam nutrientes como a colina, presentes em alimentos comuns como ovos e carne. Tratamentos atuais tentam privar o sistema desses nutrientes ou eliminar bactérias intestinais com antibióticos — estratégias difíceis de manter e que podem causar efeitos colaterais. Os autores exploram uma ideia diferente: adicionar um produto bioterapêutico vivo — uma bactéria engenheirada que carrega uma enzima capaz de converter a TMA em uma forma inofensiva e sem odor diretamente no intestino antes que ela entre na corrente sanguínea.
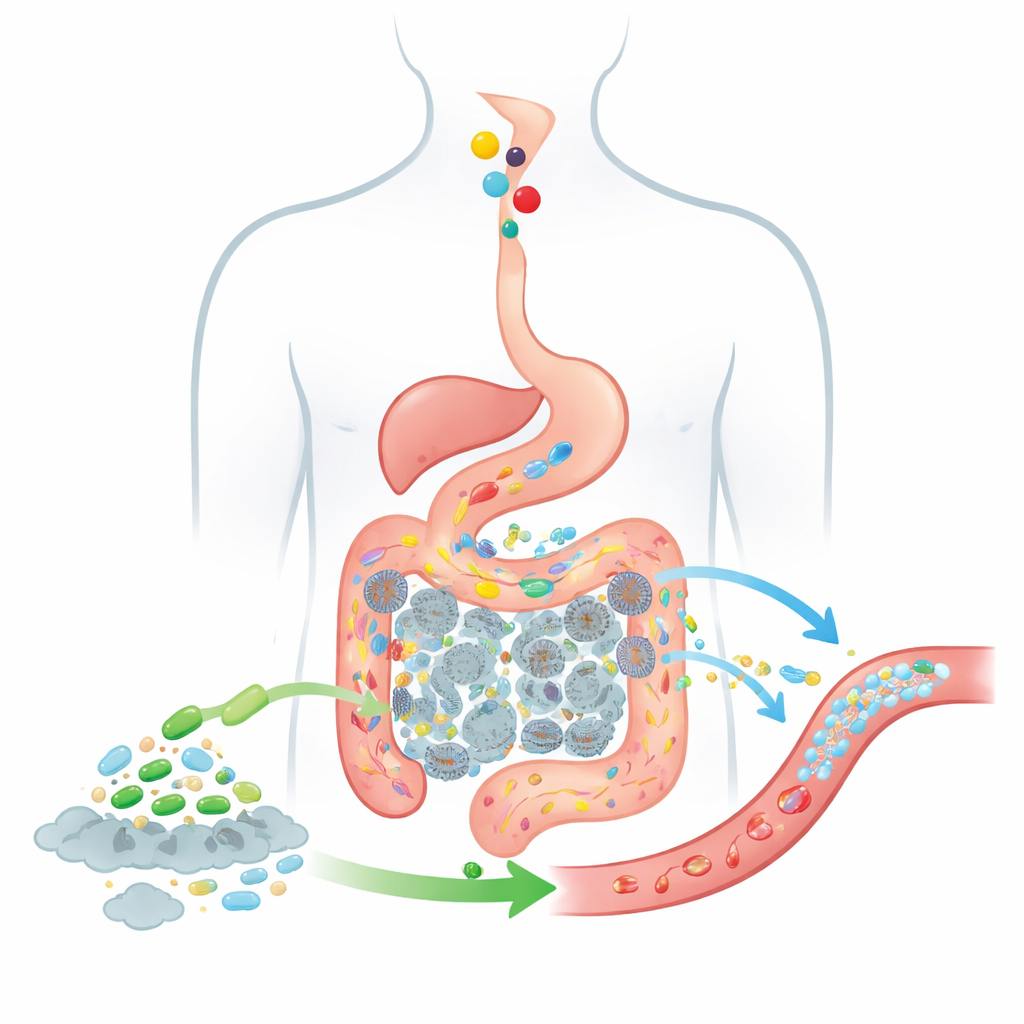
Acompanhando Alimentos e Bactérias pelo Intestino
Para prever quão eficaz tal terapia viva poderia ser, os autores estendem um modelo clássico de absorção de drogas conhecido como modelo CAT, que acompanha como substâncias ingeridas se movem do estômago por segmentos do intestino delgado até o cólon. O modelo atualizado BCAT divide o intestino em múltiplas “caixas” conectadas, cada uma representando um trecho do intestino ou do cólon com seu próprio volume de fluido, número típico de bactérias e comportamento de absorção. À medida que o alimento passa de uma caixa para a próxima, o modelo acompanha quanta colina está presente, quanto de TMA as bactérias intestinais produzem, quanto dessa TMA cruza para o sangue e como as células probióticas adicionadas viajam e atuam ao longo da mesma rota. Diferentemente de modelos anteriores, este trata a população probiótica como uma nuvem móvel e mutável de células em vez de um fundo fixo, e inclui explicitamente o cólon, onde a grande maioria da TMA é gerada.
Conferindo o Modelo com Dados do Mundo Real
Um modelo só é útil se corresponder à realidade, então a equipe testou o BCAT com dados humanos. Primeiro, perguntaram se o modelo poderia reproduzir estudos clássicos de nutrição das décadas de 1950 a 1990, nos quais voluntários consumiam doses medidas de colina e os pesquisadores depois coletavam e analisavam a TMA e sua forma neutralizada na urina. Em vários níveis de dose e estudos independentes, a fração de colina convertida em trimetilaminas girava em torno de dois terços; o BCAT capturou esse padrão com sucesso. Em seguida, aplicaram a estrutura a um probiótico engenheirado diferente, o SYNB1618, projetado para a doença hereditária fenilcetonúria. Usando dados de ensaios clínicos sobre quanto de um produto de decomposição diagnóstico aparecia na urina dos voluntários, as previsões do BCAT diferiram em apenas cerca de 5%, superando largamente modelos mais simples e de baixa resolução.
Quanto Probiótico e Quando Tomá-lo?
Com essa validação em mãos, os autores aplicaram o BCAT à trimetilaminúria. Perguntaram: qual é a menor dose probiótica que pode reduzir a exposição total de TMA no sangue em 95%, aproximadamente igualando o poder de limpeza natural de uma enzima hepática saudável? Quando probiótico e refeição são tomados juntos, o modelo sugere uma dose na ordem de dez bilhões de células, similar ao que cabe numa cápsula probiótica de venda livre. Mas o timing importa. Como as bactérias residentes já estão estabelecidas por todo o cólon enquanto os probióticos engolidos precisam viajar do estômago até lá, há um atraso antes que a terapia esteja no lugar certo. As simulações mostram que tomar o probiótico cerca de três a quatro horas antes de uma refeição rica em colina permite que ele “chegue cedo”, se espalhe pelo cólon e intercepte a TMA de forma mais eficaz. Nesse esquema, a dose necessária cai em aproximadamente um fator de quatro, o que pode reduzir preocupações de segurança relacionadas a cargas microbianas muito altas.
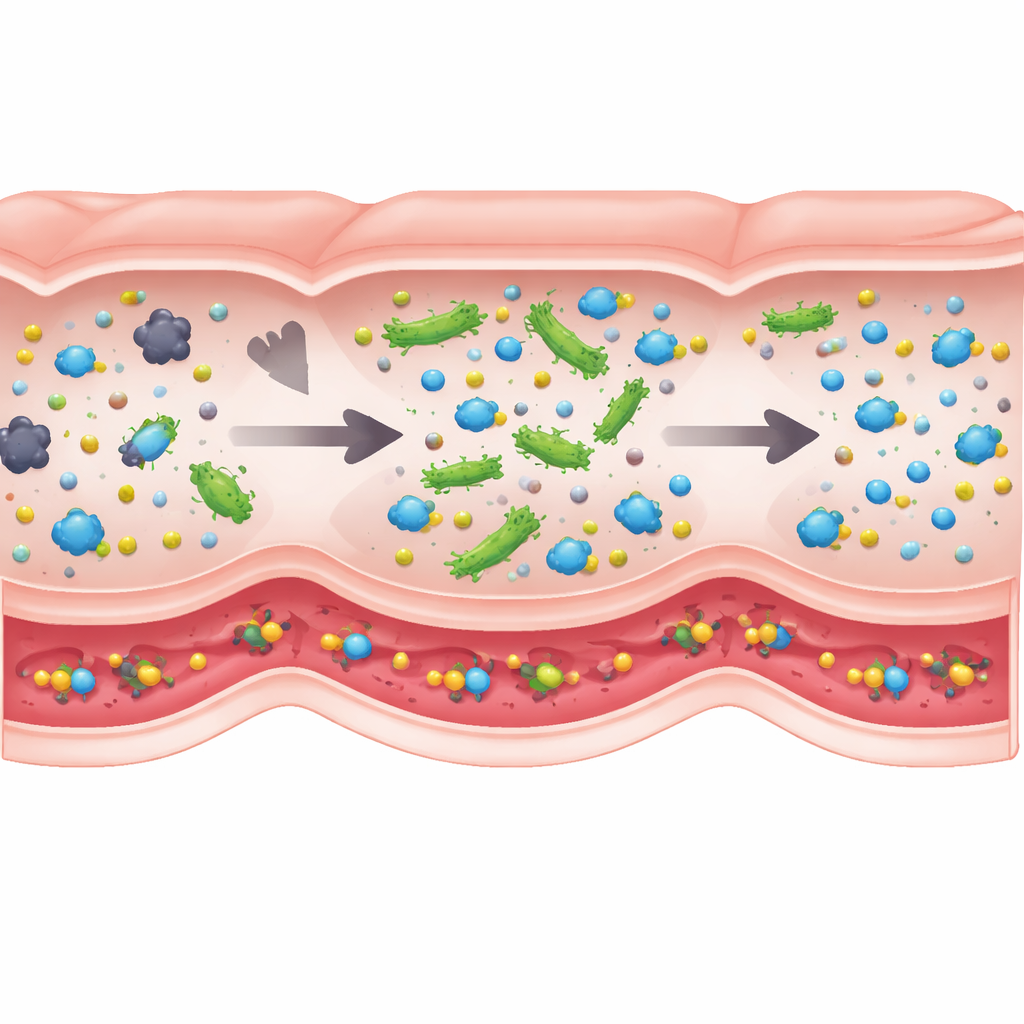
O Que Mais Importa nos Bastidores
Nem todo detalhe biológico influencia o resultado igualmente, então os autores usaram um tipo de análise de sensibilidade global para ver quais ingredientes do modelo realmente impulsionam o sucesso. O claro vencedor foi a quantidade de enzima ativa que cada célula probiótica pode carregar. Mudanças nos tempos de trânsito intestinal, nas taxas de absorção ou mesmo na densidade bacteriana total tiveram efeitos comparativamente pequenos dentro de faixas realistas. Isso significa que, ao projetar tais bioterapêuticos vivos, engenheirar células que produzam mais da enzima-chave pode ser muito mais importante do que ajustar finamente a velocidade com que elas se movem pelo intestino. Também sugere que as recomendações de dosagem do BCAT devem ser relativamente robustas entre diferentes pessoas, mesmo que seus ritmos digestivos e microbiomas variem.
De Um Distúrbio para Muitos
No fim, este trabalho não oferece apenas orientação para um distúrbio raro e socialmente constrangedor de odor. Introduz uma estrutura geral e adaptável para planejar e otimizar terapias microbianas vivas para qualquer condição em que o microbioma intestinal transforme compostos alimentares ou derivados do corpo em subprodutos nocivos. Ao unir trânsito intestinal, química microbiana nativa e limpeza enzimática engenheirada em um quadro quantitativo, o modelo BCAT pode sugerir metas de dosagem e estratégias de temporização realistas muito antes de uma cepa chegar a ensaios clínicos. Para pacientes e clínicos, isso traz a promessa de que futuros medicamentos probióticos serão não apenas parecidos com algo natural e bem aceitos, mas também previsíveis, ajustáveis e fundamentados no mesmo tipo de planejamento rigoroso usado para medicamentos convencionais.
Citação: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Palavras-chave: microbioma intestinal, terapia probiótica, trimetilaminúria, modelagem matemática, bioterapêuticos vivos