Clear Sky Science · ru
Подписано, опечатано, доставлено: универсальная модель дозирования и метаболизма живых биотерапевтических препаратов
Преобразование полезных микробов в лекарство
Многие знают, что микроорганизмы в кишечнике влияют на здоровье, но гораздо менее очевидно, как превратить этих крошечных пассажиров в точное, надёжное лекарство. В этом исследовании решается вполне практический вопрос: если мы проглатываем капсулу с модифицированными «полезными бактериями», предназначенную для нейтрализации вредного соединения в кишечнике, сколько нужно принять и когда это лучше сделать? Авторы создают математическую структуру, которая связывает то, что происходит с пищей при прохождении через желудок и кишечник, действия наших собственных микроорганизмов и то, как добавленная пробиотическая штамм может вмешаться, чтобы защитить организм.
Нарушение запаха тела как тестовый случай
Исследователи сосредотачиваются на триметиламинурии, иногда называемой «синдромом рыбного запаха». При этом состоянии мутации в печёночном ферменте означают, что сильно пахнущее соединение — триметиламин (TMA) — не нейтрализуется должным образом и накапливается в поте, дыхании и моче. TMA в основном образуется в кишечнике, когда бактерии расщепляют питательные вещества, такие как холин, из обычных продуктов вроде яиц и мяса. Современные методы лечения пытаются лишить систему этих веществ или уничтожить кишечные бактерии антибиотиками — стратегии, которые трудно поддерживать и которые могут вызывать побочные эффекты. Авторы рассматривают другую идею: добавить живой биотерапевтический продукт — инженерную бактерию, несущую фермент, способный превращать TMA в безвредную, не имеющую запаха форму прямо в кишечнике до того, как он попадёт в кровь.
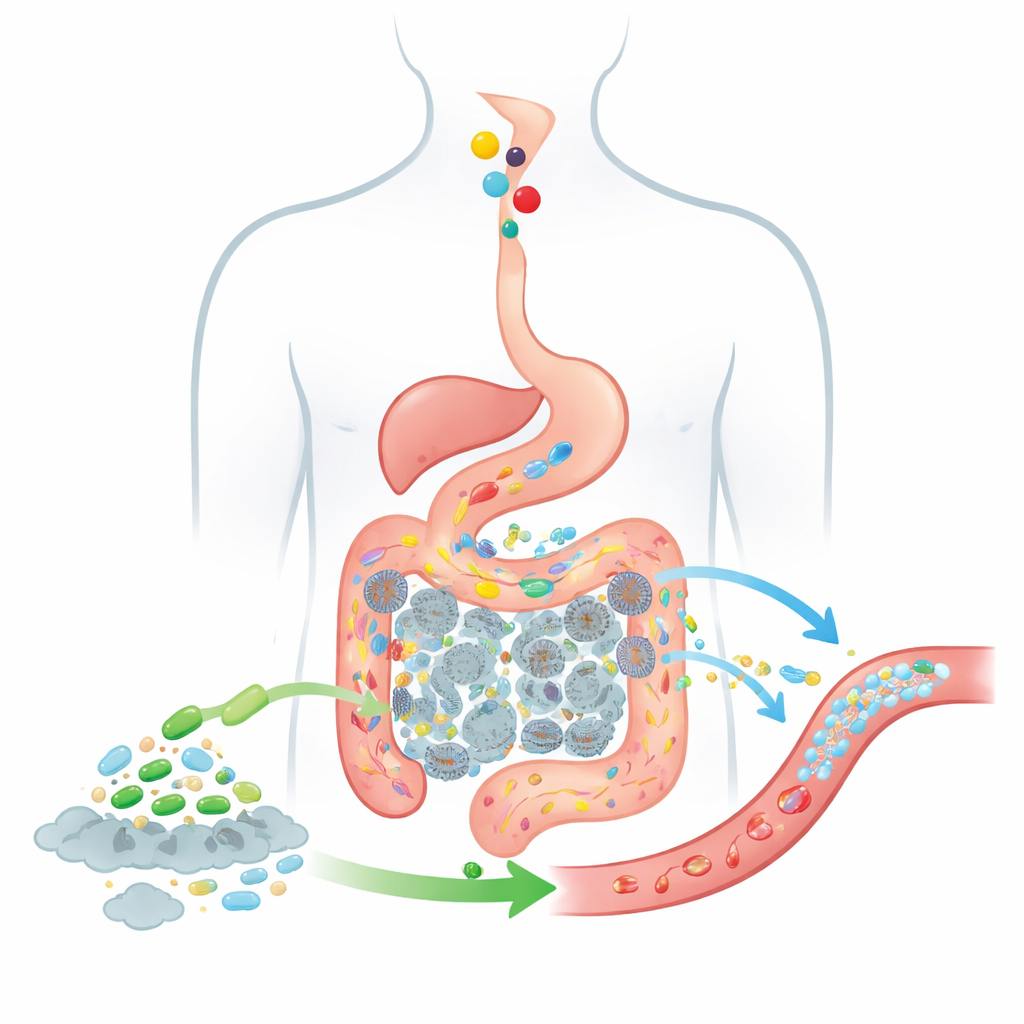
Отслеживание пищи и бактерий по кишечнику
Чтобы предсказать, насколько эффективно такая живая терапия может сработать, авторы расширяют классическую модель всасывания лекарств, известную как модель CAT, которая отслеживает, как проглоченные вещества перемещаются из желудка через сегменты тонкого кишечника и в толстую кишку. Их обновлённая модель BCAT делит кишечник на несколько связанных «коробок», каждая из которых представляет участок кишечника или толстой кишки со своим объёмом жидкости, типичными числами бактерий и поведением при абсорбции. По мере перехода пищи из одной коробки в другую модель учитывает, сколько холина присутствует, сколько TMA производят кишечные бактерии, какая часть этого TMA проникает в кровь и как добавленные клетки пробиотика перемещаются и действуют по тому же маршруту. В отличие от ранних моделей, эта рассматривает популяцию пробиотика как движущееся, изменяющееся облако клеток, а не как фиксированный фон, и явно включает толстую кишку, где генерируется подавляющая часть TMA.
Проверка модели на реальных данных
Модель полезна лишь тогда, когда соответствует реальности, поэтому команда протестировала BCAT на данных людей. Сначала они проверили, может ли модель воспроизвести классические нутритивные исследования с 1950-х по 1990-е годы, где добровольцы ели измеренные дозы холина, а исследователи позднее собирали и анализировали TMA и его нейтрализованную форму в моче. При разных уровнях доз и в независимых исследованиях доля холина, превращавшегося в триметиламины, держалась примерно на двух третях; BCAT успешно уловила эту закономерность. Затем они применили модель к другому инженерному пробиотику, SYNB1618, разработанному для наследственного заболевания фенилкетонурии. Используя данные клинических испытаний о том, какое количество диагностического продукта распада появлялось в моче участников, прогнозы BCAT отличались примерно на 5 процентов, существенно опережая более простые модели низкого разрешения.
Сколько пробиотика и когда его принимать?
Имея эту валидацию, авторы применили BCAT к триметиламинурии. Они задали вопрос: какая минимальная доза пробиотика может уменьшить общее воздействие TMA в крови на 95 процентов, что примерно соответствует естественной способности печёночного фермента к очистке? Когда пробиотик и приём пищи принимаются одновременно, модель указывает на дозу порядка десяти миллиардов клеток, близкую к тому, что помещается в типичную безрецептурную капсулу пробиотика. Но время приёма имеет значение. Поскольку резидентные кишечные бактерии уже обосновались по всей толстой кишке, а проглоченным пробиотикам нужно добраться туда из желудка, возникает задержка, прежде чем терапия окажется в нужном месте. Симуляции показывают, что приём пробиотика примерно за три–четыре часа до приёма пищи, богатой холином, позволяет ему «прибыть заранее», распространиться по толстой кишке и эффективнее перехватывать TMA. При таком расписании требуемая доза снижается примерно в четыре раза, что может уменьшить беспокойство по поводу безопасности при очень высоких микробных нагрузках.
Что важнее всего внутри модели
Не каждая биологическая деталь одинаково влияет на результат, поэтому авторы использовали вид глобального анализа чувствительности, чтобы выяснить, какие составляющие модели действительно определяют успех. Явным победителем стало количество активного фермента, которое может нести каждая клетка пробиотика. Изменения времени прохождения по кишечнику, скоростей абсорбции или даже общей плотности бактерий имели сравнительно небольшое влияние в реалистичных пределах. Это означает, что при разработке таких живых биотерапевтических средств увеличение производства ключевого фермента в клетках может быть гораздо важнее, чем тонкая настройка их скорости перемещения по кишечнику. Также это предполагает, что рекомендации по дозированию из BCAT должны быть достаточно устойчивыми для разных людей, несмотря на вариации в скорости пищеварения и микробиоме.
От одного расстройства к многим
В конечном итоге эта работа предлагает не только руководство для редкого и социально неприятного расстройства запаха. Она вводит универсальную, адаптируемую структуру для планирования и оптимизации живых микробных терапий для любых состояний, при которых микробиом кишечника превращает пищевые или собственные соединения организма в вредные побочные продукты. Объединив транзит по кишечнику, нативную микробную химию и инженерную ферментативную очистку в одну количественную картину, модель BCAT может предлагать реалистичные цели по дозированию и стратегии по времени приёма задолго до того, как штамм попадёт в клинические испытания. Для пациентов и клиницистов это приближает обещание того, что будущие пробиотические лекарства будут не только дружелюбно и естественно звучащими, но и предсказуемыми, настраиваемыми и основанными на той же строгой подготовке, что и для обычных лекарств.
Цитирование: DeVito, V.L., Karamched, B.R. Signed, sealed, delivered: a generalizable model for living biotherapeutic dosing and metabolism. npj Syst Biol Appl 12, 48 (2026). https://doi.org/10.1038/s41540-026-00685-4
Ключевые слова: микробиом кишечника, пробиотическая терапия, триметиламинурия, математическое моделирование, живые биотерапевтические препараты