Clear Sky Science · zh
纠正X连锁肌张力障碍-帕金森综合征的分子表型揭示BRD4的非典型功能
为什么这个脑部疾病的故事很重要
X‑连锁肌张力障碍‑帕金森综合征(XDP)是一种毁灭性的运动障碍,主要影响菲律宾男性,导致扭曲的动作和随着时间加重的帕金森样僵硬。尽管科学家已知触发XDP的基因突变,但尚不清楚这一改变如何在神经细胞内扰乱基因信息的处理——也不清楚如何纠正它。本研究揭示了脑细胞在复制与完成基因信息时一个被隐藏的薄弱环节,并显示调低一种著名调控蛋白BRD4的水平可以恢复较为正常的信息。该工作为治疗提供了一个新的思路:我们或许不必只试图替代缺失的蛋白,而可以修复信息本身的加工方式。
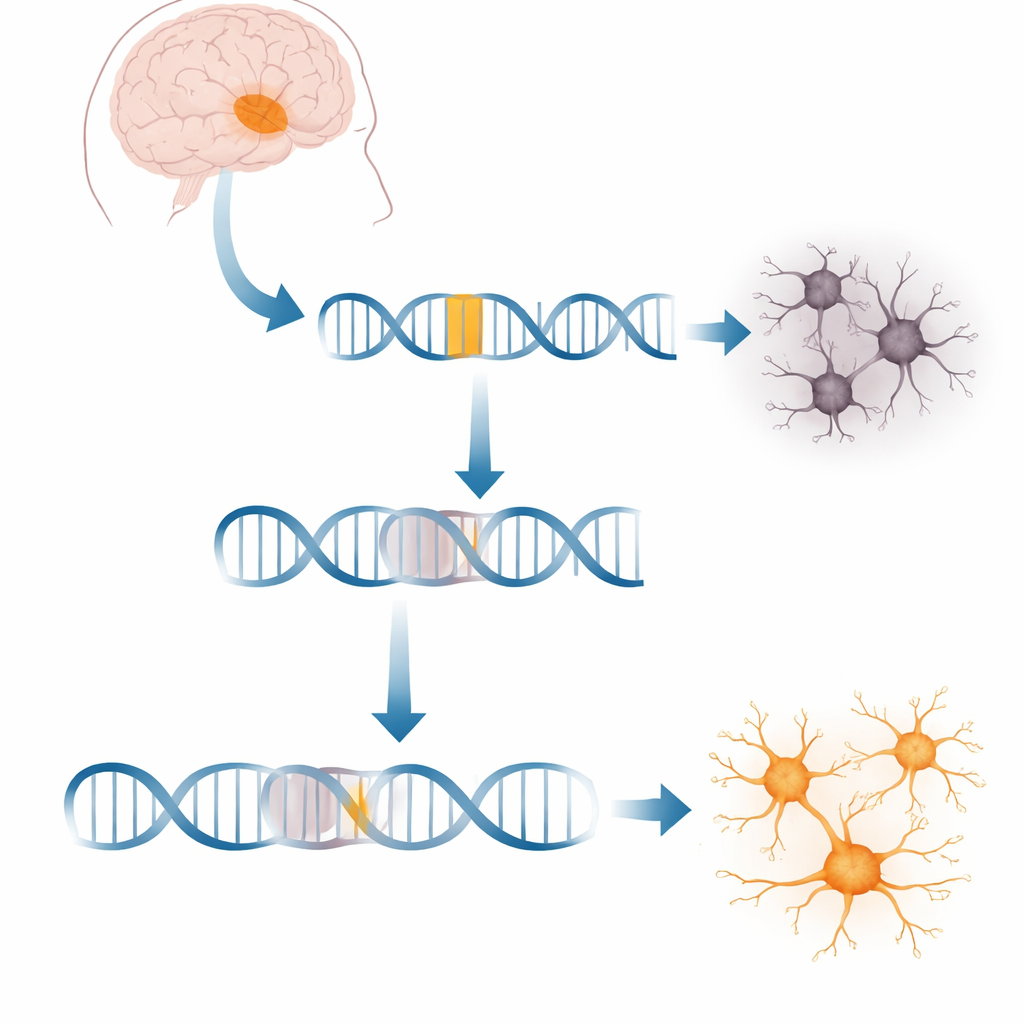
一个异常的遗传插入使关键脑基因出轨
每个细胞不断将基因抄录成信使分子以指导蛋白质的生成。在XDP中,一段称为SVA的可移动DNA插入了一个大基因TAF1内,TAF1有助于启动成千上万个其他基因的转录。该插入位于TAF1一段很长的非编码区内。患者细胞产生的全长TAF1转录本大约减少20%,扰乱了维持健康神经元所需的基因网络。尚不清楚的是,这一外来序列到底如何中断抄录过程,以及是否可以诱导细胞绕过这一阻碍。
构建一个活体传感器以检测有缺陷的基因信息
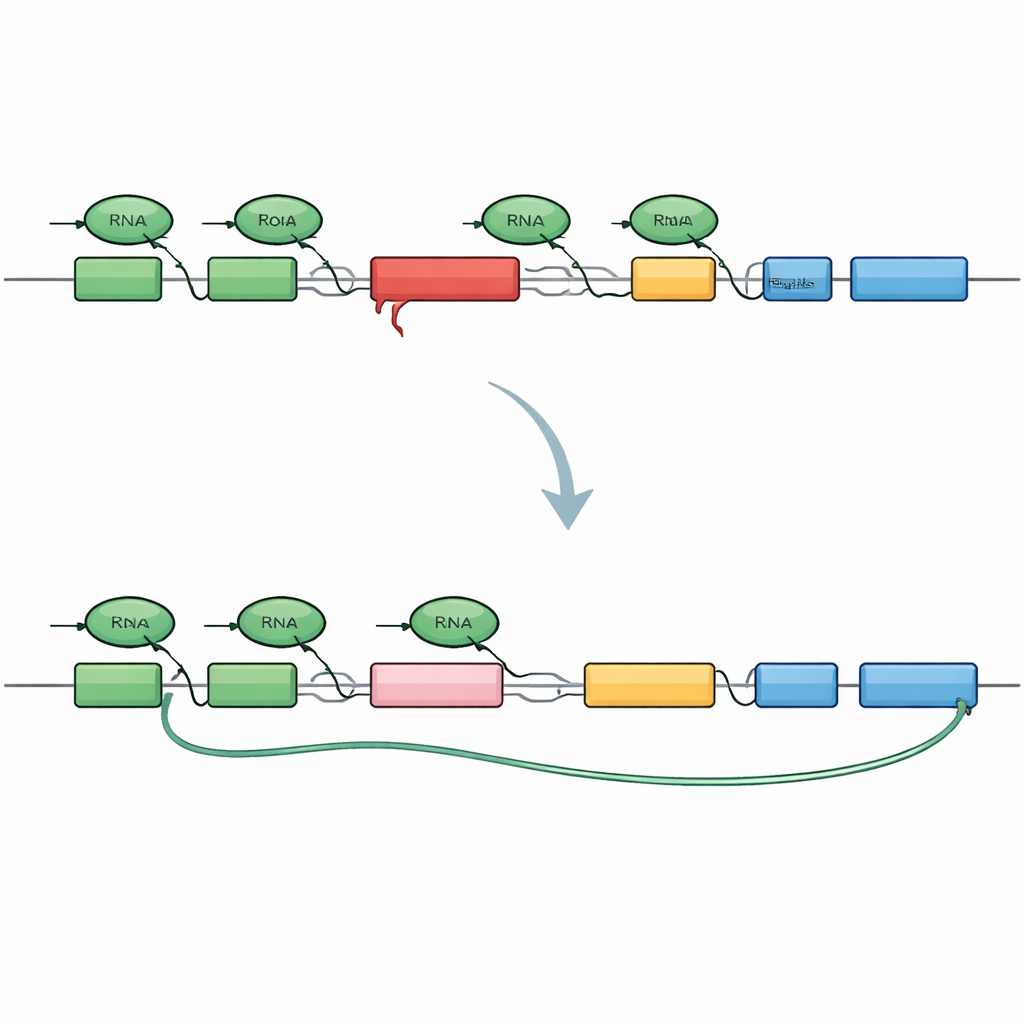
为了解剖这一问题,研究人员构建了包含患者中相同SVA插入的小型TAF1基因。他们在该迷你基因的起始端和末端分别标记了不同的荧光颜色,因此健康的抄录会同时点亮两端,而早期终止只会点亮起始端。当将该构建体置入人类细胞后,它忠实地再现了XDP的模式:许多转录本在携带SVA的内含子内过早终止,并且有一段隐藏的“加密”序列被拼接进来,产生缩短的、死胡同式的转录本和截短的蛋白片段。这一结果证实,仅SVA插入就足以将该内含子变成抄录机器的强大路障。
降低BRD4使转录能读通
借助这一活细胞传感器,团队筛选了500多种针对基因调控和染色质通路的小分子,寻找能增强迷你基因远端荧光信号的化合物。一组显著的命中过筛物都通过降解一类称为BET的蛋白起作用,其中BRD4成为主要参与者。当BRD4被耗竭时,抄录机器更有可能读过有问题的内含子,跳过加密的剪接位点并产生全长的TAF1转录本。令人惊讶的是,仅阻断BRD4常见的染色质结合口袋并不足以达到这一效果;相反,BRD4的一个先前与转录终止调控相关的尾部区域起了关键作用。这揭示了BRD4在管理转录何时及如何被截断和完成方面的一个非典型功能。
迷你大脑揭示早期组织缺陷与部分救治
为了检验该机制在更真实情境中的重要性,作者们从患者的干细胞培养出了三维类脑类器官。这些微小的“迷你大脑”模仿了早期人脑发育。带有XDP突变的类器官更小,神经干细胞及其后代的层次结构被扭曲,并伴有增加的细胞死亡,指向早期发育压力。使用长读长测序,团队在更简单的细胞模型乃至患者尸检脑组织中检测到了同一类过早终止的TAF1转录本。对XDP类器官进行短期BRD4靶向降解剂处理后,剪接模式从加密内含子外显子转向减少使用这些加密外显子,并在适度程度上增加了正常下游外显子的使用,表明转录信息加工得到部分恢复。
这对未来治疗理念意味着什么
通俗地说,XDP可被视为一种问题:一个破坏性的DNA插入把一个长基因变成了充满错误终止信号的雷区,导致细胞产生畸短的指令。本研究表明,降低BRD4活性可以帮助抄录机器忽略这些错误终止信号,继续到达基因的正确终点,从而恢复更完整的指令。尽管目前的BRD4降解药对患者来说过于粗糙且具有毒性,但它们表明“转录终结”阶段是一个脆弱且可调节的步骤。未来若能针对BRD4在信息修整中所涉及的精确伙伴和作用机制,可能为纠正XDP乃至其他由错误RNA加工驱动的疾病的分子缺陷提供途径。
引用: Capponi, S., Ehret, S., Camgöz, Z. et al. Correction of the molecular phenotype of X-linked Dystonia-Parkinsonism reveals a non-canonical function of BRD4. Nat Commun 17, 4062 (2026). https://doi.org/10.1038/s41467-026-72319-6
关键词: X连锁肌张力障碍-帕金森综合征, RNA 加工, BRD4, TAF1 基因, SVA 逆转座子