Clear Sky Science · ar
تصحيح النمط الظاهري الجزيئي لاعتلال العصبوني-الباركنسوني المرتبط بالصبغي X يكشف عن وظيفة غير تقليدية لـ BRD4
لماذا تهم هذه القصة عن اضطراب الدماغ
يُعد اعتلال العصبوني-الباركنسوني المرتبط بالصبغي X (XDP) اضطراب حركي مدمر يصيب أساسًا الرجال من الفلبين، مسبّبًا حركات التواء وتيبّس شبيه بالباركنسون يتفاقم مع مرور الوقت. على الرغم من أن العلماء يعرفون الطفرة الجينية التي تثير XDP، لم يفهموا تمامًا كيف تُشوّه هذه التغيرات رسائل الجين داخل الخلايا العصبية — أو كيفية تصحيحها. تكشف هذه الدراسة عن نقطة ضعف خفية في طريقة نسخ الخلايا الدماغية وإنهاء الرسائل الجينية، وتظهر أن تخفيض نشاط بروتين تنظيمي معروف، BRD4، يمكن أن يعيد رسائل أكثر طبيعية. يفتح العمل مجال تفكير جديد بشأن العلاج: بدلًا من الاكتفاء بمحاولة استبدال البروتين الناقص، قد نتمكن من إصلاح كيفية معالجة الرسالة نفسها.
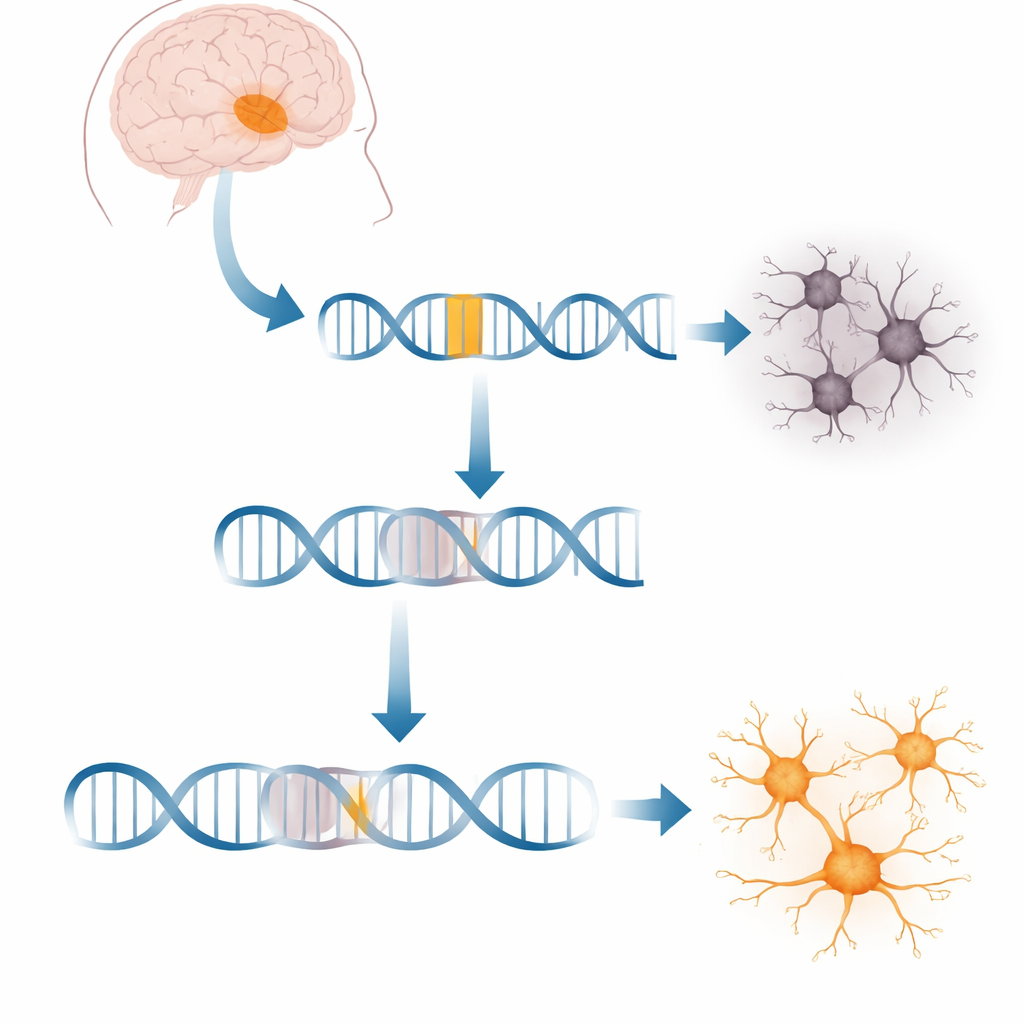
إدخال جيني غريب يعطل جينا محوريا في الدماغ
تنسخ كل خلية باستمرار الجينات إلى جزيئات رسول توجه إنتاج البروتين. في XDP، قفزت قطعة من الحمض النووي المتحرك تسمى عنصر SVA إلى داخل جين كبير يُدعى TAF1، الذي يساعد على إطلاق قراءة آلاف الجينات الأخرى. يقع هذا الإدخال عميقًا داخل أحد المقاطع غير المشفرة الطويلة في TAF1. تصنع خلايا المرضى نحو 20% أقل من رسالة TAF1 الكاملة، مما يزعزع شبكات الجينات المطلوبة لخلايا عصبية صحية. ما لم يكن واضحًا هو كيف تقطع هذه السلسلة الغريبة عملية النسخ بالضبط وما إذا كان من الممكن دفع الخلايا لتجاوز هذا العائق.
بناء حساس حي للرسائل الجينية المعيبة
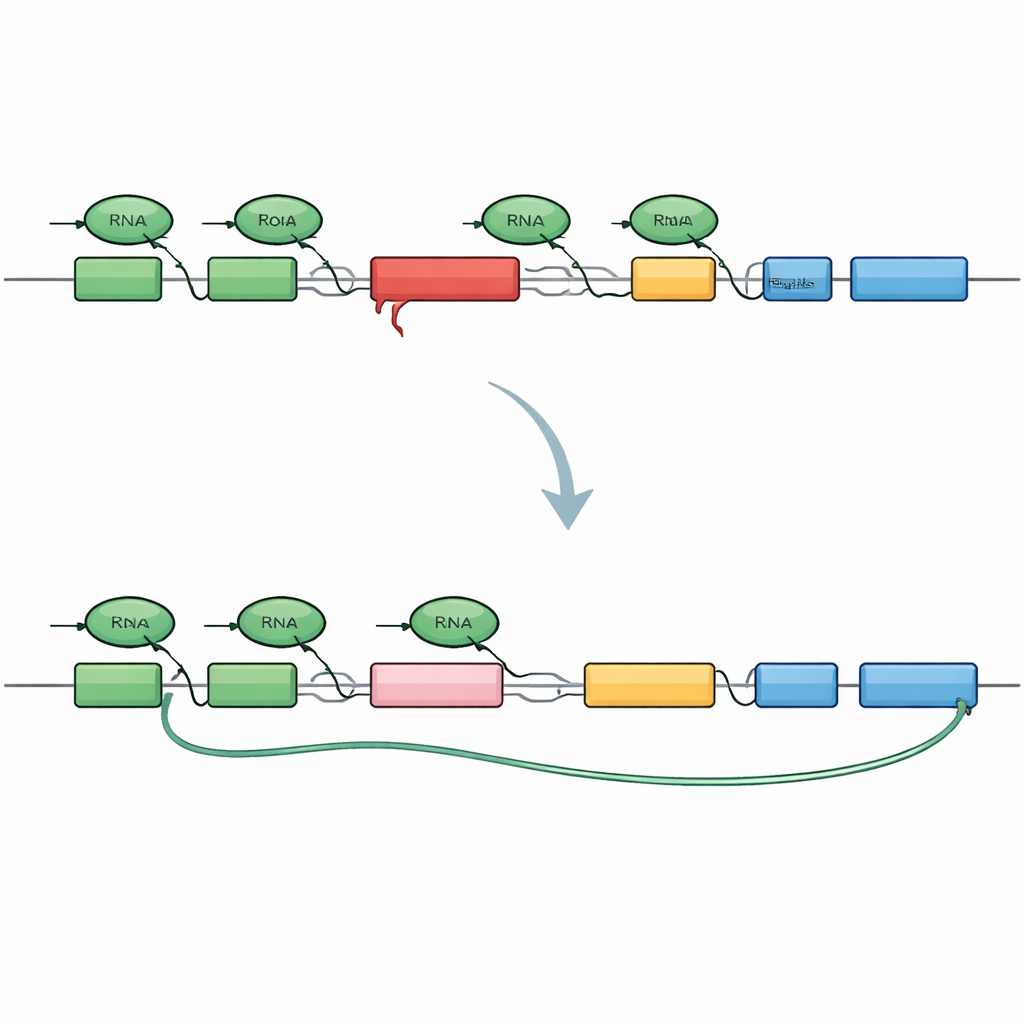
لتفكيك المشكلة، طور الباحثون نسخة مصغرة من جين TAF1 تضم نفس إدخال SVA الموجود في المرضى. وضعوا علامات بألوان فلورية مختلفة على بداية ونهاية هذا الجين المصغّر بحيث تضيء كلا الطرفين عند حدوث نسخ سليم، بينما ستضيء البداية فقط في حال انقطاع النسخ مبكرًا. عندما وُضع هذا التركيب في خلايا بشرية، كرر بدقة نمط XDP: توقفت العديد من الرسائل مبكرًا داخل الإنترون الذي يحمل SVA، وتم إدراج قطعة خفية "تشفيرية" من التسلسل عبر الربط، مما أنشأ رسائل مختصرة مسدودة وشظايا بروتينية مقطوعة. أكدت هذه النتائج أن عنصر SVA وحده يكفي لتحويل الإنترون إلى حاجز قوي أمام آلية النسخ.
خفض BRD4 يسمح بقراءة الرسائل حتى النهاية
مسلّحين بهذا الحساس الخلوي الحي، فحص الفريق أكثر من 500 جزيء صغير تستهدف مسارات التحكم في الجينات والكروماتين، بحثًا عن مركبات تزيد الإشارة الفلورية من الطرف البعيد للجين المصغّر. عملت مجموعة بارزة من الضاربين عبر تحلل عائلة من البروتينات تسمى بروتينات BET، وبرز BRD4 كلاعب رئيسي. عندما نُقص BRD4، باتت آلية النسخ أكثر احتمالًا لتخطي الإنترون المشكل، وتجاوز مواقع الربط التشفيرية وإنتاج رسائل TAF1 بطول كامل. ومن المدهش أن حجب جيوب ارتباط BRD4 بالكروماتين التقليدية لم يكن كافيًا؛ بل كانت منطقة ذيلية مختلفة في BRD4، ارتبطت سابقًا بالتحكم في إنهاء النسخ، هي المسؤولة. يكشف هذا دورًا غير تقليدي لـ BRD4 في إدارة كيفية ومكان قطع وإنهاء الرسائل.
أدمغة مصغرة تكشف عيوب نسيجية مبكرة وانقاذ جزئي
لاختبار ما إذا كانت هذه الآلية ذات أهمية في سياق أكثر واقعية، نما المؤلفون عضوانية ثلاثية الأبعاد شبيهة بالدماغ من خلايا جذعية لمرضى. تحاكي هذه "الأدمغة المصغرة" التطور المبكر للدماغ البشري. كانت العضوونات التي تحمل طفرة XDP أصغر وأظهرت طبقات مشوّهة من الخلايا الجذعية العصبية ونواتجها، إلى جانب زيادة في موت الخلايا، مما يشير إلى إجهاد تطوري مبكر. باستخدام التسلسل طويل القراءة، كشف الفريق عن نفس عائلة رسائل TAF1 المتوقفة مبكرًا التي لوحظت في نماذج الخلايا الأبسط وحتى في أنسجة أدمغة المرضى بعد الوفاة. أدى العلاج قصير المدى لعضوونات XDP بمحلل هدف BRD4 إلى تحوّل أنماط الربط بعيدًا عن الإكسونات الإنترونية التشفيرية وزيادة متواضعة في استخدام الإكسون الطبيعي التالي، مما يدل على استعادة جزئية لمعالجة الرسالة بشكل صحي.
ما الذي يعنيه ذلك لأفكار العلاج المستقبلية
بعبارات بسيطة، يمكن النظر إلى XDP كمشكلة يحول فيها إدخال DNA معيق جينًا طويلاً إلى ميدان ألغام من إشارات التوقف الكاذبة، مما يدفع الخلية لإصدار تعليمات مختصرة. تبيّن هذه الدراسة أن خفض نشاط BRD4 يمكن أن يساعد آلية النسخ الخلوية على تجاهل تلك الإيقافات الكاذبة والاستمرار إلى نهاية الجين الصحيحة، مستعيدًا تعليمات أكثر اكتمالًا. على الرغم من أن أدوية تحلل BRD4 الحالية قاسية وسمية جدًا للاستخدام المباشر في المرضى، فإنها تكشف أن مرحلة "خط النهاية" لنسخ الجينات نقطة ضعف قابلة للتعديل. قد يوفر استهداف الشركاء والأفعال المحددة لـ BRD4 المشاركة في تقليم الرسائل، في المستقبل، وسيلة لتصحيح العيوب الجزيئية في XDP وربما أمراض أخرى ناتجة عن معالجة RNA المعيبة.
الاستشهاد: Capponi, S., Ehret, S., Camgöz, Z. et al. Correction of the molecular phenotype of X-linked Dystonia-Parkinsonism reveals a non-canonical function of BRD4. Nat Commun 17, 4062 (2026). https://doi.org/10.1038/s41467-026-72319-6
الكلمات المفتاحية: اعتلال العصبوني-الباركنسوني المرتبط بالصبغي X, معالجة الحمض النووي الريبي, BRD4, جين TAF1, عناصر SVA المتنقلة