Clear Sky Science · ru
Коррекция молекулярного фенотипа X-сцепленной дистонии‑паркинсонизма выявляет неклассическую функцию BRD4
Почему эта история о заболевании мозга важна
X‑сцепленный дистония‑паркинсонизм (XDP) — разрушительное двигательное расстройство, которое поражает в основном мужчин с Филиппин: оно вызывает скручивающиеся движения и паркинсониподобную скованность, прогрессирующие со временем. Хотя ученым известна генетическая мутация, запускающая XDP, до сих пор не было ясно, как именно это изменение нарушает передачу генетических сообщений в нервных клетках и как это можно исправить. В этом исследовании обнаруживается уязвимое место в том, как клетки мозга копируют и завершают генетические сообщения, и показано, что снижение активности известного регуляторного белка BRD4 может восстановить более нормальные транскрипты. Эта работа открывает новую стратегию мышления о лечении: вместо попыток только заменить недостающий белок, возможно, удастся восстановить сам процесс обработки сообщения.
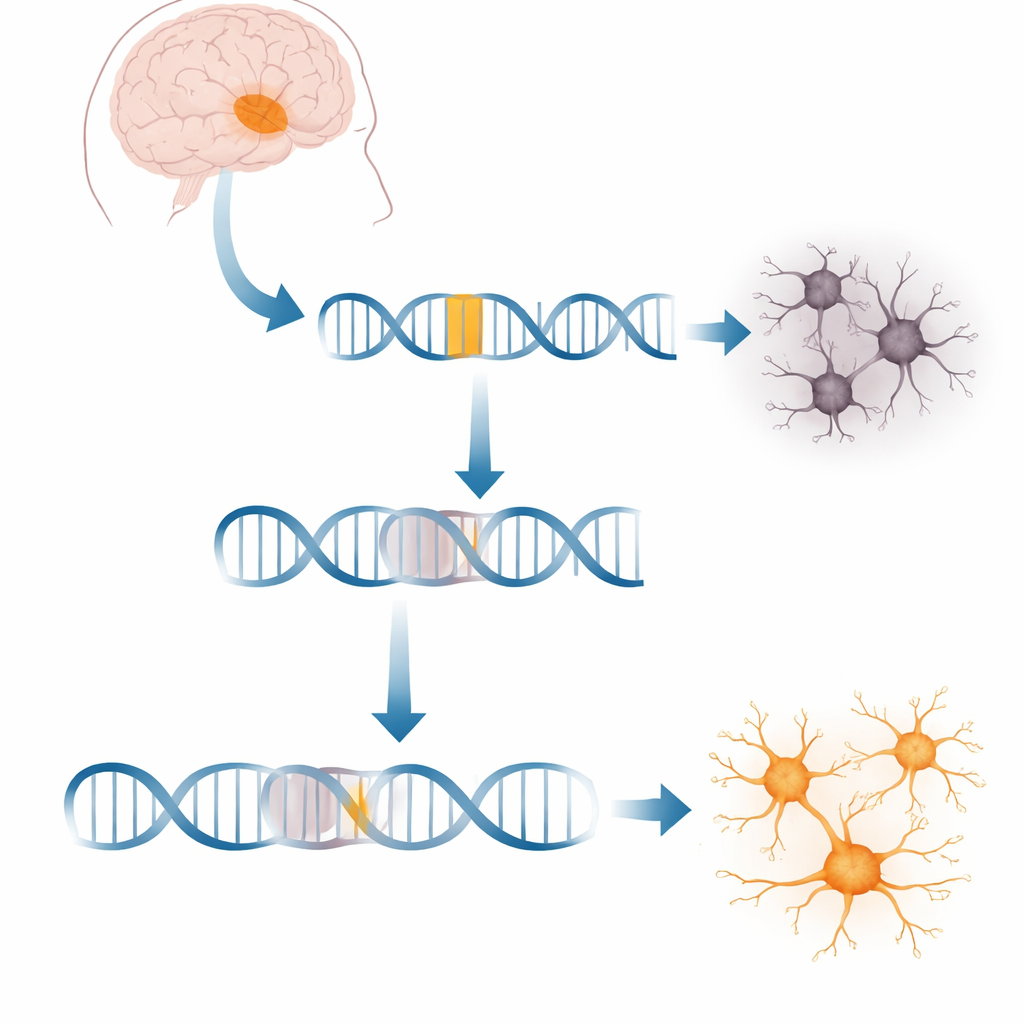
Странная вставка ДНК, срывающая работу важного генного участка в мозге
Каждая клетка постоянно переписывает гены в молекулы мРНК, которые направляют синтез белков. При XDP участок мобильной ДНК, называемый элементом SVA, вставился в большой ген под названием TAF1, который участвует в запуске транскрипции тысяч других генов. Эта вставка находится глубоко внутри одного из длинных некодирующих участков TAF1. В клетках пациентов образуется примерно на 20% меньше полноразмерной мРНК TAF1, что нарушает сети генов, необходимых для нормальной работы нейронов. Ранее оставалось неясным, как именно эта чужеродная последовательность прерывает процесс копирования и можно ли заставить клетки обойти это препятствие.
Создание живого датчика для дефектных сообщений гена
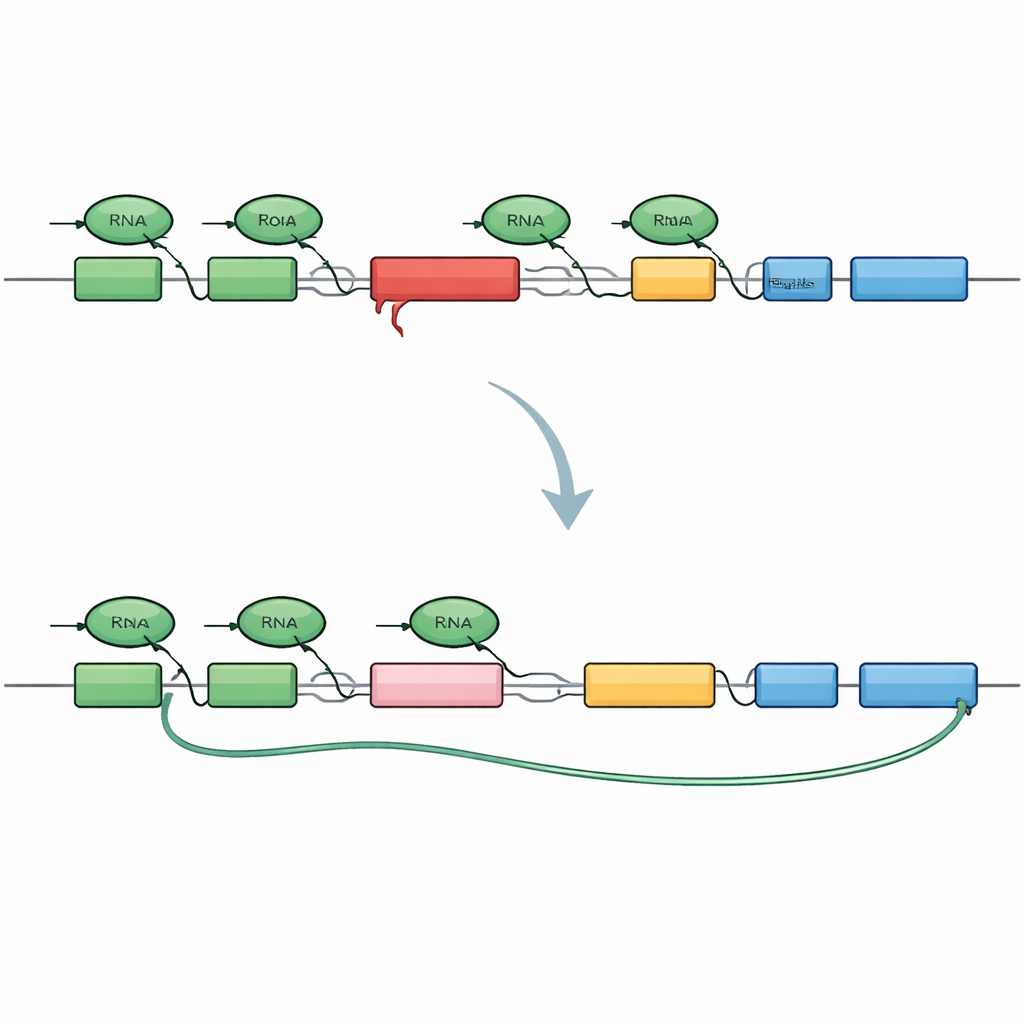
Чтобы разобраться в проблеме, исследователи создали миниатюрную версию гена TAF1, включающую ту же вставку SVA, которая найдена у пациентов. Начало и конец этого мини‑гена были помечены разными флуоресцентными цветами, так что при нормальной транскрипции загорались обе метки, а при преждевременном обрыве светилась только стартовая. Когда конструкт вводили в человеческие клетки, он точно воспроизводил картину XDP: многие транскрипты обрывались преждевременно внутри интрона, содержащего SVA, и скрытая «криптическая» последовательность встраивалась сплайсингом, создавая укороченные, тупиковые транскрипты и усеченные фрагменты белка. Это подтвердило, что одна лишь SVA‑вставка способна превратить интрон в серьёзное препятствие для аппарата транскрипции.
Понижение BRD4 позволяет транскрипту проходить дальше
Оснащённые этим живым датчиком, учёные просcreenировали более 500 небольших молекул, нацеленных на пути регуляции генов и хроматиновые механизмы, в поисках соединений, усиливающих флуоресцентный сигнал от дальнего конца мини‑гена. Поразительная группа активных соединений действовала через деградацию белков семейства BET, причём BRD4 выделился как основной участник. При истощении BRD4 аппарат транскрипции чаще проходил проблемный интрон, обходил криптические сайты сплайсинга и вырабатывал полноразмерные мРНК TAF1. Удивительно, что простое блокирование привычных сайтых связывания BRD4 с хроматином было недостаточно; вместо этого ответственность лежала на другом хвостовом участке BRD4, ранее связанном с контролем завершения транскрипции. Это указывает на неклассическую роль BRD4 в управлении тем, как и где сообщения обрываются и завершаются.
Мини‑мозги выявляют ранние тканевые дефекты и частичное восстановление
Чтобы проверить, имеет ли этот механизм значение в более реалистичной модели, авторы вырастили трёхмерные органоиды, напоминающие мозг, из стволовых клеток пациентов. Эти крошечные «мини‑мозги» имитируют раннее развитие человеческого мозга. Органоиды с мутацией XDP были меньше по размеру и демонстрировали искажённые слои нейрональных стволовых клеток и их потомков, а также повышенную гибель клеток, указывая на ранний стресс в развитии. С помощью секвенирования длинных ридов команда обнаружила ту же семью преждевременно завершённых транскриптов TAF1, что и в простых клеточных моделях и даже в посмертной ткани мозга пациентов. Кратковременное лечение XDP‑органоидов деградирующим агентом, нацеленным на BRD4, сместило схемы сплайсинга в сторону исключения криптических интронных экзонов и умеренно увеличило использование нормального нижестоящего экзона, указывая на частичное восстановление правильной обработки сообщений.
Что это значит для будущих идей лечения
В обыденном описании XDP можно рассматривать как проблему, при которой нарушающая вставка ДНК превращает длинный ген в минное поле ложных сигналов остановки, заставляя клетку выпускать урезанные инструкции. Это исследование показывает, что снижение активности BRD4 помогает транскрипционному аппарату игнорировать эти ложные остановки и доходить до правильного конца гена, восстанавливая более полные инструкции. Хотя нынешние препараты, индуцирующие деградацию BRD4, слишком грубые и токсичные для прямого применения у пациентов, они демонстрируют, что этап «финишной» фазы транскрипции уязвим и поддаётся регулированию. Нацеливание на точные партнёры и функции BRD4, участвующие в обрезке сообщений, в будущем могло бы предложить способ исправить молекулярные дефекты XDP и, возможно, других заболеваний, вызванных нарушением процессинга РНК.
Цитирование: Capponi, S., Ehret, S., Camgöz, Z. et al. Correction of the molecular phenotype of X-linked Dystonia-Parkinsonism reveals a non-canonical function of BRD4. Nat Commun 17, 4062 (2026). https://doi.org/10.1038/s41467-026-72319-6
Ключевые слова: X-сцепленный дистония‑паркинсонизм, процессинг РНК, BRD4, ген TAF1, ретротранспозон SVA