Clear Sky Science · pt
Correção do fenótipo molecular da distonia‑parkinsonismo ligada ao X revela uma função não canônica do BRD4
Por que esta história sobre um distúrbio cerebral importa
A Distonia‑Parkinsonismo ligada ao X (XDP) é um transtorno de movimento devastador que afeta principalmente homens das Filipinas, causando movimentos torsionais e rigidez semelhante ao Parkinson que se agravam com o tempo. Embora os pesquisadores conheçam a mutação genética que desencadeia a XDP, eles ainda não compreenderam exatamente como essa alteração embaralha as mensagens do gene dentro dos neurônios — nem como corrigi‑la. Este estudo revela um ponto fraco oculto na forma como as células cerebrais copiam e finalizam as mensagens genéticas e mostra que reduzir a atividade de uma proteína reguladora conhecida, o BRD4, pode restaurar mensagens mais próximas do normal. O trabalho abre uma nova perspectiva de tratamento: em vez de apenas tentar repor proteínas ausentes, talvez seja possível reparar o processamento da própria mensagem.
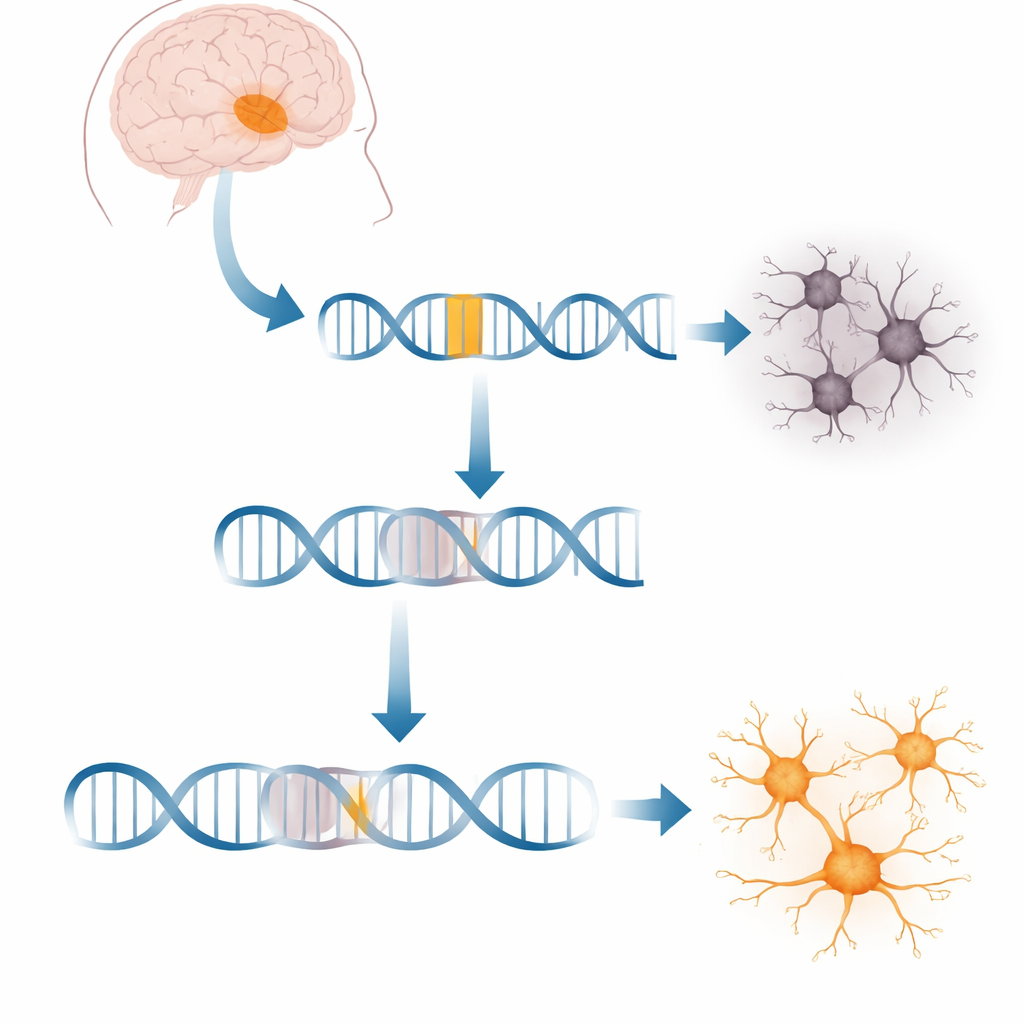
Um inserto genético estranho que atrapalha um gene cerebral chave
Cada célula copia constantemente genes em moléculas mensageiras que orientam a produção de proteínas. Na XDP, um trecho de DNA móvel chamado elemento SVA saltou para dentro de um gene grande chamado TAF1, que ajuda a iniciar a leitura de milhares de outros genes. Esse inserto fica profundamente dentro de um dos longos trechos não codificadores do TAF1. As células de pacientes produzem cerca de 20% a menos de mensagem completa do TAF1, perturbando redes de genes necessárias para neurônios saudáveis. O que não estava claro era exatamente como essa sequência estranha interrompe o processo de cópia e se as células podem ser induzidas a contornar o bloqueio.
Construindo um sensor vivo para mensagens genéticas defeituosas
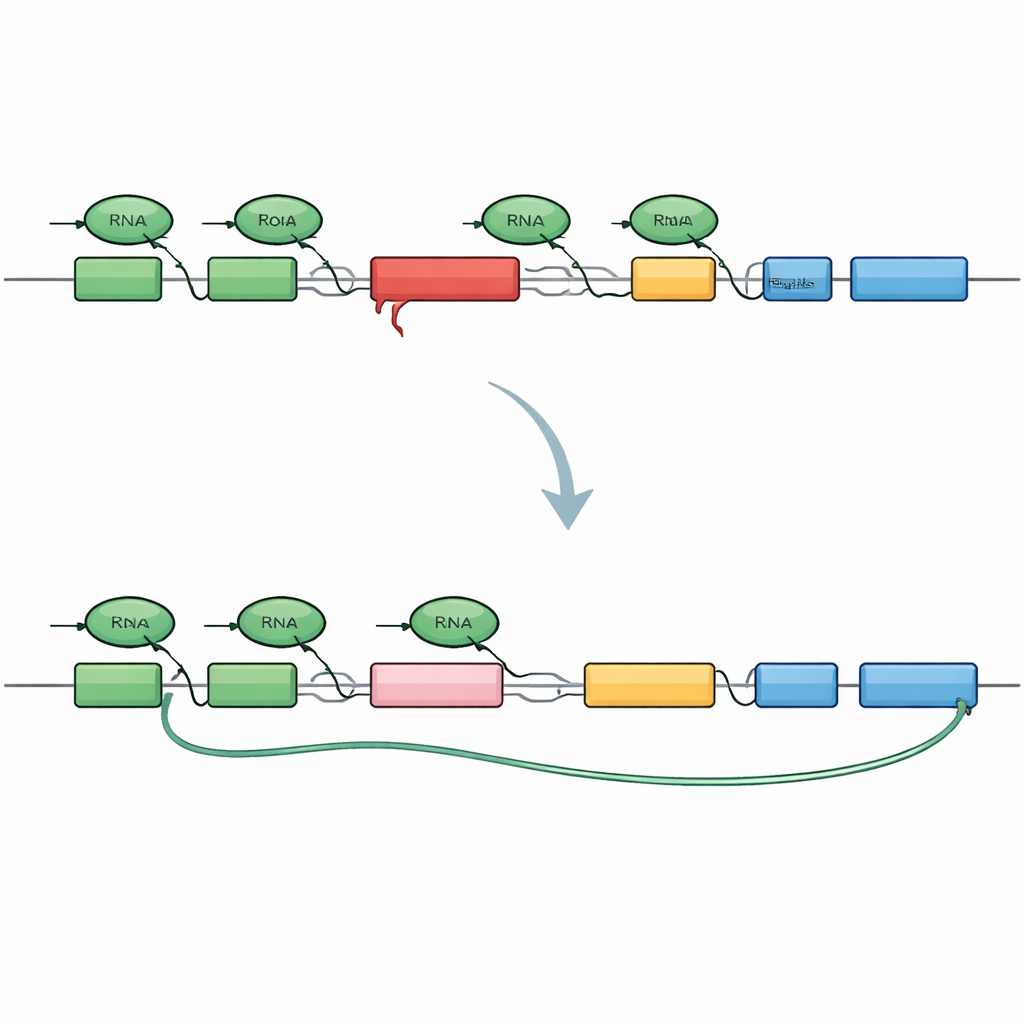
Para dissecar o problema, os pesquisadores construíram uma versão em miniatura do gene TAF1 que inclui o mesmo inserto SVA encontrado em pacientes. Eles marcaram o início e o fim desse mini‑gene com cores fluorescentes diferentes, de modo que uma cópia saudável acendesse ambas as extremidades, enquanto uma interrupção prematura acendesse apenas o início. Quando esse construto foi inserido em células humanas, ele reproduziu fielmente o padrão observado na XDP: muitas mensagens terminavam prematuramente dentro do íntron que contém o SVA, e um trecho “críptico” de sequência era emendado, criando mensagens encurtadas e sem saída e fragmentos proteicos truncados. Isso confirmou que o SVA sozinho é suficiente para transformar o íntron em um forte bloqueio para a maquinaria de transcrição.
Reduzir o BRD4 permite que as mensagens sejam lidas por completo
Com esse sensor em células vivas, a equipe triou mais de 500 pequenas moléculas que atuam em vias de controle gênico e cromatina, buscando compostos que ampliassem o sinal fluorescente da extremidade distante do mini‑gene. Um grupo marcante de acertos atuou degradando uma família de proteínas chamadas BET, com o BRD4 emergindo como protagonista. Quando o BRD4 foi reduzido, a maquinaria de transcrição teve mais probabilidade de avançar além do íntron problemático, ignorar os sítios de emenda crípticos e produzir mensagens completas do TAF1. Surpreendentemente, bloquear apenas os domínios conhecidos de ligação à cromatina do BRD4 não foi suficiente; em vez disso, uma região da cauda do BRD4, anteriormente associada ao controle do término da transcrição, foi a responsável. Isso revela um papel não canônico do BRD4 no gerenciamento de como e onde as mensagens são cortadas e finalizadas.
Mini‑cérebros revelam defeitos teciduais precoces e resgate parcial
Para testar se esse mecanismo importa em um cenário mais realista, os autores cultivaram organoides cerebrais tridimensionais a partir de células‑tronco de pacientes. Esses pequenos “mini‑cérebros” imitam o desenvolvimento cerebral humano inicial. Organoides com a mutação XDP eram menores e mostravam camadas distorcidas de células‑tronco neurais e seus descendentes, além de aumento da morte celular, apontando para estresse no desenvolvimento precoce. Usando sequenciamento de leitura longa, a equipe detectou a mesma família de mensagens TAF1 terminadas prematuramente observada em modelos celulares mais simples e até em tecido cerebral post‑mortem de pacientes. Tratamento de curto prazo dos organoides XDP com um degradador direcionado ao BRD4 deslocou os padrões de emenda, reduzindo os éxons intrônicos crípticos e aumentando modestamente o uso do éxon normal a jusante, indicando uma restauração parcial do processamento adequado das mensagens.
O que isso significa para ideias de tratamento futuras
Em termos práticos, a XDP pode ser vista como um problema em que um inserto de DNA disruptivo transforma um gene longo em um campo minado de sinais de parada falsos, fazendo com que a célula produza instruções atrofiadas. Este estudo mostra que diminuir a atividade do BRD4 pode ajudar a maquinaria de transcrição a ignorar essas paradas falsas e seguir até o término correto do gene, restaurando instruções mais completas. Embora os atuais fármacos degradadores de BRD4 sejam bem rudimentares e tóxicos demais para uso direto em pacientes, eles mostram que a fase de “linha de chegada” da transcrição é uma etapa vulnerável e ajustável. Mirar os parceiros e as ações precisas do BRD4 envolvidos no recorte das mensagens pode, no futuro, oferecer uma forma de corrigir os defeitos moleculares da XDP e possivelmente de outras doenças impulsionadas por processamento defeituoso de RNA.
Citação: Capponi, S., Ehret, S., Camgöz, Z. et al. Correction of the molecular phenotype of X-linked Dystonia-Parkinsonism reveals a non-canonical function of BRD4. Nat Commun 17, 4062 (2026). https://doi.org/10.1038/s41467-026-72319-6
Palavras-chave: Distonia‑Parkinsonismo ligada ao X, Processamento de RNA, BRD4, gene TAF1, retrotransposon SVA