Clear Sky Science · it
Correzione del fenotipo molecolare della distonia‑parkinsonismo legata all’X rivela una funzione non canonica di BRD4
Perché questa storia sulla malattia cerebrale è importante
La distonia‑parkinsonismo legata all’X (XDP) è un devastante disturbo del movimento che colpisce principalmente uomini dalle Filippine, provocando movimenti torsionali e rigidità simile al morbo di Parkinson che peggiorano nel tempo. Sebbene gli scienziati conoscano la mutazione genetica che innesca la XDP, non avevano ancora compreso esattamente come questa alterazione comprometta i messaggi del gene nelle cellule nervose — né come correggerla. Questo studio individua un punto debole nascosto nel modo in cui le cellule cerebrali copiano e completano i messaggi genetici e mostra che ridurre l’attività di una proteina regolatoria ben nota, BRD4, può ripristinare messaggi più vicini alla normalità. Il lavoro apre una nuova prospettiva terapeutica: invece di limitarsi a sostituire una proteina mancante, potremmo essere in grado di riparare il modo in cui il messaggio stesso viene processato.
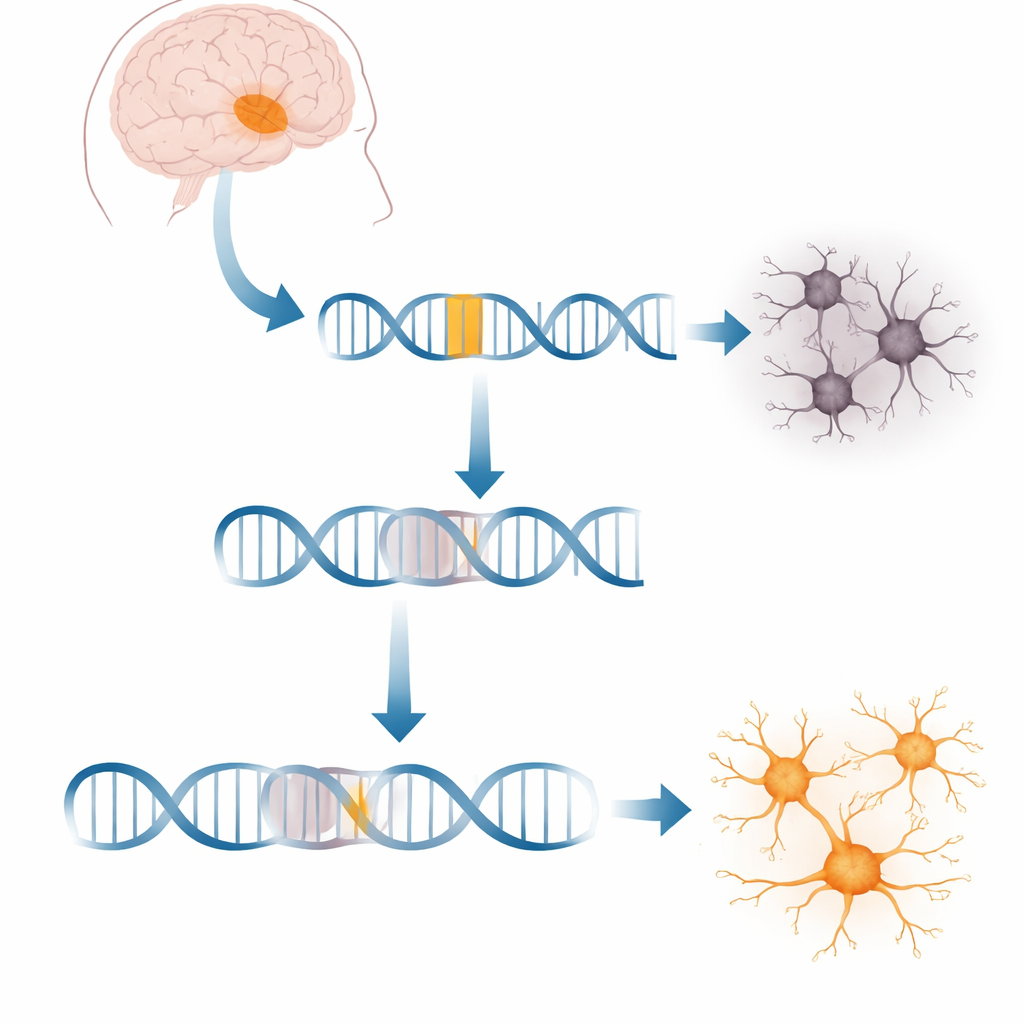
Un inserto genetico insolito che manda fuori strada un gene cerebrale chiave
Ogni cellula copia continuamente i geni in molecole messaggere che guidano la produzione proteica. Nella XDP, un tratto di DNA mobile chiamato elemento SVA è saltato dentro un grande gene chiamato TAF1, che contribuisce ad avviare la lettura di migliaia di altri geni. Questo inserto si trova in profondità in uno dei lunghi tratti non codificanti di TAF1. Le cellule dei pazienti producono circa il 20% in meno di trascritto TAF1 a lunghezza completa, alterando reti geniche necessarie per la salute dei neuroni. Non era chiaro come questa sequenza estranea interrompa il processo di trascrizione e se le cellule possano essere indotte a superare l’ostacolo.
Costruire un sensore vivo per i messaggi genici difettosi
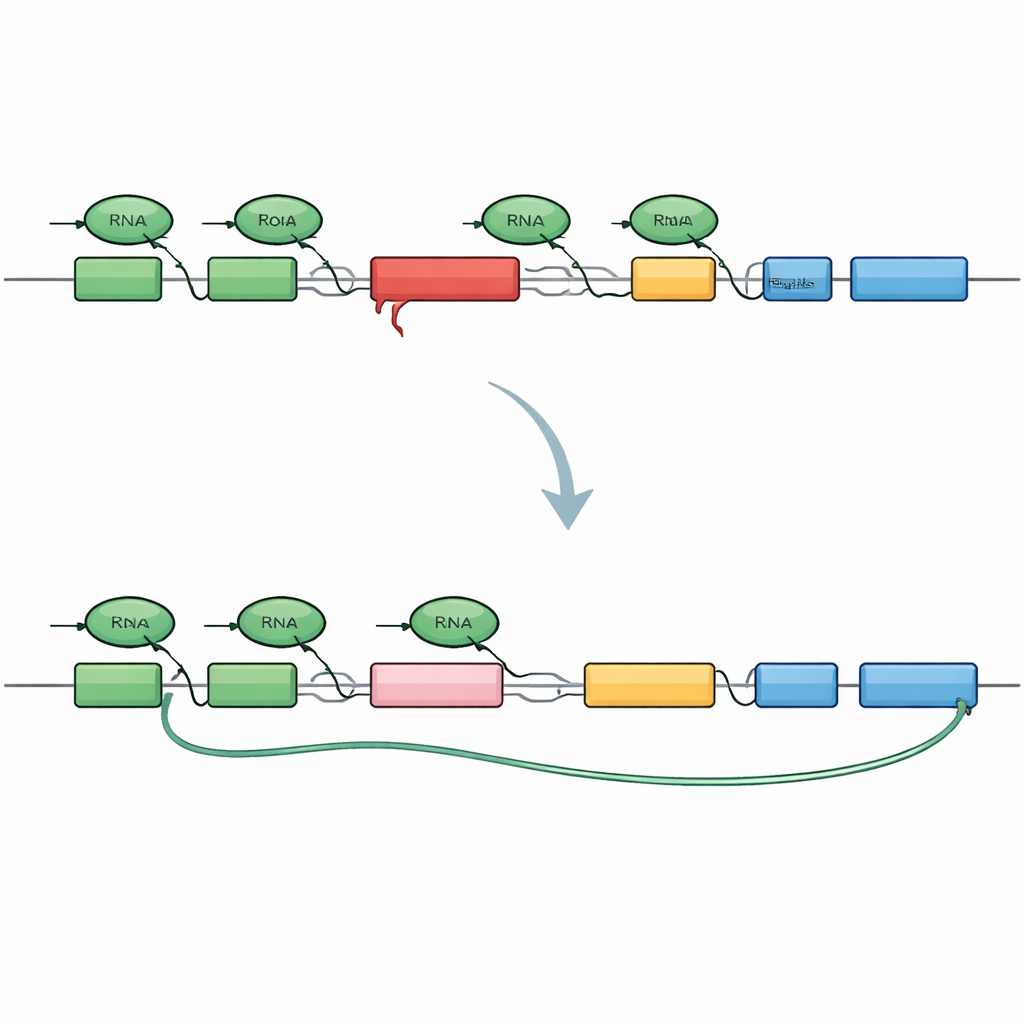
Per dissezionare il problema, i ricercatori hanno progettato una versione in miniatura del gene TAF1 che include lo stesso inserto SVA trovato nei pazienti. Hanno etichettato l’inizio e la fine di questo mini‑gene con colori fluorescenti diversi in modo che una trascrizione sana illuminasse entrambe le estremità, mentre un arresto prematuro accendesse solo l’estremità iniziale. Quando questo costrutto è stato inserito in cellule umane, ha riprodotto fedelmente il modello osservato nella XDP: molti trascritti si interrompevano prematuramente all’interno dell’introne che porta l’SVA, e un pezzo di sequenza “critico” nascosto veniva inserito tramite splicing, creando messaggi accorciati e senza uscita e frammenti proteici tronchi. Questo ha confermato che l’SVA da solo è sufficiente a trasformare l’introne in un forte ostacolo per la macchina di trascrizione.
Abbassare BRD4 permette la lettura completa dei messaggi
Dotati di questo sensore in cellule vive, il gruppo ha testato oltre 500 piccole molecole che prendono di mira vie di controllo genico e la cromatina, cercando composti che aumentassero il segnale fluorescente dalla parte finale del mini‑gene. Un gruppo sorprendente di hits agiva degradando una famiglia di proteine chiamate BET, con BRD4 che emergeva come protagonista principale. Quando BRD4 veniva depletato, la macchina di trascrizione era più propensa a leggere oltre l’introne problematico, saltare i siti di splicing critici e produrre trascritti TAF1 a lunghezza completa. Sorprendentemente, bloccare semplicemente le tasche di legame alla cromatina di BRD4 non bastava; invece, una diversa regione terminale di BRD4, precedentemente collegata al controllo della fine della trascrizione, era responsabile. Questo rivela un ruolo non canonico di BRD4 nella gestione di come e dove i messaggi vengono tagliati e completati.
I mini‑cervelli rivelano difetti tessutali precoci e un recupero parziale
Per verificare se questo meccanismo avesse rilevanza in un contesto più realistico, gli autori hanno coltivato organoidi cerebrali tridimensionali da cellule staminali dei pazienti. Questi piccoli “mini‑cervelli” imitano lo sviluppo cerebrale umano precoce. Gli organoidi portatori della mutazione XDP erano più piccoli e presentavano strati distorti di cellule staminali neurali e loro discendenti, insieme a un aumento della morte cellulare, segnali di stress nello sviluppo precoce. Con sequenziamento a lettura lunga, il gruppo ha rilevato la stessa famiglia di trascritti TAF1 interrotti prematuramente osservata nei modelli cellulari più semplici e persino nel tessuto cerebrale postmortem dei pazienti. Un trattamento a breve termine degli organoidi XDP con un degradatore mirato a BRD4 ha spostato gli schemi di splicing lontano dagli esoni intronici critici e ha aumentato modestamente l’uso dell’esone normale a valle, indicando un parziale ripristino di un processamento dei messaggi più sano.
Cosa significa per le idee terapeutiche future
In termini pratici, la XDP può essere vista come un problema in cui un inserto di DNA disturbante trasforma un gene lungo in un campo minato di falsi segnali di arresto, facendo sì che la cellula produca istruzioni tronche. Questo studio mostra che ridurre l’attività di BRD4 può aiutare la macchina di trascrizione a ignorare quei falsi arresti e proseguire fino al corretto termine del gene, ripristinando istruzioni più complete. Sebbene gli attuali farmaci degradanti BRD4 siano ancora troppo grezzi e tossici per un uso diretto nei pazienti, essi rivelano che la fase di “traguardo” della trascrizione è un punto vulnerabile e modulabile. Mirare ai partner e alle azioni specifiche di BRD4 coinvolti nel rifinitura dei messaggi potrebbe, in futuro, offrire un modo per correggere i difetti molecolari della XDP e forse di altre malattie guidate da un errato processamento dell’RNA.
Citazione: Capponi, S., Ehret, S., Camgöz, Z. et al. Correction of the molecular phenotype of X-linked Dystonia-Parkinsonism reveals a non-canonical function of BRD4. Nat Commun 17, 4062 (2026). https://doi.org/10.1038/s41467-026-72319-6
Parole chiave: Distonia‑Parkinsonismo legata all’X, Elaborazione dell’RNA, BRD4, Gene TAF1, Retrotrasposone SVA