Clear Sky Science · sv
Korrigering av den molekylära fenotypen vid X‑bundet dystoni‑parkinsonism avslöjar en icke‑kanonisk funktion hos BRD4
Varför den här hjärnsjukdomshistorien är viktig
X‑bundet dystoni‑parkinsonism (XDP) är en förödande rörelsesjukdom som främst drabbar män från Filippinerna och ger krampartade vridrörelser och parkinsonlik stelhet som förvärras med tiden. Även om forskare har identifierat den genetiska förändring som utlöser XDP, har de inte fullt ut förstått hur denna förändring ställer till det för genens budskap inne i nervcellerna — eller hur den ska rättas till. Denna studie avslöjar en dold svag punkt i hur hjärnceller kopierar och avslutar genetiska budskap och visar att nedreglering av det välkända regleringsproteinet BRD4 kan återställa mer normala budskap. Arbetet öppnar en ny tankelinje för behandling: istället för att bara försöka ersätta saknat protein kan vi kanske reparera hur budskapet i sig bearbetas.
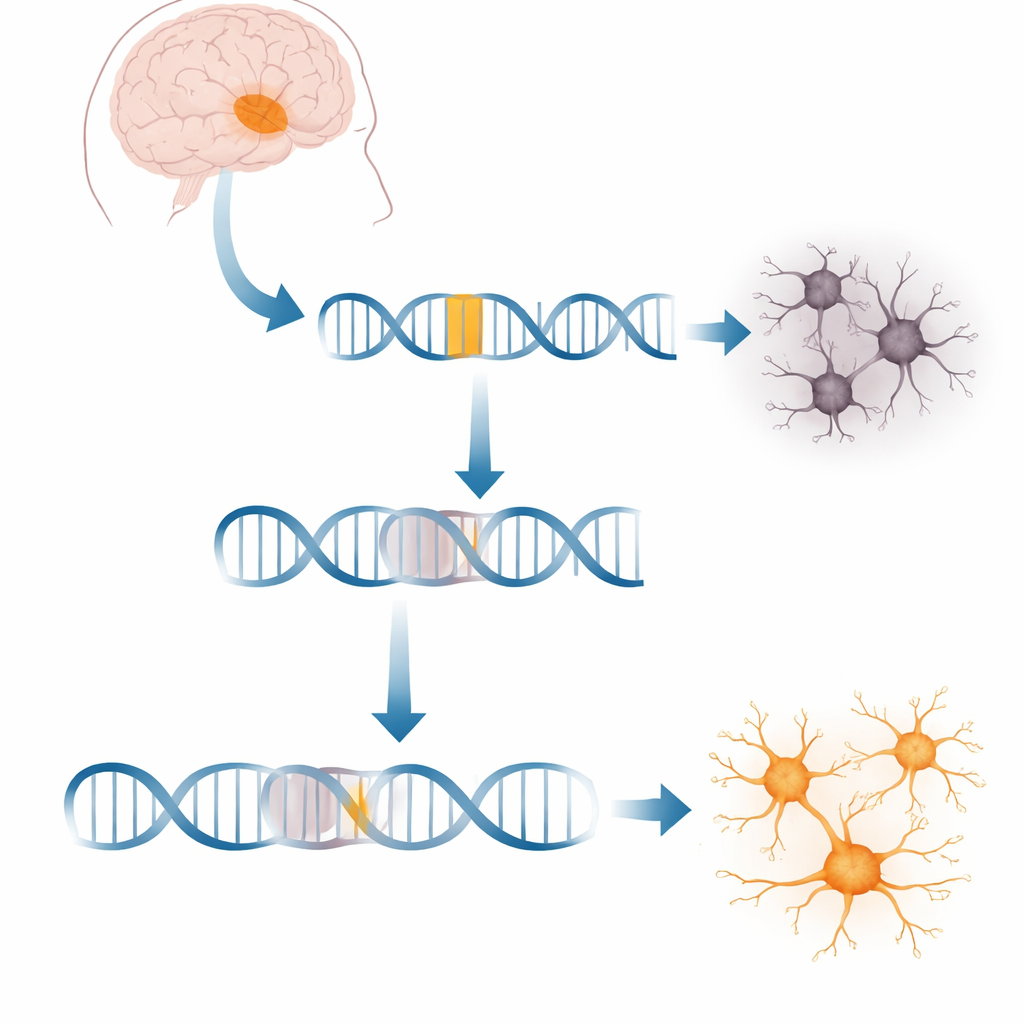
En märklig genetisk insert som stjälper en viktig hjärngen
Varje cell kopierar ständigt gener till budbärarmolekyler som styr proteinproduktionen. I XDP har ett stycke rörlig DNA, kallat ett SVA‑element, hoppat in i en stor gen som heter TAF1, vilken hjälper till att starta avläsningen av tusentals andra gener. Denna insättning ligger djupt inne i en av TAF1:s långa icke‑kodande regioner. Patienternas celler producerar ungefär 20 % mindre fullängds‑TAF1‑budskap, vilket rubbar nätverk av gener som behövs för friska neuroner. Vad som varit oklart är exakt hur denna främmande sekvens stör kopieringsprocessen och om celler kan övertalas att kringgå hindret.
Bygga en levande sensor för felaktiga genbudskap
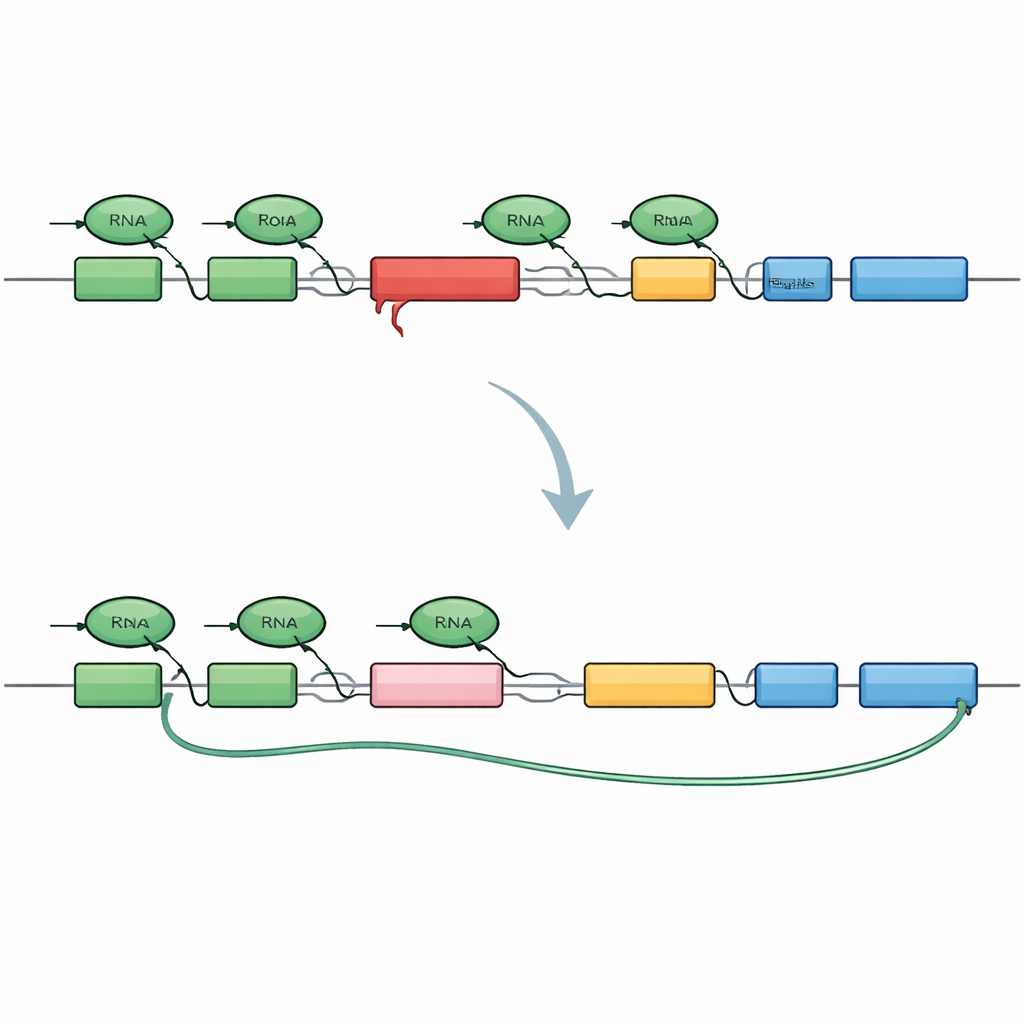
För att dissekera problemet konstruerade forskarna en miniatyrversion av TAF1‑genen som innehåller samma SVA‑insättning som hos patienter. De märkta början och slutet av den här mini‑genen med olika fluorescerande färger så att frisk avläsning skulle lysa upp båda ändarna, medan ett tidigt avbrott bara skulle lysa upp starten. När konstruktionen sattes in i mänskliga celler reproducerade den troget XDP‑mönstret: många budskap avbröts för tidigt inom intronet som bär SVA:t, och en dold ”kryptisk” sekvensdel splicades in, vilket skapade förkortade, dödliga budskap och trunkerade proteinklippor. Detta bekräftade att SVA:t ensam är tillräckligt för att förvandla intronet till ett starkt vägblock för kopieringsmaskineriet.
Neddragning av BRD4 tillåter att budskapen läses igenom
Med denna levande cell‑sensor skannade teamet mer än 500 småmolekyler som riktar sig mot genreglering och kromatinvägar, i jakt på föreningar som ökade den fluorescerande signalen från mini‑genens fjärrände. En tydlig grupp träffar verkade samtliga genom att nedbryta en familj proteiner kallade BET‑proteiner, där BRD4 framträdde som huvudaktören. När BRD4 utarmades var kopieringsmaskineriet mer benäget att läsa förbi det problematiska intronet, hoppa över de kryptiska splice‑sites och producera fullängds‑TAF1‑budskap. Överraskande nog räckte det inte att enbart blockera BRD4:s vanliga kromatinbindande fickor; istället var en annan tail‑region av BRD4, tidigare kopplad till kontroll av transkriptionens avslutning, ansvarig. Detta avslöjar en icke‑kanonisk roll för BRD4 i att hantera hur och var budskap skärs av och avslutas.
Mini‑hjärnor avslöjar tidiga vävnadsdefekter och partiell räddning
För att testa om denna mekanism spelar roll i en mer realistisk miljö odlade författarna tredimensionella hjärnliknande organoider från patienters stamceller. Dessa små ”mini‑hjärnor” efterliknar tidig mänsklig hjärnutveckling. Organoider som bar XDP‑mutationen var mindre och visade förvrängda lager av neurala stamceller och deras avkomma, tillsammans med ökad celldöd, vilket tyder på tidig utvecklingsstress. Med långläsningssekvensering upptäckte teamet samma familj av förtidsavslutade TAF1‑budskap som sågs i enklare cellmodeller och även i postmortem hjärnvävnad från patienter. Korttidsbehandling av XDP‑organoider med en BRD4‑riktad degrader försköt splicingen bort från kryptiska introniska exoner och ökade måttligt användningen av den normala efterföljande exonen, vilket indikerar en partiell återställning av hälsosam budskapsbearbetning.
Vad detta betyder för framtida behandlingsidéer
I vardagstermer kan XDP ses som ett problem där en störande DNA‑insättning förvandlar en lång gen till ett minfält av falska stopp‑signaler, vilket får cellen att spotta ut förkrympta instruktioner. Denna studie visar att sänkning av BRD4‑aktivitet kan hjälpa det cellulära kopieringsmaskineriet att ignorera dessa falska stopp och fortsätta till genens rätta slut, vilket återställer mer fullständiga instruktioner. Trots att dagens BRD4‑nedbrytande läkemedel är alltför grova och toxiska för direkt användning hos patienter, visar de att transkriptionens ”målgångs”fas är ett sårbart och justerbart steg. Att rikta in sig på de precisa partnerna och funktionerna hos BRD4 som är involverade i budskapstrimning kan i framtiden erbjuda ett sätt att korrigera de molekylära felen vid XDP och möjligen andra sjukdomar drivna av felaktig RNA‑bearbetning.
Citering: Capponi, S., Ehret, S., Camgöz, Z. et al. Correction of the molecular phenotype of X-linked Dystonia-Parkinsonism reveals a non-canonical function of BRD4. Nat Commun 17, 4062 (2026). https://doi.org/10.1038/s41467-026-72319-6
Nyckelord: X‑bundet dystoni‑parkinsonism, RNA‑bearbetning, BRD4, TAF1‑genen, SVA‑retrotransposon