Clear Sky Science · nl
Correctie van het moleculaire fenotype van X-gebonden dystonie‑Parkinsonisme onthult een niet-canonische functie van BRD4
Waarom dit verhaal over een hersenaandoening belangrijk is
X‑gebonden dystonie‑Parkinsonisme (XDP) is een verwoestende bewegingsstoornis die vooral mannen uit de Filipijnen treft en leidt tot verkrampende draaibewegingen en Parkinson‑achtige stijfheid die in de loop van de tijd verergeren. Hoewel onderzoekers de genetische mutatie kennen die XDP veroorzaakt, begrepen ze niet precies hoe deze verandering de genetische boodschappen in zenuwcellen verstoort — of hoe die te corrigeren. Deze studie legt een verborgen zwakte bloot in de manier waarop hersencellen genetische boodschappen kopiëren en afronden en laat zien dat het terugschakelen van een bekende regulatorische eiwit, BRD4, meer normale boodschappen kan herstellen. Het werk opent een nieuwe denkrichting voor behandeling: in plaats van alleen te proberen ontbrekend eiwit te vervangen, zouden we kunnen herstellen hoe het bericht zelf wordt verwerkt.
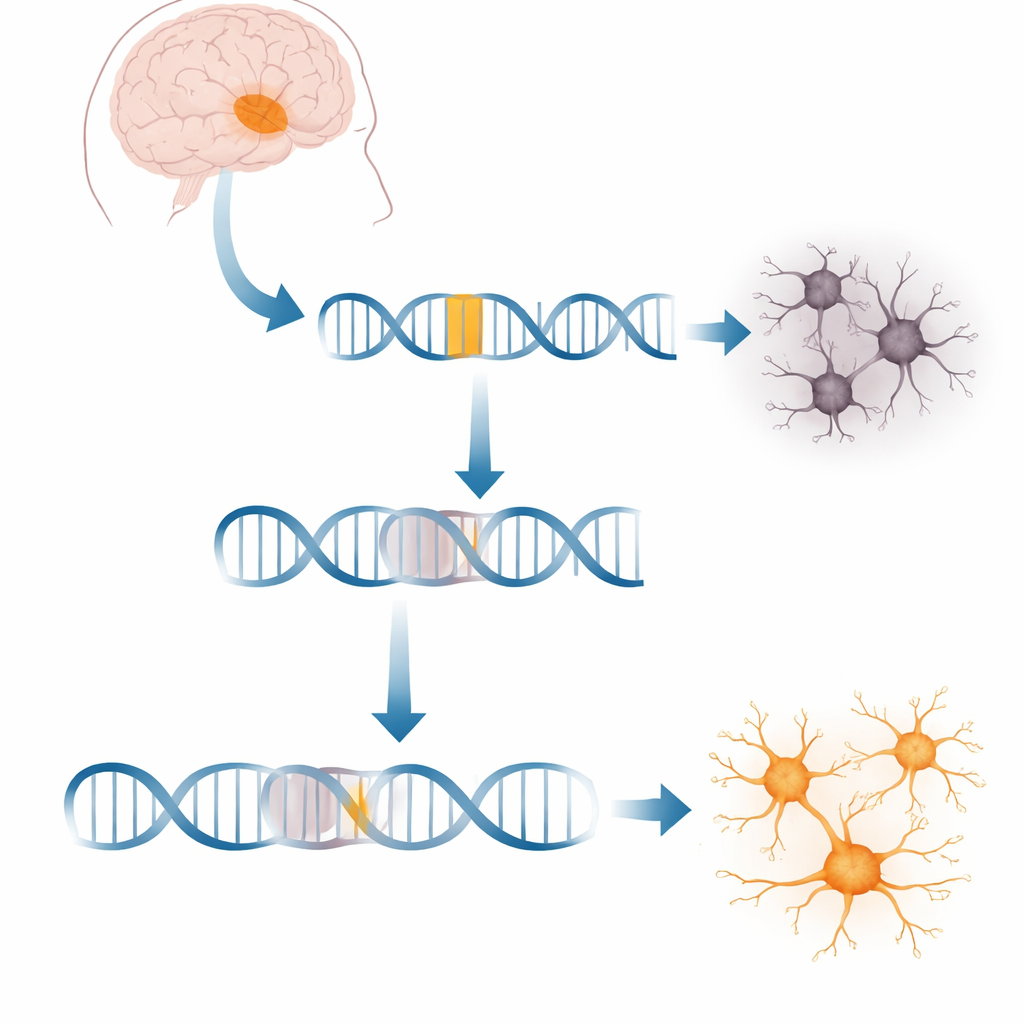
Een vreemd genetisch invoegsel dat een sleutelgen in de hersenen ontspoort
Elke cel kopieert voortdurend genen naar boodschappermoleculen die de eiwitproductie sturen. Bij XDP is een stuk mobiele DNA, een SVA-element, in een groot gen genaamd TAF1 gesprongen, dat helpt bij het starten van het aflezen van duizenden andere genen. Dit invoegsel bevindt zich diep in een van de lange niet-coderende stukken van TAF1. Cellen van patiënten maken ongeveer 20% minder volledige TAF1-boodschappen, wat netwerken van genen verstoort die nodig zijn voor gezonde neuronen. Wat onduidelijk bleef, was precies hoe deze vreemde sequentie het kopieerproces onderbreekt en of cellen kunnen worden aangezet om die blokkade te omzeilen.
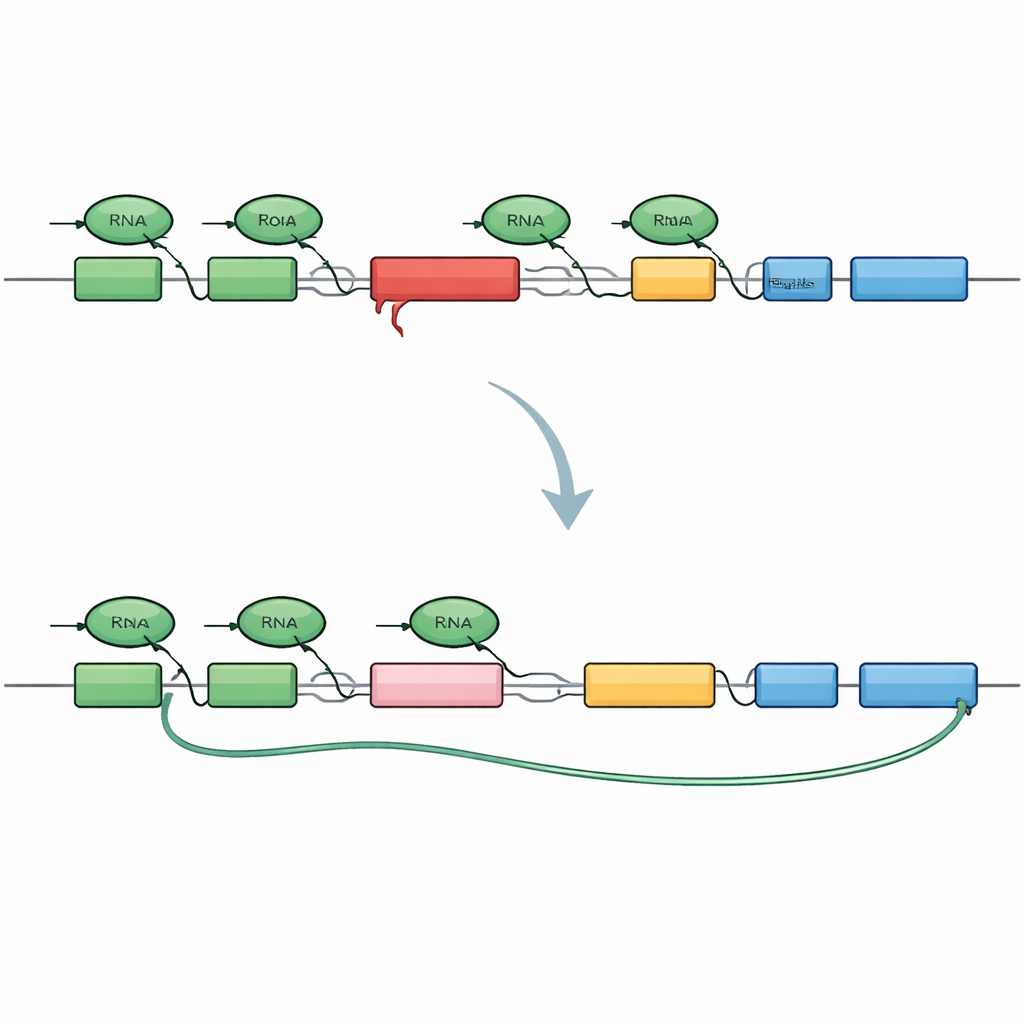
Een levende sensor bouwen voor foutieve genberichten
Om het probleem te ontleden, maakten de onderzoekers een miniatuurversie van het TAF1-gen die hetzelfde SVA-invoegsel bevatte als bij patiënten. Ze markeerden het begin en einde van dit mini-gen met verschillende fluorescerende kleuren zodat gezond aflezen beide uiteinden zou laten oplichten, terwijl vroegtijdig afbreken alleen het begin zou laten zien. Toen dit construct in menselijke cellen werd ingebracht, reproduceerde het trouw het XDP-patroon: veel boodschappen stopten voortijdig binnen het intron dat het SVA draagt, en een verborgen “cryptisch” stuk sequentie werd ingesplitst, waardoor verkorte, doodlopende boodschappen en ingekorte eiwitfragmenten ontstonden. Dit bevestigde dat het SVA op zich voldoende is om het intron te veranderen in een sterke blokkade voor het kopieerapparaat.
BRD4 verlagen laat boodschappen doorlezen
Met deze sensor in levende cellen screeneden de onderzoekers meer dan 500 kleine moleculen die gericht zijn op genregulatie en chromatinepaden, op zoek naar verbindingen die het fluorescerende signaal van het verre uiteinde van het mini-gen versterkten. Een opvallende groep hits werkte door een familie eiwitten, de BET-eiwitten, af te breken, waarbij BRD4 naar voren kwam als de voornaamste speler. Wanneer BRD4 werd uitgeput, las het kopieerapparaat vaker voorbij het problematische intron, werden de cryptische splice-sites overgeslagen en werden volledige TAF1-boodschappen geproduceerd. Verrassend genoeg was het blokkeren van BRD4’s gebruikelijke chromatinebindende pockets alleen niet voldoende; in plaats daarvan was een andere staartregio van BRD4, eerder in verband gebracht met het beheersen van het einde van transcriptie, verantwoordelijk. Dit onthult een niet-canonische rol voor BRD4 in het beheren van hoe en waar boodschappen worden geknipt en afgerond.
Mini‑hersenen tonen vroege weefselschade en deels herstel
Om te testen of dit mechanisme ook in een realistischer model van belang is, kweekten de auteurs driedimensionale hersenachtige organoïden uit stamcellen van patiënten. Deze kleine “mini‑hersenen” bootsen vroege menselijke hersenontwikkeling na. Organoïden met de XDP-mutatie waren kleiner en toonden vervormde lagen van neurale stamcellen en hun nakomelingen, samen met verhoogde celdood, wat wijst op vroege ontwikkelingsstress. Met long‑read sequencing detecteerde het team dezelfde familie van voortijdig afgebroken TAF1‑boodschappen die in eenvoudigere celmodellen en zelfs in postmortaal hersenweefsel van patiënten werd gezien. Kortdurende behandeling van XDP-organoïden met een BRD4‑gericht degrader verschuifte splicingpatronen weg van cryptische intronexonen en verhoogde bescheiden het gebruik van het normale downstream exoon, wat wijst op een gedeeltelijk herstel van gezonde boodschapverwerking.
Wat dit betekent voor toekomstige behandelideeën
In gewone bewoordingen kan XDP worden gezien als een probleem waarbij een verstorend DNA‑invoegsel een lang gen verandert in een mijnenveld van valse stopsignalen, waardoor de cel afgekapte instructies uitbrengt. Deze studie toont aan dat het verlagen van BRD4‑activiteit het kopieerapparaat kan helpen die valse stops te negeren en door te lezen tot het juiste einde van het gen, waardoor vollediger instructies worden hersteld. Hoewel de huidige BRD4‑afbrekende middelen veel te grof en toxisch zijn voor direct gebruik bij patiënten, laten ze zien dat de ‘finishlijn’-fase van genafschrift een kwetsbare en instelbare stap is. Het richten op de precieze partners en acties van BRD4 die betrokken zijn bij het afhandelen van berichten kan in de toekomst een manier bieden om de moleculaire defecten van XDP en mogelijk andere ziekten die door foutieve RNA‑verwerking worden aangedreven, te corrigeren.
Bronvermelding: Capponi, S., Ehret, S., Camgöz, Z. et al. Correction of the molecular phenotype of X-linked Dystonia-Parkinsonism reveals a non-canonical function of BRD4. Nat Commun 17, 4062 (2026). https://doi.org/10.1038/s41467-026-72319-6
Trefwoorden: X-gebonden dystonie‑Parkinsonisme, RNA-verwerking, BRD4, TAF1-gen, SVA-retrotransposon