Clear Sky Science · zh
在实体癌细胞中针对性降解USP7揭示了去泛素化酶降解剂与抑制剂的不同效应
为什么分解一个蛋白对癌症很重要
癌症治疗常常旨在阻断有害蛋白的活性,但一种新兴思路是将这些蛋白从细胞中彻底移除。本研究聚焦于一种名为USP7的蛋白,它帮助其他蛋白避免被自然降解,研究提出了一个简单而影响深远的问题:是临时关闭USP7更好,还是完全清除它更有利?通过在来自胰腺癌和黑色素瘤的实体肿瘤细胞中比较这两种策略,研究人员发现了对设计更安全、更精确药物非常重要的差异。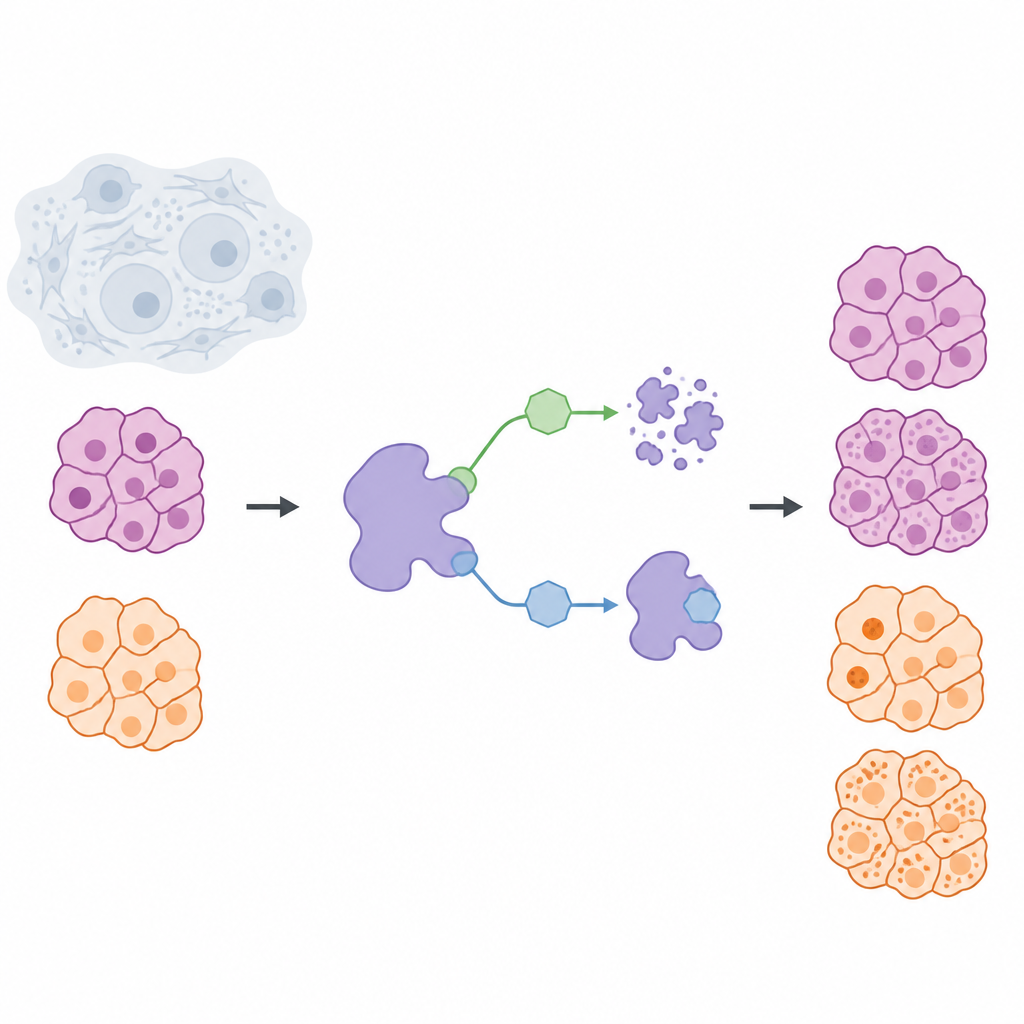
两种不同工具控制同一靶点
团队构建了一套化学工具箱,用两种截然不同的方式在活细胞中控制USP7。一类分子,称为抑制剂,附着在USP7上并阻断其活性,但蛋白本身仍保留在细胞中。第二类分子,称为降解剂,更像是带有引导标签的移除工具:它们将USP7引向细胞的“废物处理”机器,使该蛋白被降解清除。为使比较公平,科学家们首先设计出一个高度选择性的抑制剂NK192,它能强力结合USP7且很少影响其他蛋白。在此基础上,他们进一步构建了一系列降解剂分子,这些分子既能识别USP7,又能招募名为VHL的细胞降解系统,从而高效地将USP7从癌细胞中剥离。
为不同癌细胞定制的去除剂
当研究者在胰腺和黑色素瘤细胞系中测试他们的降解剂库时,发现USP7结合部分与VHL招募部分之间的连接子形状和刚性对性能有强烈影响。经过几轮设计与测试,他们筛选出两个表现突出的降解剂:在胰腺癌细胞中效果最佳的NK250,以及在黑色素瘤细胞中更有效的NK266。这些分子在极低剂量下即可几乎完全清除USP7,后续实验确认该效应依赖于预期的降解通路。通过灵敏的检测手段,研究团队表明NK250特别容易与USP7和VHL形成稳定的三元复合体,这解释了其快速作用的机制。
放大镜下的细胞内部变化
为了观察在阻断或移除USP7后细胞其他部分发生了什么,科学家们使用先进的质谱技术测量了处理过的癌细胞中成千上万种蛋白质。降解剂产生了出人意料的聚焦响应:USP7消失了,一小部分已知的相互作用伙伴蛋白尤其是组成一种基因沉默机器——Polycomb复合体的成分,在两种癌型中都下降。这些变化放松了对某些通常被抑制基因的控制,证实了USP7支持特定的基因沉默程序。重要的是,许多先前报道的USP7潜在伙伴在这些实体癌细胞中并未改变,突出显示了USP7功能在不同细胞类型间存在强烈差异。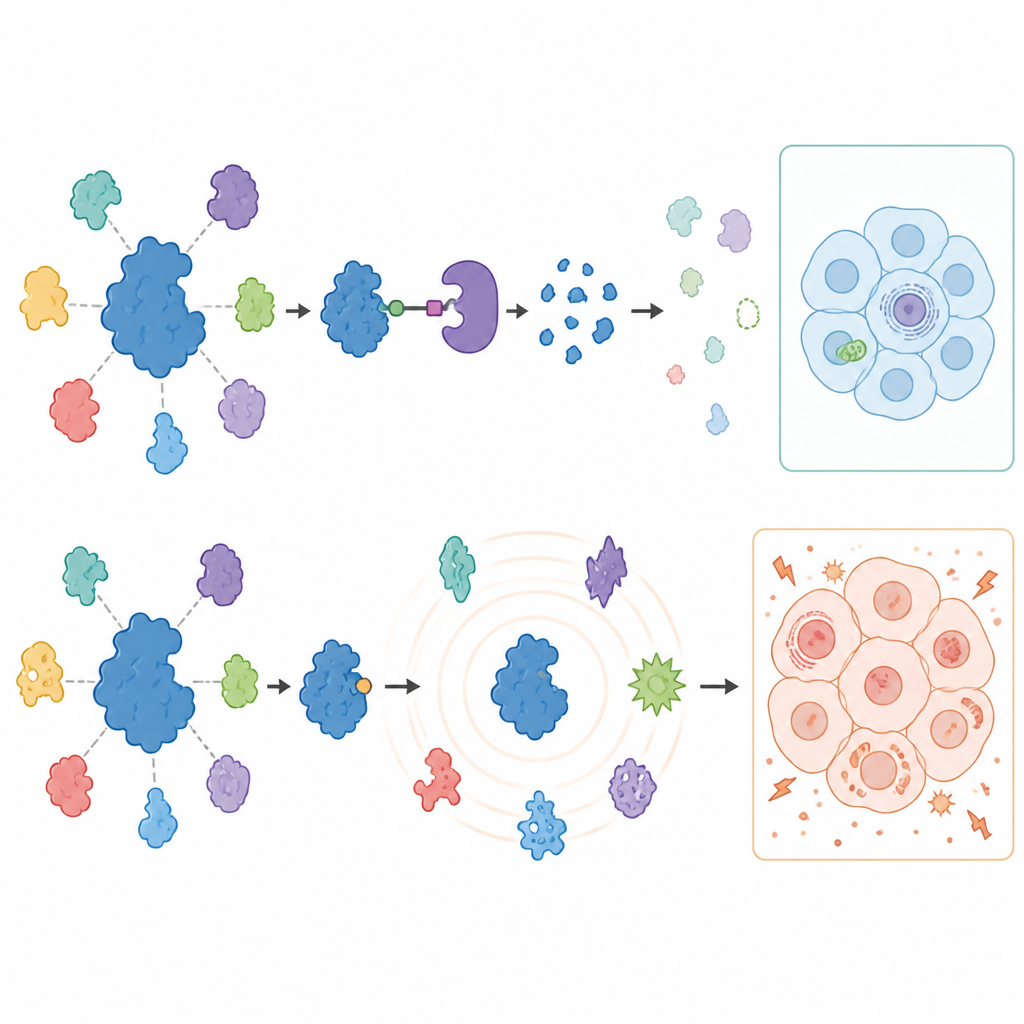
当阻断远远超出靶点时
抑制剂在更长时间尺度上讲述了完全不同的故事。最初一天内,蛋白质变化模式在很大程度上与降解剂相似,指向USP7的真实功能。但在三天的处理后,抑制剂引发了一波广泛且有时异常的蛋白变化,包括出现这些癌细胞中通常不见的蛋白。细胞也开始大量依赖糖代谢,线粒体产生能量的能力降低,并在葡萄糖受限时更易发生细胞死亡。关键的是,这些代谢扰动同样出现在通过基因编辑删除USP7的黑色素瘤细胞中,证明这些效应是抑制剂的脱靶作用所致,而非USP7本身的结果。
这对未来癌症药物意味着什么
这项工作显示,经过精心设计的降解剂可以高精度地清除USP7,从而揭示实体癌中一组聚焦的真实下游基因调控效应。相比之下,即便是早期检测看起来干净的良好表征抑制剂,在长期使用时也可能触发广泛的、与USP7无关的改变。对科学家和药物开发者而言,结论明确:降解剂是清晰解析单一蛋白在不同癌症中真实作用的强大工具,而抑制剂更适合用于短期的功能验证。将这两类互补工具结合起来,有助于更清楚地理解并最终利用USP7及其相关蛋白进行癌症治疗。
引用: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
关键词: USP7, PROTAC 降解剂, 癌细胞, 蛋白抑制, 细胞代谢