Clear Sky Science · nl
Gerichte afbraak van USP7 in solide kankercellen onthult verschillende effecten van deubiquitinase-degraders en -inhibitors
Waarom het afbreken van één eiwit ertoe doet bij kanker
Veel kankerbehandelingen zijn gericht op het blokkeren van schadelijke eiwitten, maar een opkomend idee is om die eiwitten helemaal uit de cel te verwijderen. Deze studie onderzoekt een eiwit dat USP7 heet, dat andere eiwitten helpt om natuurlijke afbraak te ontlopen, en stelt een ogenschijnlijk simpele vraag met grote consequenties: is het beter USP7 tijdelijk uit te schakelen, of het helemaal te laten verdwijnen? Door deze twee strategieën te vergelijken in solide tumorcellen van pancreaskanker en melanoom, ontdekken de onderzoekers belangrijke verschillen die van belang zijn bij het ontwerpen van veiligere en preciezere geneesmiddelen. 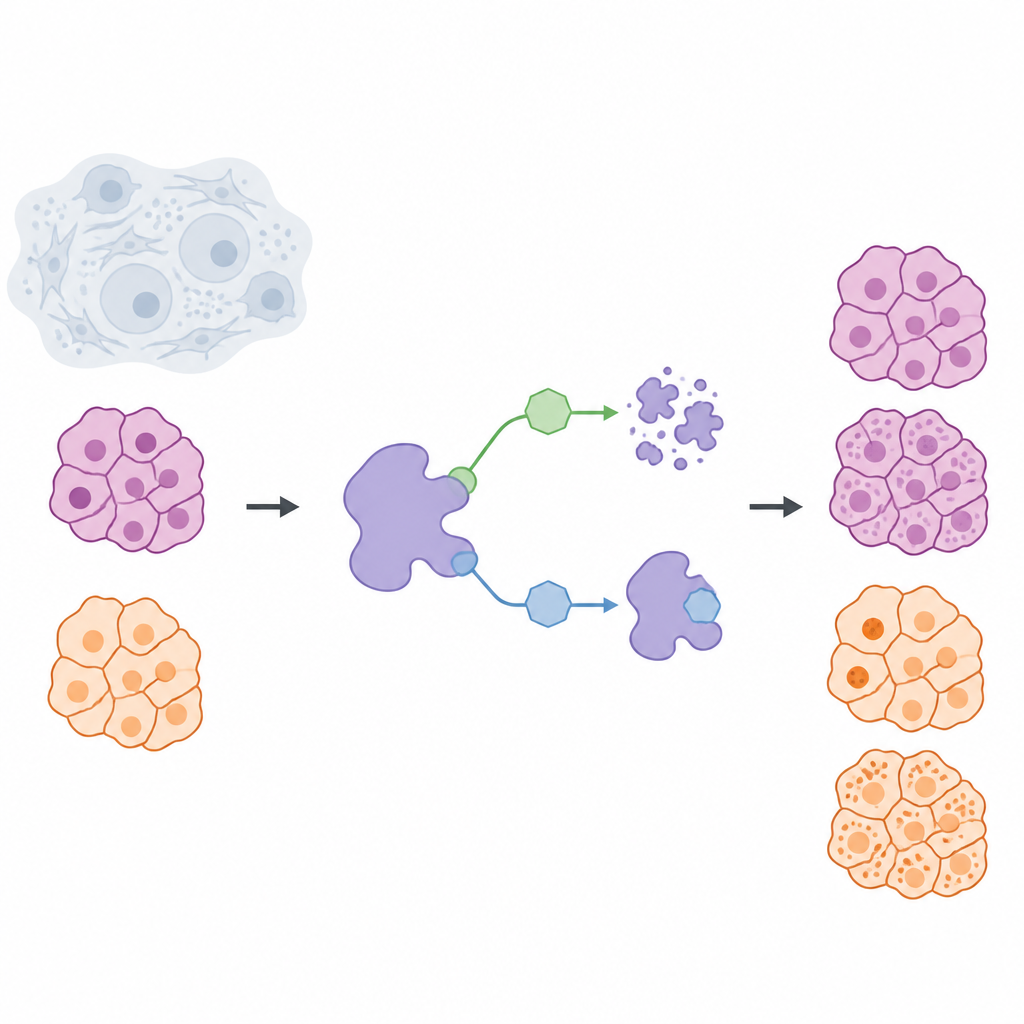
Twee verschillende gereedschappen om hetzelfde doel te sturen
Het team bouwde een chemische gereedschapskist om USP7 in levende cellen op twee verschillende manieren te beheersen. De ene groep moleculen, remmers genoemd, hecht zich aan USP7 en stopt de activiteit terwijl het eiwit zelf op zijn plaats blijft. De tweede groep, degraders genoemd, werkt meer als geleide verwijderingslabels: ze brengen USP7 in contact met het afvalverwerkingssysteem van de cel zodat het eiwit wordt afgebroken en verwijderd. Om de vergelijking eerlijk te maken, ontwikkelden de wetenschappers eerst een zeer selectieve remmer, NK192, die sterk aan USP7 bindt en zelden andere eiwitten aantast. Vanuit dit uitgangspunt ontwierpen ze vervolgens een serie degradermoleculen die zowel USP7 herkennen als het cellulaire afbraakcomplex VHL rekruteren, waardoor ze USP7 efficiënt uit kankercellen kunnen strippen.
Maatwerk-verwijderaars voor verschillende kankercellen
Toen de onderzoekers hun degraderbibliotheek testten in pancreatische en melanoomcelijnen, ontdekten ze dat de vorm en stijfheid van de linker tussen het USP7-bindende deel en het VHL-recruterende deel sterk bepalend waren voor de werking. Na meerdere ontwerp- en testcycli kwamen ze uit op twee opvallende degraders: NK250, dat het beste werkt in pancreaskankercellen, en NK266, dat effectiever is in melanoomcellen. Deze moleculen konden USP7 vrijwel volledig verwijderen bij zeer lage concentraties, en vervolgexperimenten bevestigden dat het effect afhankelijk was van de bedoelde afbraakroute. Met gevoelige assays toonden de onderzoekers aan dat NK250 in het bijzonder een stabiel drie-eenheidcomplex vormt met USP7 en VHL, wat zijn snelle werking verklaart.
Inzoomen op wat er binnenin de cel verandert
Om te zien wat er met de rest van de cel gebeurt wanneer USP7 wordt geblokkeerd of verwijderd, maten de wetenschappers duizenden eiwitten in behandelde kankercellen met geavanceerde massaspectrometrie. Degraders veroorzaakten een verrassend gefocuste reactie: USP7 verdween en een beperkte set bekende partner-eiwitten, vooral componenten van een gen-onderdrukkingsmachine genaamd het Polycomb-complex, nam in beide kankertypes af. Deze veranderingen hieven de rem op bepaalde genen die normaal stil worden gehouden, wat bevestigt dat USP7 specifieke genonderdrukkingsprogramma’s ondersteunt. Belangrijk is dat veel eerder voorgestelde USP7-partners niet veranderden in deze solide kankercellen, wat onderstreept dat de rol van USP7 sterk tussen celtypen kan verschillen. 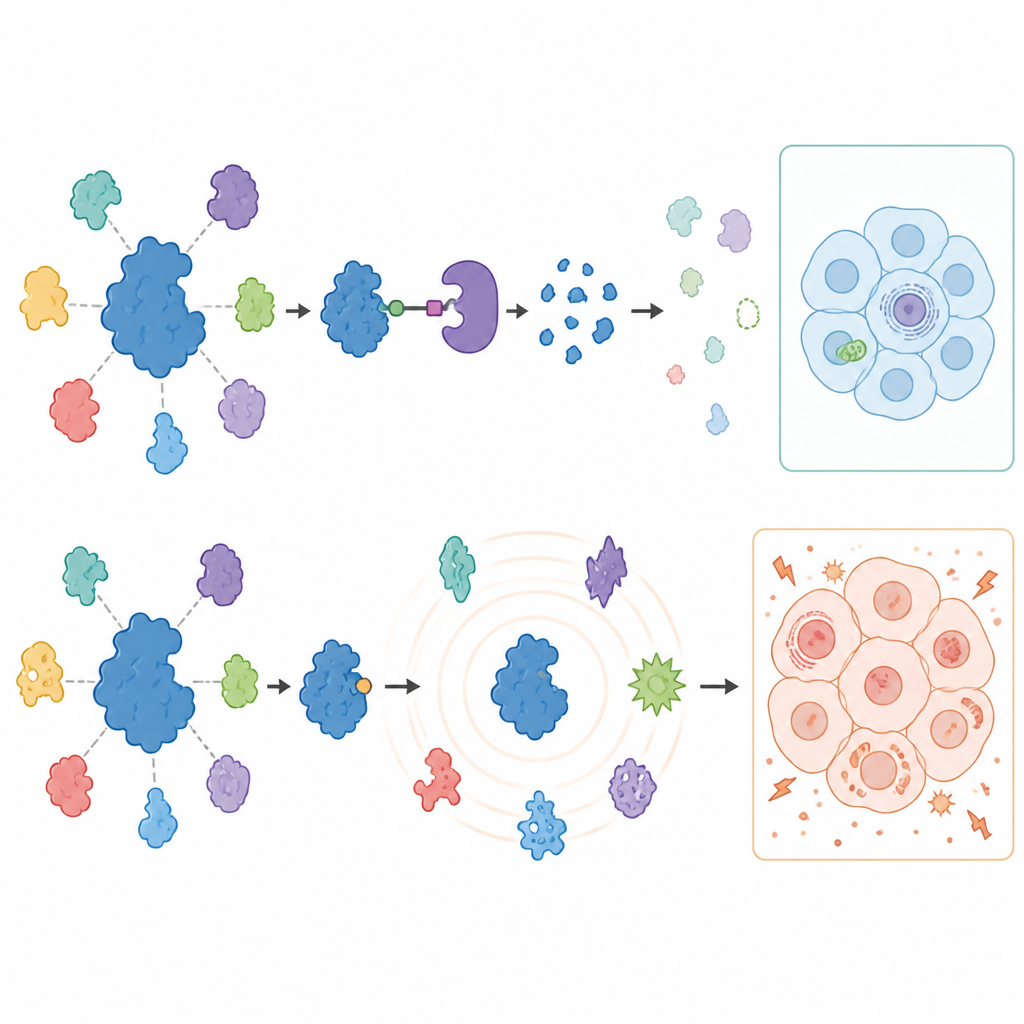
Wanneer blokkering te ver buiten het doel schiet
Remmers vertelden een heel ander verhaal op langere termijn. De eerste dag weerspiegelde het patroon van eiwitveranderingen grotendeels wat met degraders werd gezien, wat wees op werkelijke USP7-functies. Maar na drie dagen behandeling veroorzaakten de remmers een golf van brede en soms vreemde eiwitverschuivingen, inclusief het verschijnen van eiwitten die normaal niet in deze kankers voorkomen. De cellen gingen ook zwaar leunen op suiker, toonden verminderde capaciteit om energie in hun mitochondriën te genereren, en werden vatbaar voor celdood wanneer glucose beperkt was. Cruciaal is dat deze metabole verstoringen ook optraden in melanoomcellen waarin USP7 door genetische verwijdering was uitgeschakeld, wat aantoont dat ze werden veroorzaakt door off-target effecten van de remmers en niet door USP7 zelf.
Wat dit betekent voor toekomstige kankertherapieën
Dit werk laat zien dat zorgvuldig ontworpen degraders USP7 met hoge precisie kunnen verwijderen en een gefocuste set van echte downstream-effecten op genregulatie in solide kankers blootleggen. Daarentegen kunnen zelfs goed gekarakteriseerde remmers die in vroege tests schoon lijken, bij langdurig gebruik wijdverspreide, USP7-onafhankelijke veranderingen teweegbrengen. Voor wetenschappers en geneesmiddelenontwikkelaars is de boodschap duidelijk: degraders zijn krachtige instrumenten om schoon te ontleden wat een enkel eiwit werkelijk doet in verschillende kankers, terwijl remmers het meest geschikt zijn voor kortetermijnonderzoeken van activiteit. Samen openen deze complementaire tools een helderdere weg om USP7 en verwante eiwitten in kankertherapie te begrijpen en uiteindelijk te benutten.
Bronvermelding: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Trefwoorden: USP7, PROTAC-degrader, kankercellen, eiwitremming, celmetabolisme