Clear Sky Science · pl
Ukierunkowana degradacja USP7 w komórkach nowotworów litych ujawnia odmienne efekty degraderów deubikwitynazy i inhibitorów
Dlaczego rozbicie jednego białka ma znaczenie w raku
Leczenie raka często polega na blokowaniu aktywności szkodliwych białek, ale rosnące zainteresowanie budzi pomysł całkowitego usunięcia tych białek z komórek. Badanie koncentruje się na białku USP7, które chroni inne białka przed naturalnym rozkładem, i stawia proste, ale mające duże konsekwencje pytanie: czy lepiej tymczasowo wyłączyć USP7, czy pozbyć się go całkowicie? Porównując te dwie strategie w komórkach guzów litych pochodzących z raka trzustki i czerniaka, badacze odkrywają istotne różnice ważne dla projektowania bezpieczniejszych i bardziej precyzyjnych leków. 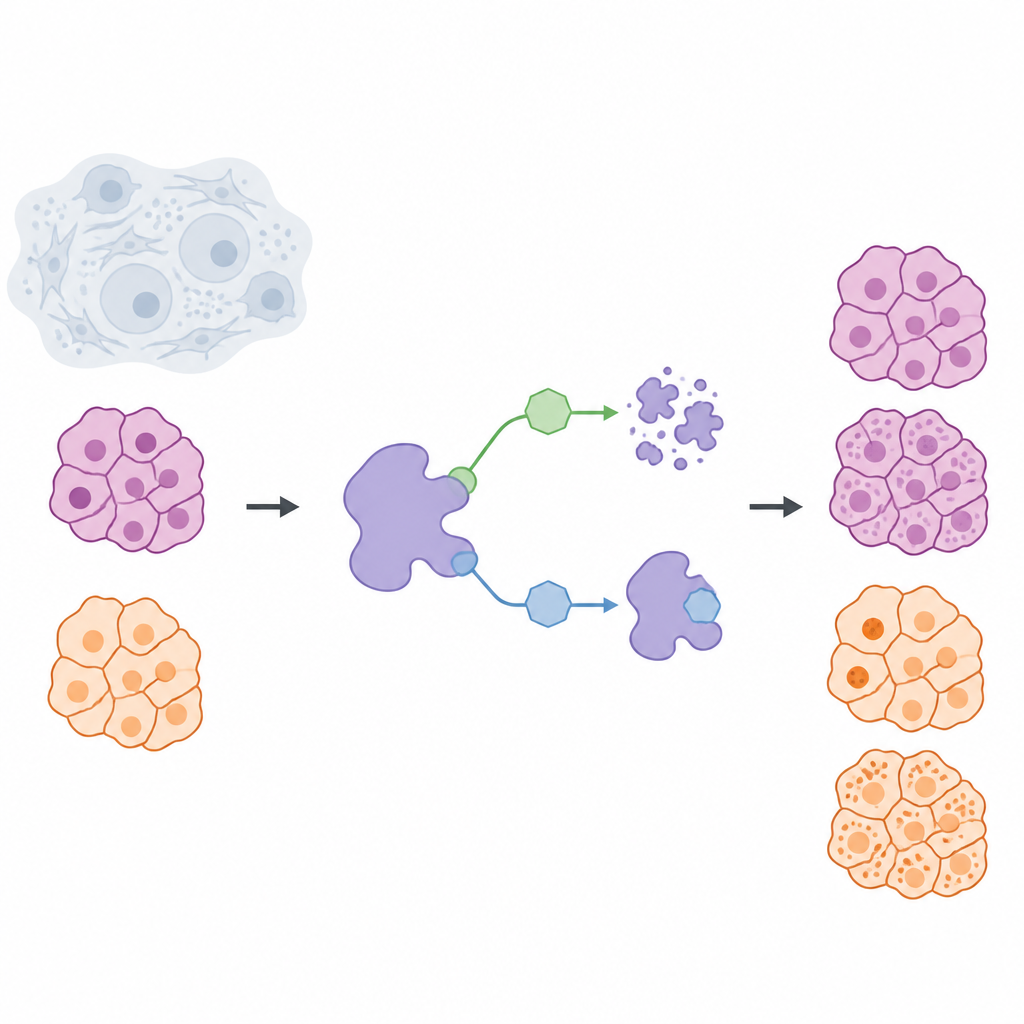
Dwa różne narzędzia do kontrolowania tego samego celu
Zespół zbudował chemiczne narzędzia do kontrolowania USP7 w żywych komórkach na dwa odmienne sposoby. Jeden zestaw cząsteczek, zwany inhibitorami, przyłącza się do USP7 i hamuje jego aktywność, podczas gdy samo białko pozostaje na miejscu. Drugi zestaw, zwany degraderami, działa jak znaczniki usuwania: przyciągają USP7 do komórek systemu utylizacji, dzięki czemu białko jest rozkładane i usuwane. Aby porównanie było uczciwe, naukowcy najpierw zaprojektowali wysoce selektywny inhibitor, NK192, który silnie wiąże USP7 i rzadko oddziałuje z innymi białkami. Na jego bazie opracowali następnie serię degraderów, które zarówno rozpoznają USP7, jak i rekrutują system utylizacji komórkowej znany jako VHL, pozwalając na efektywne usuwanie USP7 z komórek nowotworowych.
Specjalnie zaprojektowane „usuwacze” dla różnych komórek nowotworowych
Testując bibliotekę degraderów w liniach komórkowych raka trzustki i czerniaka, badacze odkryli, że kształt i sztywność łącznika między częścią wiążącą USP7 a rekrutującą VHL silnie wpływają na wydajność. Po kilku rundach projektowania i testów wyłoniono dwa wyróżniające się degradery: NK250, działający najlepiej w komórkach raka trzustki, oraz NK266, bardziej skuteczny w komórkach czerniaka. Te cząsteczki mogły niemal całkowicie usunąć USP7 przy bardzo niskich dawkach, a badania kontrolne potwierdziły, że efekt zależał od zamierzonej drogi utylizacji. Przy użyciu czułych metod autorzy wykazali, że szczególnie NK250 tworzy stabilny trójelementowy kompleks z USP7 i VHL, co wyjaśnia jego szybką aktywność.
Zbliżenie: co zmienia się wewnątrz komórki
Aby zobaczyć, co dzieje się z pozostałą częścią komórki, gdy USP7 jest zablokowany lub usunięty, naukowcy zmierzyli tysiące białek w leczonych komórkach nowotworowych przy użyciu zaawansowanej spektrometrii mas. Degradery wywołały zaskakująco skoncentrowaną odpowiedź: USP7 zniknęło, a ograniczony zestaw znanych partnerów, szczególnie składniki maszyny wyciszającej geny zwanej kompleksem Polycomb, uległ obniżeniu w obu typach nowotworów. Zmiany te zdjąły hamulce z niektórych genów, które zwykle są wyciszone, potwierdzając, że USP7 wspiera określone programy wyciszania genów. Co ważne, wielu wcześniej sugerowanych partnerów USP7 nie zmieniło się w tych nowotworach litych, podkreślając, że rola USP7 silnie zależy od typu komórek. 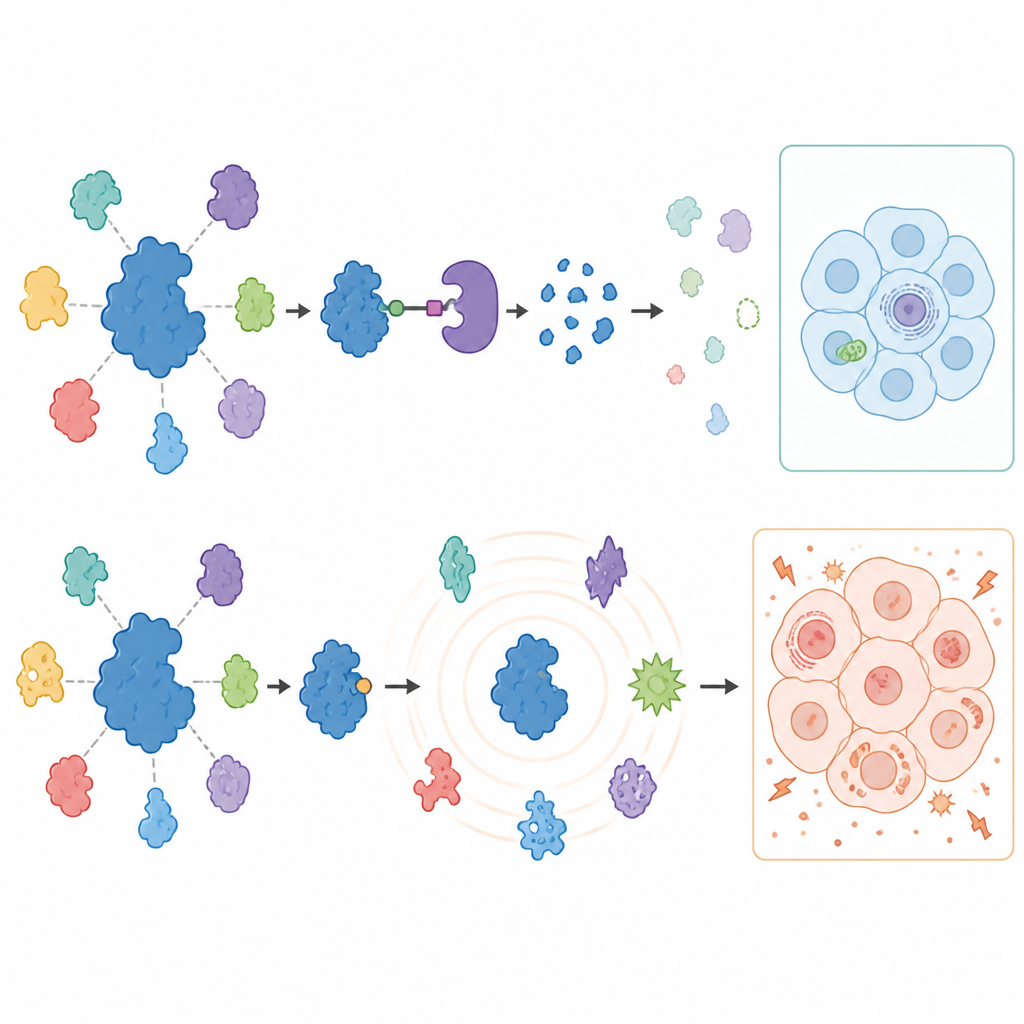
Kiedy blokowanie wykracza daleko poza cel
Inhibitory pokazały bardzo inną historię przy dłuższym czasie działania. Przez pierwszą dobę wzór zmian białkowych w dużej mierze odzwierciedlał to, co zaobserwowano przy degraderach, wskazując na autentyczne funkcje USP7. Jednak po trzech dniach leczenia inhibitory spowodowały falę szerokich i czasem dziwnych przesunięć białkowych, w tym pojawienie się białek rzadko występujących w tych nowotworach. Komórki zaczęły też silnie polegać na cukrze, wykazały zmniejszoną zdolność do generowania energii w mitochondriach i stały się podatne na śmierć komórkową przy ograniczeniu glukozy. Co kluczowe, te zaburzenia metaboliczne wystąpiły także w komórkach czerniaka, w których USP7 zostało usunięte przez edycję genową, co dowodzi, że były one spowodowane działaniami pozatargetowymi inhibitorów, a nie brakiem USP7.
Co to oznacza dla przyszłych leków przeciwnowotworowych
Praca ta pokazuje, że starannie zaprojektowane degradery mogą usuwać USP7 z wysoką precyzją, ujawniając skoncentrowany zestaw rzeczywistych efektów wtórnych związanych z kontrolą genów w nowotworach litych. W przeciwieństwie do tego, nawet dobrze scharakteryzowane inhibitory, które wydają się czyste w wczesnych testach, mogą wywołać szerokie, niezależne od USP7 zmiany przy dłuższym stosowaniu. Dla naukowców i twórców leków przesłanie jest jasne: degradery są potężnym narzędziem do precyzyjnego rozpoznania funkcji pojedynczego białka w różnych nowotworach, podczas gdy inhibitory najlepiej stosować do krótkoterminowego testowania aktywności. Razem te komplementarne narzędzia otwierają jaśniejszą drogę do zrozumienia i ostatecznego wykorzystania USP7 oraz pokrewnych białek w terapii nowotworowej.
Cytowanie: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Słowa kluczowe: USP7, PROTAC degrader, komórki nowotworowe, inhibicja białka, metabolizm komórkowy