Clear Sky Science · sv
Målinriktad nedbrytning av USP7 i solida cancerceller avslöjar skilda effekter av deubikvitinas-degraderare och hämmare
Varför nedbrytning av ett enda protein spelar roll för cancer
Cancerbehandlingar syftar ofta till att blockera aktiviteten hos skadliga proteiner, men en växande idé är att helt ta bort dessa proteiner från cellerna. Denna studie undersöker ett protein kallat USP7, som hjälper andra proteiner att undvika naturlig nedbrytning, och ställer en enkel fråga med stora konsekvenser: är det bättre att tillfälligt stänga av USP7 eller att bli av med det helt? Genom att jämföra dessa två strategier i solida tumörceller från pankreascancer och melanom avslöjar forskarna viktiga skillnader som är betydelsefulla för utformningen av säkrare och mer precisa läkemedel. 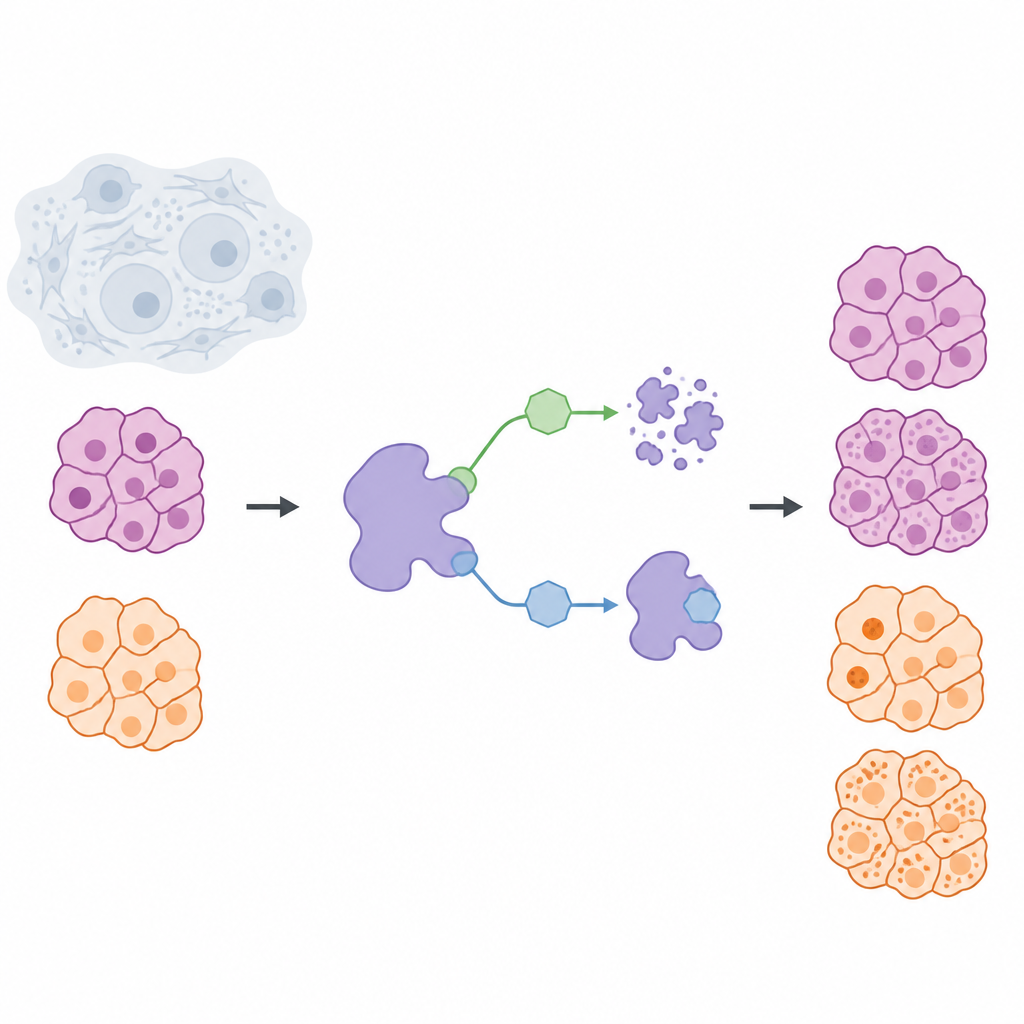
Två olika verktyg för att kontrollera samma mål
Forskargruppen byggde en kemisk verktygslåda för att styra USP7 i levande celler på två olika sätt. En uppsättning molekyler, kallade hämmare, binder till USP7 och stoppar dess aktivitet medan proteinet självt förblir närvarande. Den andra uppsättningen, kallad degraderare, fungerar mer som riktade borttagningsetiketter: de för USP7 i kontakt med cellens avfallshanteringsmaskineri så att proteinet bryts ned och rensas bort. För att göra jämförelsen rättvis designade forskarna först en högselektiv hämmare, NK192, som binder starkt till USP7 och sällan påverkar andra proteiner. Utifrån denna stomme konstruerade de sedan en serie degraderarmolekyler som både kan känna igen USP7 och rekrytera ett cellulärt nedbrytningssystem känt som VHL, vilket gör att de effektivt kan avlägsna USP7 från cancerceller.
Specialanpassade borttagare för olika cancerceller
När forskarna testade sitt degraderbibliotek i pankreas- och melanomcellinjer upptäckte de att form och styvhet hos länken mellan USP7-bindande delen och VHL-rekryterande delen starkt påverkade prestandan. Efter flera omgångar av design och testning identifierade de två framstående degraderare: NK250, som fungerar bäst i pankreascellinjer, och NK266, som är mer effektiv i melanomceller. Dessa molekyler kunde nästan helt avlägsna USP7 vid mycket låga doser, och uppföljande experiment bekräftade att effekten berodde på den avsedda nedbrytningsvägen. Med känsliga analyser visade teamet att NK250 i synnerhet bildar ett stabilt treparts-komplex med USP7 och VHL, vilket förklarar dess snabba verkan.
Inzoomning på vad som förändras inne i cellen
För att se vad som händer i resten av cellen när USP7 blockeras eller tas bort mätte forskarna tusentals proteiner i behandlade cancerceller med avancerad massespektrometri. Degraderare gav ett överraskande fokuserat svar: USP7 försvann, och en begränsad uppsättning kända partnerproteiner, särskilt komponenter i ett genavstängningsmaskineri kallat Polycomb-komplexet, minskade i båda cancertyperna. Dessa förändringar lättade på bromsarna för vissa gener som normalt hålls tysta, vilket bekräftar att USP7 stöder specifika genavstängningsprogram. Viktigt är att många tidigare föreslagna USP7-partners inte förändrades i dessa solida cancerceller, vilket belyser att USP7:s roll varierar starkt mellan celltyper. 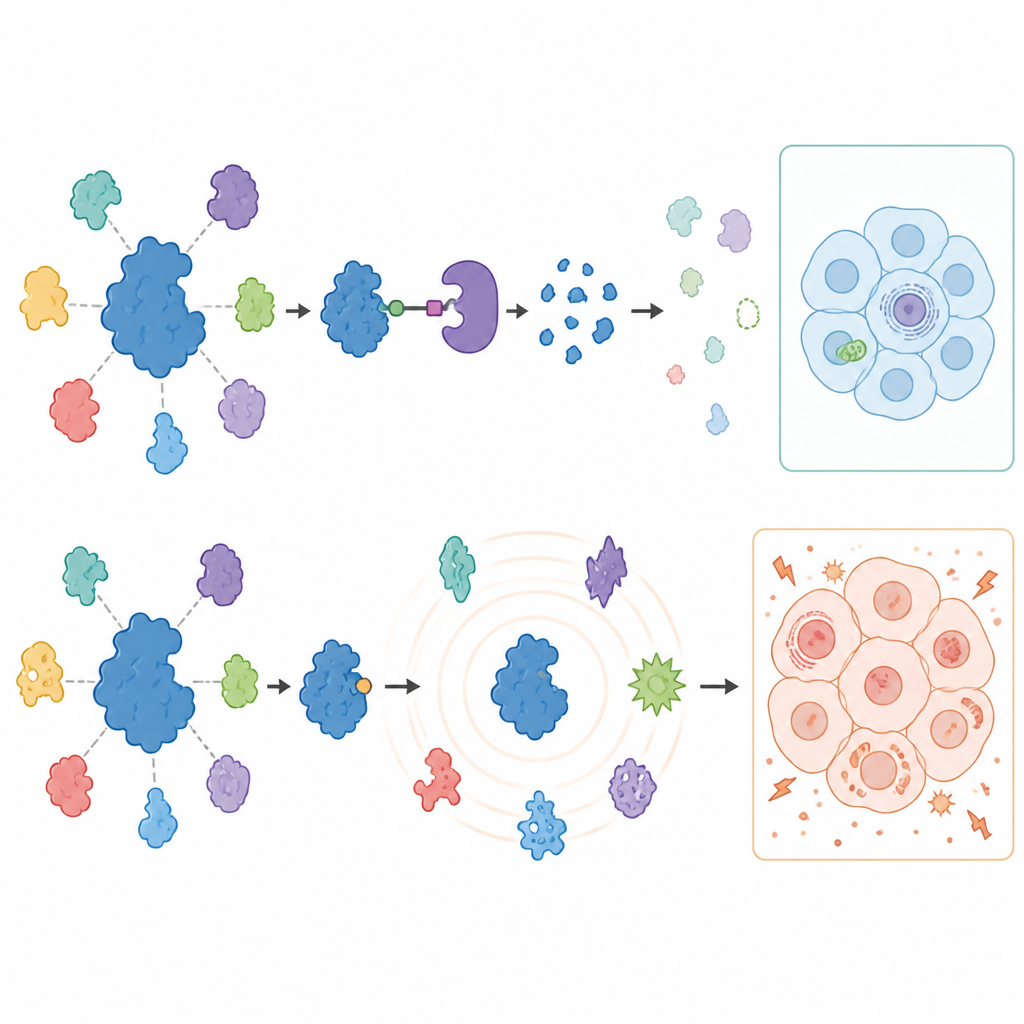
När blockering går för långt bortom målet
Hämmare berättade en mycket annorlunda historia över längre tid. Under den första dagen speglade mönstret av proteinförändringar till stor del vad som sågs med degraderare, vilket pekar på verkliga USP7-funktioner. Men efter tre dagars behandling orsakade hämmarna en våg av breda och ibland ovanliga proteinförskjutningar, inklusive uppträdandet av proteiner som normalt inte återfinns i dessa cancerformer. Cellerna började också bli starkt beroende av socker, visade minskad förmåga att generera energi i sina mitokondrier och blev benägna att dö när glukos var begränsat. Avgörande är att dessa metabola störningar fortfarande uppstod i melanomceller där USP7 hade tagits bort genom genredigering, vilket bevisar att de orsakades av hämmarnas off-target-verkningar snarare än av USP7 självt.
Vad detta betyder för framtida cancerläkemedel
Denne studie visar att noggrant designade degraderare kan avlägsna USP7 med hög precision och avslöja en fokuserad uppsättning sanna downstream-effekter på genreglering i solida cancerformer. I kontrast kan även välkaraktäriserade hämmare som verkar rena i tidiga tester utlösa omfattande, USP7-oberoende förändringar vid långvarig användning. För forskare och läkemedelsutvecklare är budskapet tydligt: degraderare är kraftfulla verktyg för att rent dissekera vad ett enskilt protein verkligen gör i olika cancerformer, medan hämmare är bäst som korttidsverktyg för att testa aktivitet. Tillsammans öppnar dessa komplementära verktyg en klarare väg för att förstå och så småningom utnyttja USP7 och närliggande proteiner i cancerterapi.
Citering: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Nyckelord: USP7, PROTAC degrader, cancerceller, proteininhibering, cellmetabolism