Clear Sky Science · ar
التحلل الموجه لـ USP7 في خلايا السرطان الصلبة يكشف تأثيرات مميزة لمحللّي ومثبطات الديوتبيكويناز
لماذا يهم تحطيم بروتين واحد لمرض السرطان
غالبًا ما تهدف علاجات السرطان إلى إيقاف نشاط البروتينات الضارة، لكن فكرة متنامية هي إزالة هذه البروتينات من الخلايا تمامًا. تنظر هذه الدراسة إلى بروتين يُدعى USP7، الذي يساعد بروتينات أخرى على تجنب التحلل الطبيعي، وتطرح سؤالًا بسيطًا بعواقب كبيرة: هل من الأفضل إيقاف USP7 مؤقتًا أم التخلص منه تمامًا؟ بمقارنة هاتين الاستراتيجيتين في خلايا أورام صلبة من سرطان البنكرياس والورم الميلانيني، يكشف الباحثون عن اختلافات مهمة لها أثر في تصميم أدوية أكثر أمانًا ودقة. 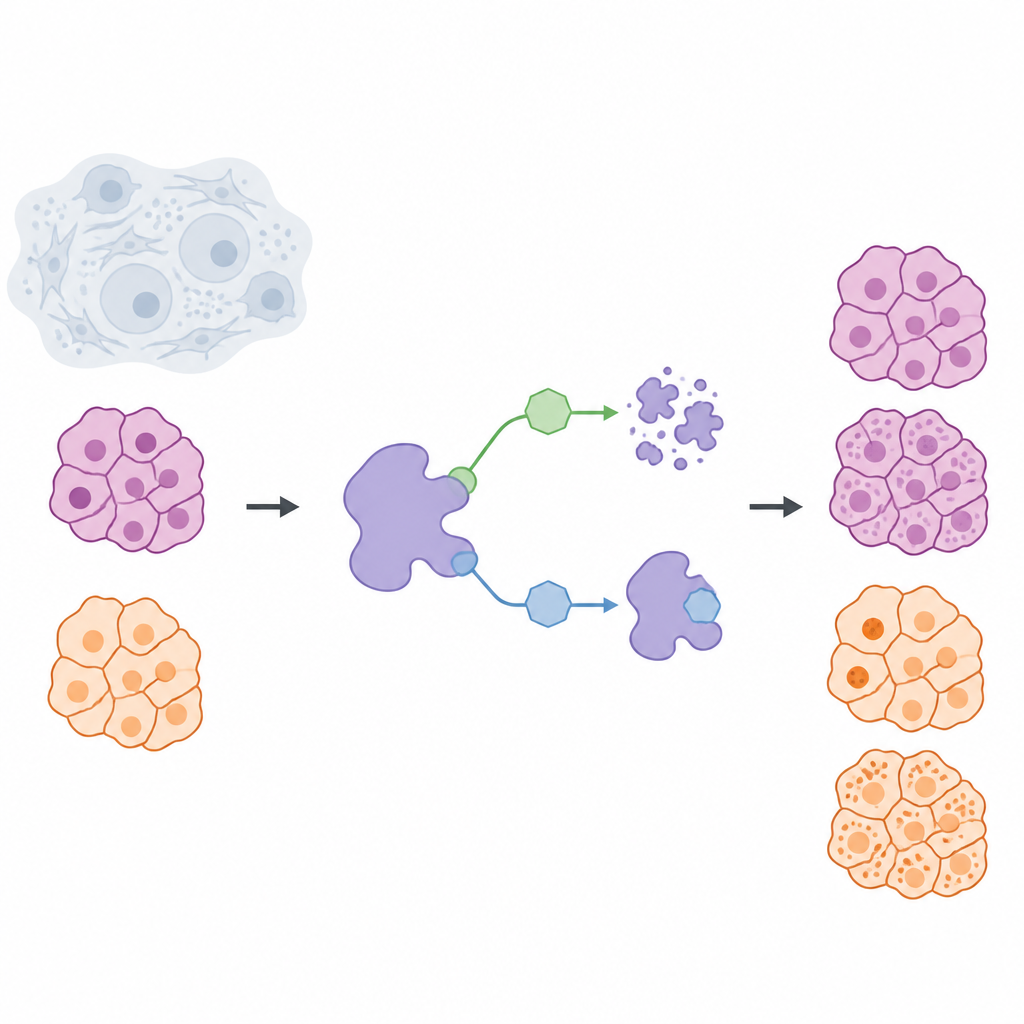
أداتان مختلفتان للتحكم في نفس الهدف
بنى الفريق مجموعة كيميائية للتحكم في USP7 داخل الخلايا بطريقتين مميزتين. مجموعة من الجزيئات، تُسمى المثبطات، ترتبط بـ USP7 وتوقف نشاطه بينما يبقى البروتين في مكانه. أما المجموعة الثانية، المسماة المحللات، فتعمل كعلامات إزالة موجهة: تجلب USP7 إلى آلية التخلص الخلوي حتى يُتفكك البروتين ويُزال. لجعل المقارنة عادلة، صمّم العلماء أولًا مثبطًا انتقائيًا للغاية، NK192، يرتبط بقوة بـ USP7 ونادرًا ما يؤثر على بروتينات أخرى. ومن هذا القالب طوروا سلسلة من جزيئات المحلل التي يمكنها التعرف على USP7 وتجند نظام التخلص الخلوي المعروف باسم VHL، مما يسمح لها بإزالة USP7 من خلايا السرطان بكفاءة.
مزيّلات مصممة خصيصًا لأنواع سرطانية مختلفة
عند اختبار مكتبة المحللات في خطوط خلايا سرطان البنكرياس والورم الميلانيني، اكتشفوا أن شكل الوصلة وصلابتها بين جزء الربط بـ USP7 والجزء المجند لـ VHL أثر بشكل كبير على الأداء. بعد عدة جولات من التصميم والاختبار، توصلوا إلى محللين بارزين: NK250، الذي يعمل بأفضل شكل في خلايا سرطان البنكرياس، وNK266، الأكثر فاعلية في خلايا الورم الميلانيني. كانت هذه الجزيئات قادرة على إزالة USP7 تقريبًا تمامًا بجرعات منخفضة جدًا، وأكدت تجارب لاحقة أن التأثير يعتمد على مسار التخلص المخطط له. وباستخدام اختبارات حساسة، أظهر الفريق أن NK250 على وجه الخصوص يشكل مركبًا مستقرًا ثلاثي الأجزاء مع USP7 وVHL، ما يفسر فعاليته السريعة.
تقريبًا لما يتغير داخل الخلية
لرؤية ما يحدث لباقي الخلية عندما يُوقف أو يُزال USP7، قاس العلماء آلاف البروتينات في خلايا السرطان المعالجة باستخدام مطيافية الكتلة المتقدمة. أنتجت المحللات استجابة مركزة مفاجِئة: اختفى USP7، وتراجع مجموعة محدودة من البروتينات الشريكة المعروفة، خصوصًا مكونات آلة إسكات الجينات المسماة مركب بوليكوم، في كلا نوعي السرطان. راحت هذه التغيرات ترفع المكابح عن بعض الجينات التي عادة ما تُحافظ على كتمها، مؤكدة أن USP7 يدعم برامج إسكات جينية محددة. ومن المهم أن العديد من الشركاء المقترحين سابقًا لـ USP7 لم تتغير مستوياتهم في هذه الخلايا السرطانية الصلبة، مما يبرز أن دور USP7 يختلف بشدة بين أنواع الخلايا. 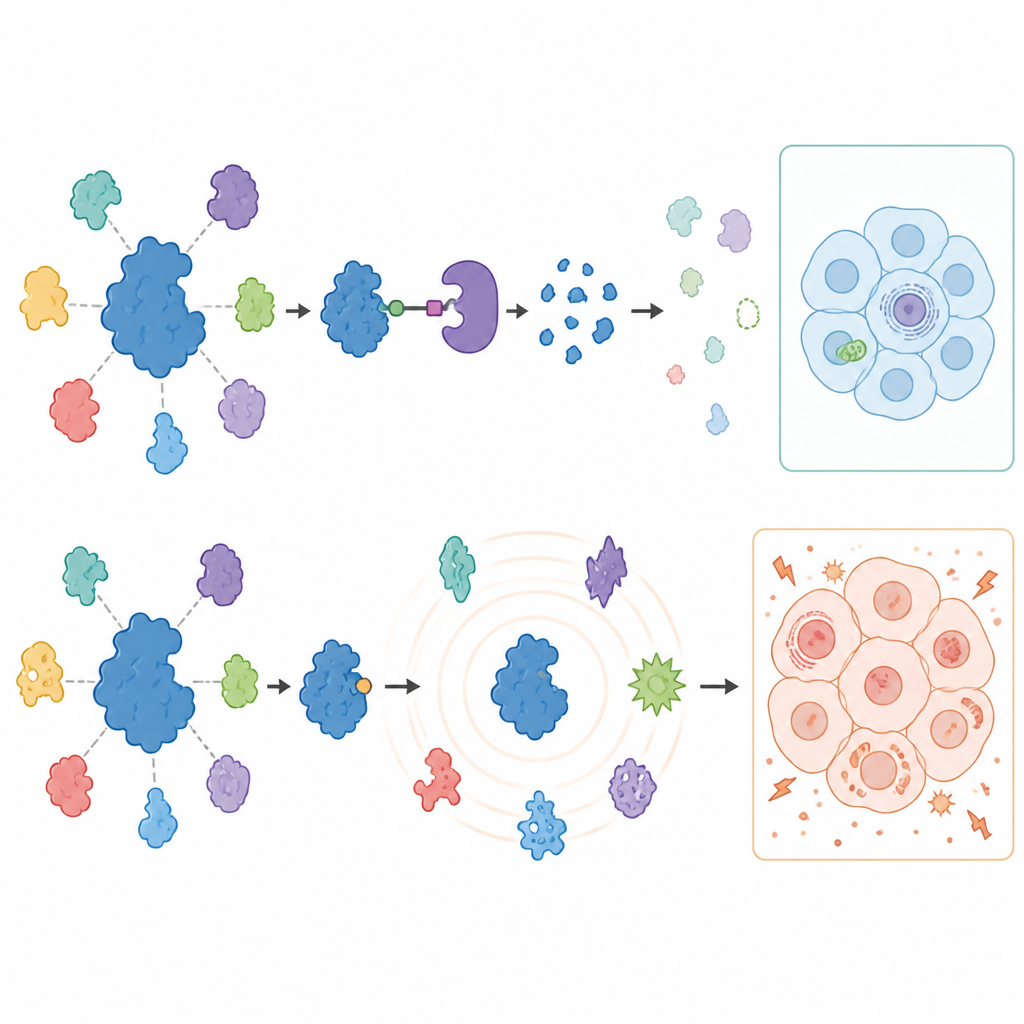
عندما يتجاوز التثبيط الهدف كثيرًا
سردت المثبطات قصة مختلفة تمامًا على مدى أطول. في اليوم الأول، طابعت أنماط تغير البروتينات إلى حد كبير ما شوهد مع المحللات، مشيرة إلى وظائف حقيقية لـ USP7. لكن بعد ثلاثة أيام من العلاج، سببت المثبطات موجة من التحولات البروتينية الواسعة وأحيانًا الغريبة، بما في ذلك ظهور بروتينات غير معتادة في هذه الأنواع من السرطان. كما بدأت الخلايا تعتمد بشكل كبير على السكر، وأظهرت قدرة أقل على توليد الطاقة في الميتوكوندريا، وأصبحت عرضة للموت الخلوي عندما كان الجلوكوز محدودًا. والأهم من ذلك، أن هذه الاضطرابات الأيضية حدثت أيضًا في خلايا الورم الميلانيني التي أُزيل فيها USP7 عن طريق التعديل الجيني، مما يثبت أنها ناجمة عن أفعال خارج الهدف للمثبطات وليس عن USP7 نفسه.
ماذا يعني هذا لأدوية السرطان المستقبلية
تُظهر هذه الدراسة أن المحللات المصممة بعناية يمكنها إزالة USP7 بدقة عالية، مكشوفة مجموعة مركزة من التأثيرات الحقيقية التالية على التحكم الجيني في السرطانات الصلبة. بالمقابل، حتى المثبطات الموصوفة جيدًا والتي تبدو نقية في الاختبارات المبكرة يمكن أن تُحدث تغييرات واسعة مستقلة عن USP7 عند استخدامها لفترات أطول. للعلماء ومطوري الأدوية، الرسالة واضحة: المحللات أدوات قوية لتفكيك ما يفعله بروتين واحد فعلًا في سرطانات مختلفة بشكلٍ نظيف، بينما تُعدّ المثبطات أفضل للاختبارات قصيرة المدى للنشاط. معًا، تفتح هاتان الأداتان المتكاملتان طريقًا أوضح لفهم واستغلال USP7 والبروتينات ذات الصلة في علاج السرطان.
الاستشهاد: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
الكلمات المفتاحية: USP7, مُحلّل PROTAC, خلايا سرطانية, تثبيط البروتين, استقلاب الخلية