Clear Sky Science · pt
Degradação direcionada de USP7 em células de câncer sólido revela efeitos distintos de degradadores e inibidores de desubiquitinase
Por que degradar uma proteína importa no câncer
Tratamentos contra o câncer costumam visar o bloqueio da atividade de proteínas prejudiciais, mas uma ideia em ascensão é remover essas proteínas das células por completo. Este estudo examina uma proteína chamada USP7, que protege outras proteínas da degradação natural, e faz uma pergunta simples com grandes consequências: é melhor desligar a USP7 temporariamente ou eliminá‑la totalmente? Ao comparar essas duas estratégias em células de tumores sólidos de câncer de pâncreas e melanoma, os pesquisadores revelam diferenças importantes que importam para o desenho de fármacos mais seguros e precisos. 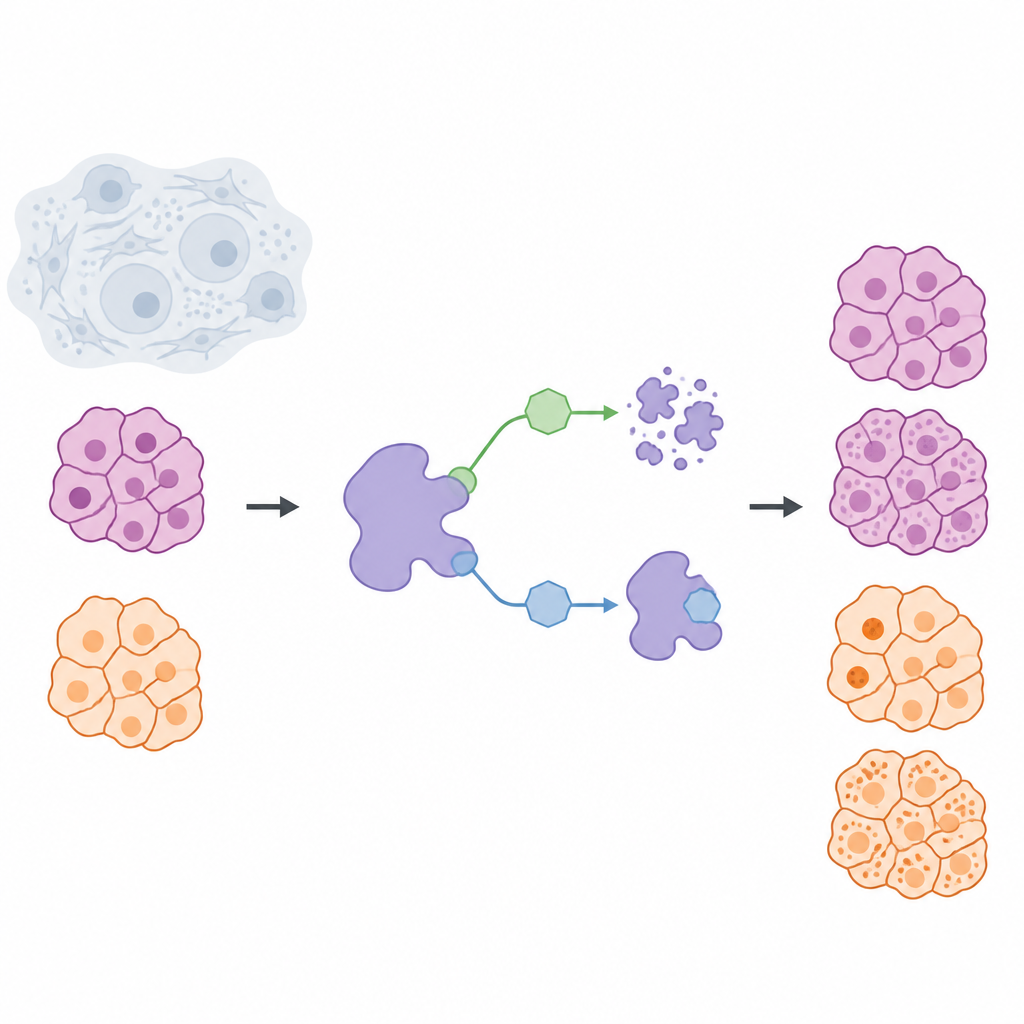
Dois instrumentos diferentes para controlar o mesmo alvo
A equipe construiu uma caixa de ferramentas química para controlar a USP7 em células vivas de duas maneiras distintas. Um conjunto de moléculas, chamadas inibidores, liga‑se à USP7 e interrompe sua atividade enquanto a própria proteína permanece presente. O segundo conjunto, chamados degradadores, age mais como etiquetas de remoção guiada: eles aproximam a USP7 da maquinaria de descarte da célula para que a proteína seja degradada e eliminada. Para tornar a comparação justa, os cientistas primeiro desenvolveram um inibidor altamente seletivo, NK192, que se liga fortemente à USP7 e raramente afeta outras proteínas. A partir desse esqueleto, então projetaram uma série de degradadores capazes tanto de reconhecer a USP7 quanto de recrutar um sistema celular de eliminação conhecido como VHL, permitindo remover a USP7 de células cancerígenas de forma eficiente.
Removedores feitos sob medida para diferentes células cancerígenas
Ao testar sua biblioteca de degradadores em linhagens celulares de pâncreas e melanoma, os pesquisadores descobriram que a forma e a rigidez do conector entre a parte que se liga à USP7 e a parte que recruta o VHL influenciavam fortemente o desempenho. Após várias rodadas de desenho e testes, chegaram a dois degradadores de destaque: NK250, que funciona melhor em células de câncer de pâncreas, e NK266, mais eficaz em células de melanoma. Essas moléculas puderam quase eliminar completamente a USP7 em doses muito baixas, e experimentos de acompanhamento confirmaram que o efeito dependia da via de descarte celular pretendida. Usando ensaios sensíveis, a equipe mostrou que o NK250 em particular forma um complexo estável de três partes com USP7 e VHL, explicando sua ação rápida.
Observando de perto o que muda dentro da célula
Para ver o que acontece ao resto da célula quando a USP7 é bloqueada ou removida, os cientistas mediram milhares de proteínas em células cancerígenas tratadas usando espectrometria de massa avançada. Os degradadores produziram uma resposta surpreendentemente focada: a USP7 desapareceu, e um conjunto limitado de parceiros conhecidos, especialmente componentes de uma máquina de silenciamento gênico chamada complexo Polycomb, diminuiu em ambos os tipos de câncer. Essas mudanças afrouxaram os freios sobre certos genes que normalmente são mantidos silenciosos, confirmando que a USP7 sustenta programas específicos de silenciamento gênico. Importante, muitos parceiros de USP7 previamente sugeridos não mudaram nessas células de câncer sólido, destacando que o papel da USP7 varia fortemente entre tipos celulares. 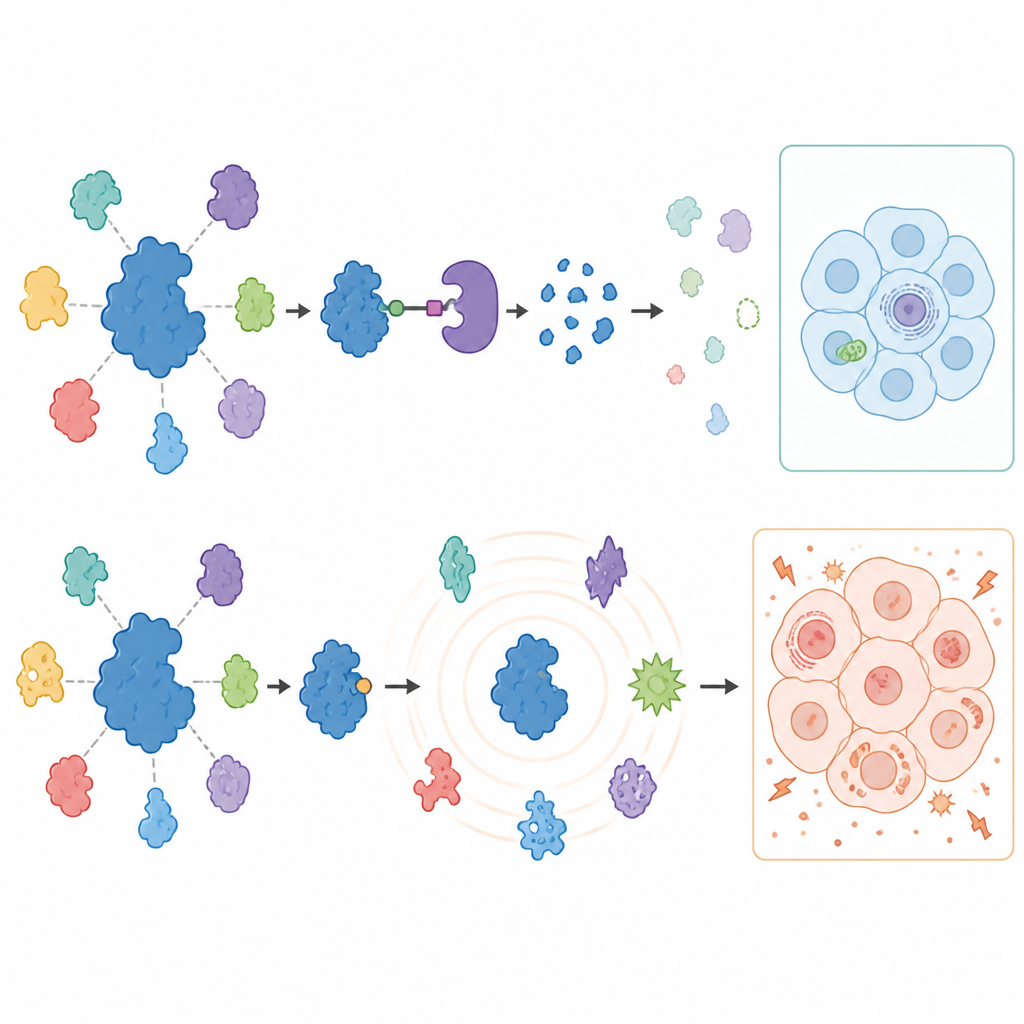
Quando o bloqueio vai muito além do alvo
Os inibidores contaram uma história bem diferente ao longo de tratamentos mais longos. No primeiro dia, o padrão de alterações proteicas espelhava em grande parte o observado com os degradadores, apontando para funções genuínas da USP7. Mas após três dias de tratamento, os inibidores causaram uma onda de mudanças proteicas amplas e às vezes atípicas, incluindo o aparecimento de proteínas não habitualmente presentes nesses cânceres. As células também passaram a depender fortemente de glicose, mostraram capacidade reduzida de gerar energia nas mitocôndrias e ficaram mais propensas à morte celular quando a glicose era limitada. Crucialmente, essas perturbações metabólicas ainda ocorriam em células de melanoma nas quais a USP7 havia sido removida por edição genética, provando que foram causadas por ações fora do alvo dos inibidores e não pela USP7 em si.
O que isso significa para futuros fármacos contra o câncer
Este trabalho mostra que degradadores cuidadosamente projetados podem remover a USP7 com alta precisão, revelando um conjunto focado de efeitos a jusante verdadeiros sobre o controle gênico em cânceres sólidos. Em contraste, mesmo inibidores bem caracterizados que parecem limpos em testes iniciais podem desencadear mudanças disseminadas, independentes de USP7, quando usados por períodos mais longos. Para cientistas e desenvolvedores de fármacos, a mensagem é clara: degradadores são ferramentas poderosas para dissecar de forma limpa o que uma única proteína realmente faz em diferentes cânceres, enquanto inibidores são mais indicados para testes de atividade de curto prazo. Juntas, essas ferramentas complementares abrem um caminho mais claro para entender e, eventualmente, explorar a USP7 e proteínas relacionadas na terapia do câncer.
Citação: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Palavras-chave: USP7, degradador PROTAC, células cancerígenas, inibição de proteína, metabolismo celular