Clear Sky Science · de
Zielgerichteter Abbau von USP7 in soliden Krebszellen zeigt unterschiedliche Effekte von Deubiquitinase-Degradatoren und -Inhibitoren
Warum der Abbau eines einzelnen Proteins für Krebs wichtig ist
Krebsbehandlungen zielen häufig darauf ab, die Aktivität schädlicher Proteine zu blockieren, doch eine zunehmende Idee ist, diese Proteine ganz aus der Zelle zu entfernen. In dieser Studie untersuchen die Forschenden ein Protein namens USP7, das andere Proteine vor dem natürlichen Abbau schützt, und stellen eine einfache Frage mit großen Konsequenzen: Ist es besser, USP7 vorübergehend auszuschalten oder es vollständig zu beseitigen? Durch den Vergleich dieser beiden Strategien in soliden Tumorzellen aus Pankreaskarzinom und Melanom enthüllen die Autorinnen und Autoren wichtige Unterschiede, die für die Entwicklung sicherer und präziser Medikamente relevant sind. 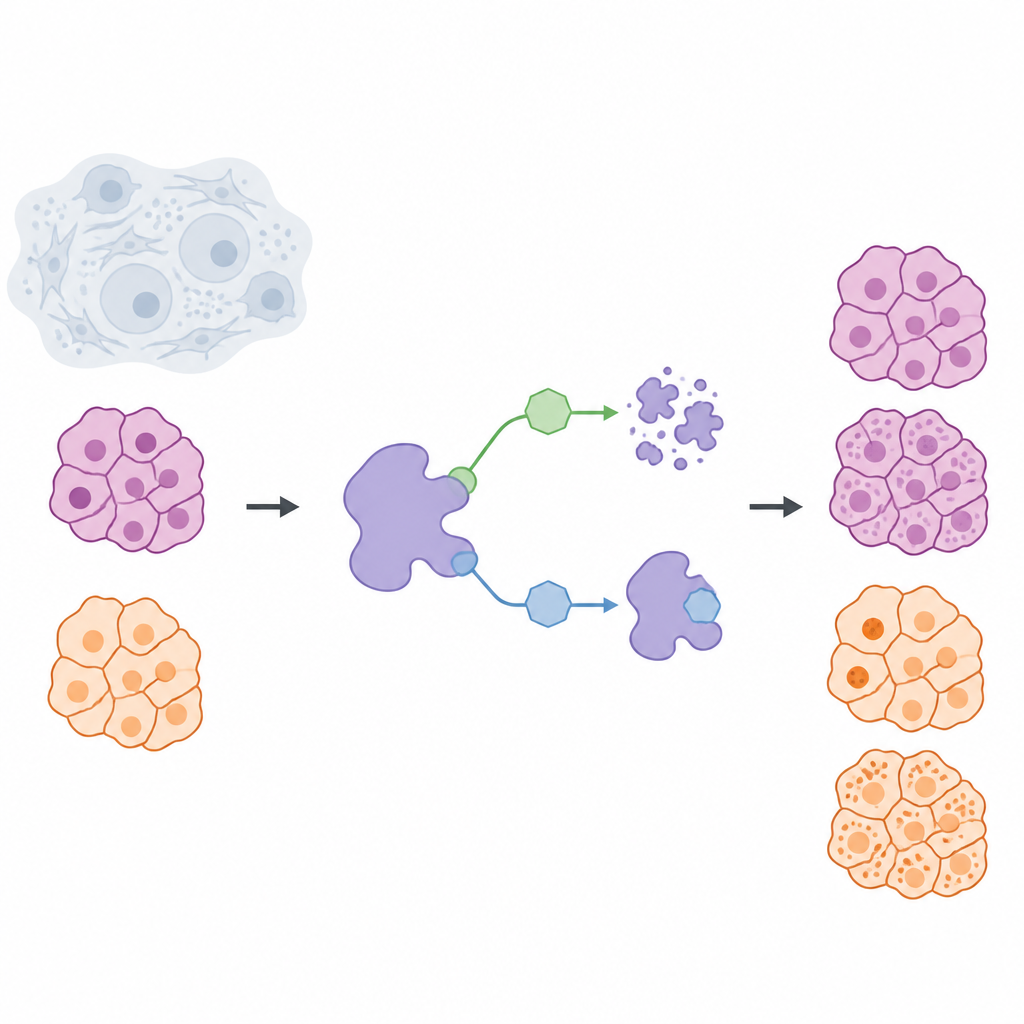
Zwei verschiedene Werkzeuge zur Kontrolle desselben Ziels
Das Team baute eine chemische Toolbox, um USP7 in lebenden Zellen auf zwei unterschiedliche Weisen zu steuern. Eine Gruppe von Molekülen, sogenannte Inhibitoren, bindet an USP7 und stoppt dessen Aktivität, während das Protein selbst in der Zelle verbleibt. Die zweite Gruppe, Degradatoren, wirken eher wie gezielte Entfernungsmarkierungen: Sie bringen USP7 mit dem zellulären Entsorgungssystem in Kontakt, sodass das Protein abgebaut und eliminiert wird. Um den Vergleich fair zu machen, entwarfen die Wissenschaftler zunächst einen hochselektiven Inhibitor, NK192, der USP7 stark bindet und kaum andere Proteine berührt. Auf dieser Grundlage entwickelten sie dann eine Reihe von Degradatoren, die sowohl USP7 erkennen als auch das zelluläre Entsorgungssystem VHL rekrutieren können, sodass USP7 in Krebszellen effizient entfernt wird.
Maßgeschneiderte Entferner für verschiedene Krebszellen
Als die Forschenden ihre Degradator-Bibliothek in Pankreas- und Melanomzelllinien testeten, stellten sie fest, dass Form und Steifigkeit des Linkers zwischen dem USP7-bindenden Teil und dem VHL-rekrutierenden Teil die Wirksamkeit stark beeinflussten. Nach mehreren Design- und Testzyklen identifizierten sie zwei herausragende Degradatoren: NK250, das in Pankreaskrebszellen am besten wirkt, und NK266, das in Melanomzellen wirksamer ist. Diese Moleküle konnten USP7 bei sehr niedrigen Dosen nahezu vollständig entfernen, und Folgeexperimente bestätigten, dass der Effekt vom vorgesehenen Entsorgungsweg abhängt. Mithilfe empfindlicher Assays zeigte das Team, dass insbesondere NK250 einen stabilen Dreierkomplex mit USP7 und VHL bildet, was seine schnelle Wirkung erklärt.
Hineinzoomen auf die zellulären Veränderungen
Um zu sehen, was mit der übrigen Zelle geschieht, wenn USP7 blockiert oder entfernt wird, maßen die Wissenschaftler tausende Proteine in behandelten Krebszellen mittels fortgeschrittener Massenspektrometrie. Degradatoren lösten eine überraschend fokussierte Antwort aus: USP7 verschwand und eine begrenzte Gruppe bekannter Partnerproteine, insbesondere Komponenten eines Gen-Silencing-Komplexes namens Polycomb, nahm in beiden Krebsarten ab. Diese Veränderungen lösten die Bremse bestimmter Gene, die normalerweise stillgehalten werden, und bestätigten, dass USP7 spezifische Gen-Silencing-Programme unterstützt. Wichtig ist, dass viele zuvor vorgeschlagene USP7-Partner in diesen soliden Krebszellen nicht verändert wurden, was hervorhebt, dass die Rolle von USP7 stark zwischen Zelltypen variiert. 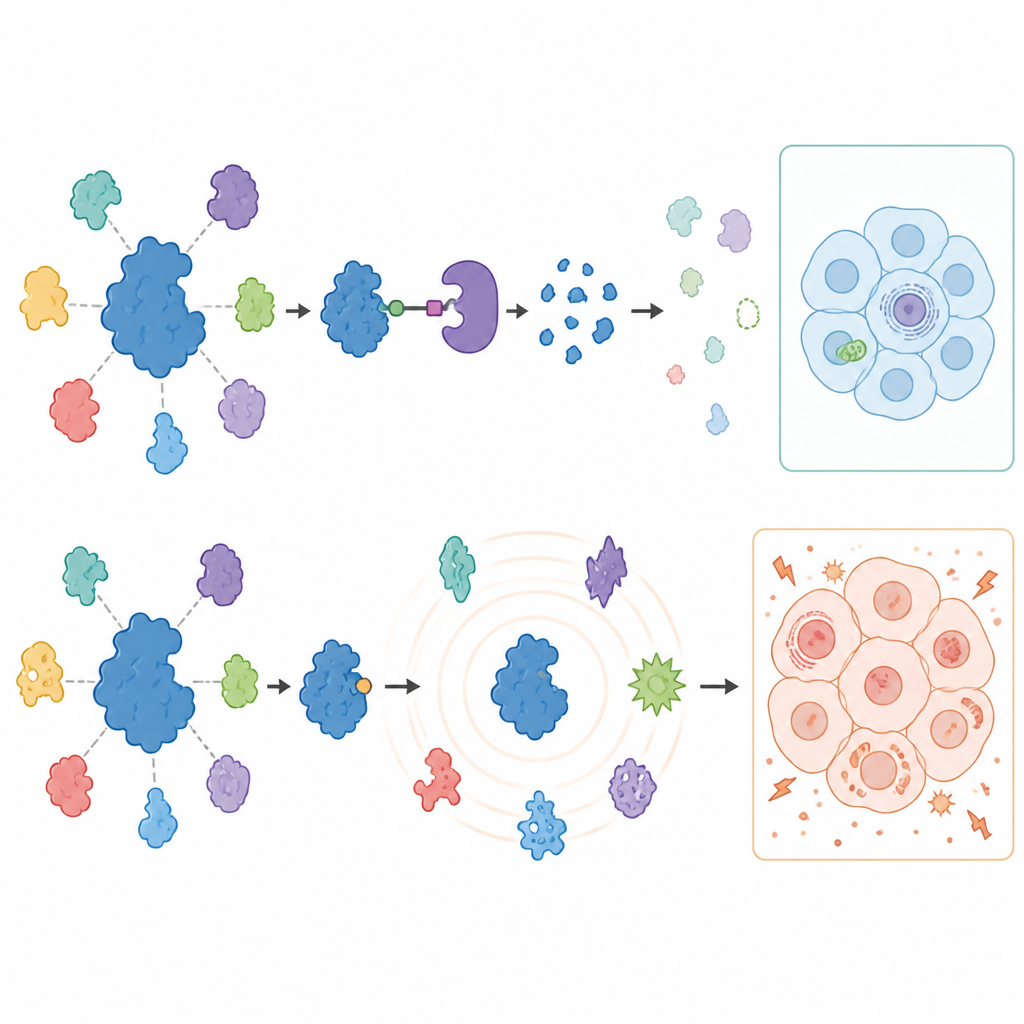
Wenn Blockade weit über das Ziel hinausgeht
Inhibitoren erzählten eine ganz andere Geschichte über längere Zeiträume. Am ersten Tag spiegelte das Muster der Proteinveränderungen weitgehend das wider, was mit Degradatoren beobachtet wurde, und wies auf echte USP7-Funktionen hin. Nach drei Tagen Behandlung jedoch verursachten die Inhibitoren eine Welle breiter und teils ungewöhnlicher Proteinverschiebungen, einschließlich des Auftretens von Proteinen, die in diesen Krebsarten normalerweise nicht vorkommen. Die Zellen begannen außerdem, sich stark auf Zucker zu verlassen, zeigten eine verringerte Fähigkeit, Energie in ihren Mitochondrien zu erzeugen, und wurden anfällig für Zelltod bei Glukosemangel. Entscheidend ist, dass diese metabolischen Störungen auch in Melanomzellen auftraten, in denen USP7 durch Geneditierung entfernt worden war, was beweist, dass sie durch Off-Target-Wirkungen der Inhibitoren und nicht durch USP7 selbst verursacht wurden.
Was das für zukünftige Krebsmedikamente bedeutet
Diese Arbeit zeigt, dass sorgfältig entwickelte Degradatoren USP7 mit hoher Präzision entfernen können und dabei eine fokussierte Reihe echter nachgeschalteter Effekte auf die Genkontrolle in soliden Tumoren offenlegen. Im Gegensatz dazu können selbst gut charakterisierte Inhibitoren, die in frühen Tests sauber erscheinen, bei längerer Anwendung weitreichende, USP7-unabhängige Veränderungen auslösen. Für Wissenschaftler und Wirkstoffentwickler ist die Botschaft klar: Degradatoren sind leistungsfähige Werkzeuge, um sauber zu klären, was ein einzelnes Protein in verschiedenen Krebsarten tatsächlich bewirkt, während Inhibitoren sich am besten für kurzfristige Aktivitätstests eignen. Zusammen eröffnen diese komplementären Werkzeuge einen klareren Weg zum Verständnis und letztlich zur therapeutischen Nutzung von USP7 und verwandten Proteinen bei Krebs.
Zitation: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Schlüsselwörter: USP7, PROTAC-Degradator, Krebszellen, Proteininhibition, Zellstoffwechsel