Clear Sky Science · tr
Katı tümör hücrelerinde USP7’nin hedefe yönelik yıkımı: deubiquitinaz degrader’ları ve inhibitörlerinin farklı etkilerini ortaya koyuyor
Tek bir proteinin parçalanmasının neden önemli olduğu
Kanser tedavileri sıklıkla zararlı proteinlerin etkinliğini engellemeyi hedefler, ancak öne çıkan bir yaklaşım bu proteinleri hücrelerden tamamen uzaklaştırmaktır. Bu çalışma, diğer proteinlerin doğal parçalanmasından kaçınmasına yardımcı olan USP7 adlı bir proteini inceliyor ve basit ama büyük sonuçları olan bir soru soruyor: USP7’yi geçici olarak kapatmak mı yoksa onu tamamen yok etmek mi daha iyi? Araştırmacılar, pankreas kanseri ve melanom kaynaklı katı tümör hücrelerinde bu iki stratejiyi karşılaştırarak daha güvenli ve daha hassas ilaç tasarımları için önem taşıyan farkları ortaya koyuyorlar. 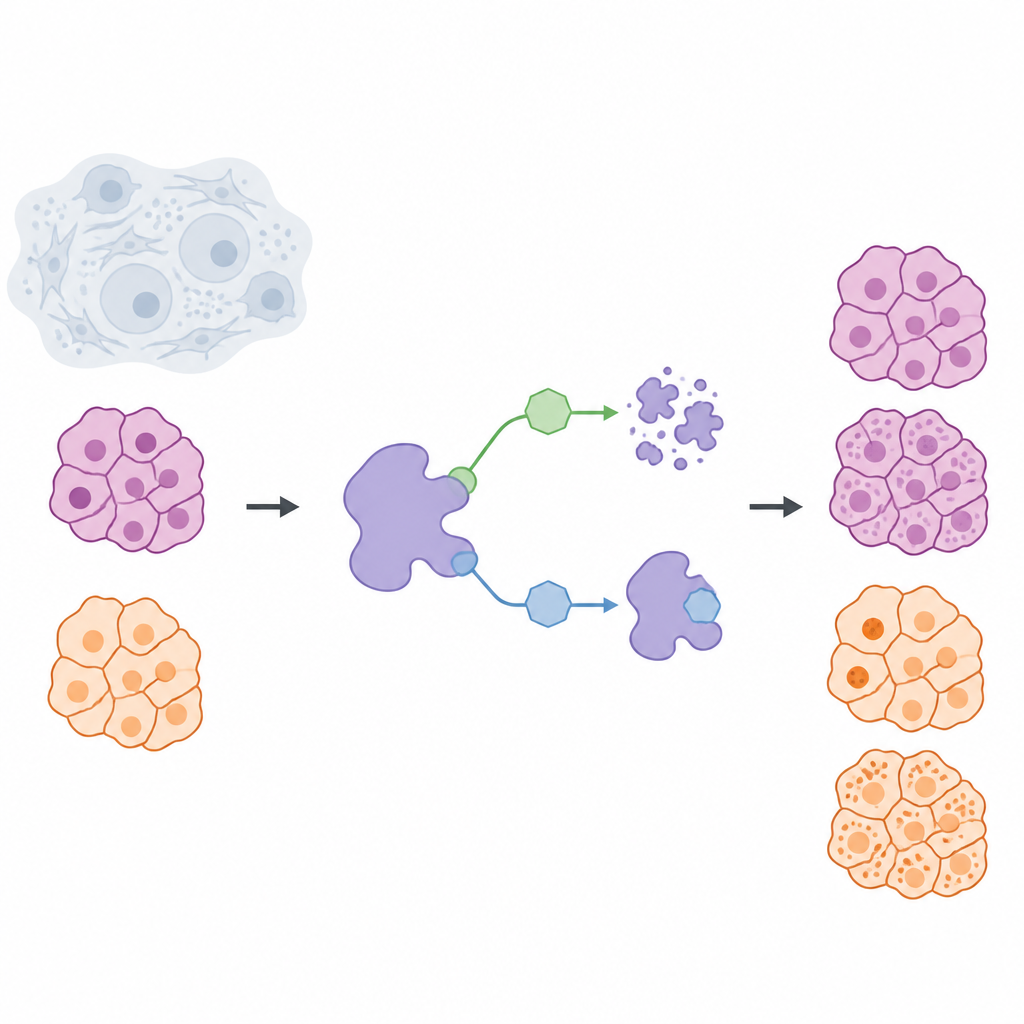
Aynı hedefi kontrol etmek için iki farklı araç
Takım, USP7’yi canlı hücrelerde iki farklı yolla kontrol etmek üzere bir kimyasal alet kutusu geliştirdi. Bir grup molekül —inhibitörler— USP7’ye tutunup etkinliğini durdururken proteinin kendisi yerinde kalır. İkinci grup —degrader’lar— daha çok kılavuzlu çıkarma etiketleri gibi davranır: USP7’yi hücrenin atık imha mekanizmasıyla temas ettirerek proteinin parçalanıp temizlenmesini sağlarlar. Bu karşılaştırmayı adil kılmak için bilim insanları önce USP7’ye güçlü biçimde bağlanan ve nadiren diğer proteinlere temas eden yüksek seçiciliğe sahip bir inhibitör; NK192 tasarladılar. Bu iskeletten yola çıkarak hem USP7’yi tanıyabilen hem de VHL adı verilen hücresel imha sistemini devreye sokabilen bir dizi degrader molekülü mühendislik ile geliştirdiler; böylece USP7’yi kanser hücrelerinden etkili biçimde silebildiler.
Farklı kanser hücreleri için özel tasarlanmış çıkarıcılar
Araştırmacılar degrader kitaplığını pankreas ve melanom hücre hatlarında test ettiklerinde, USP7’ye bağlanan kısım ile VHL’yi çağıran kısım arasındaki bağlayıcı şeklinin ve rijitliğinin performansı güçlü şekilde etkilediğini keşfettiler. Birkaç tasarım ve test turunun ardından iki öne çıkan degrader’a ulaştılar: pankreas kanseri hücrelerinde en iyi performansı gösteren NK250 ve melanom hücrelerinde daha etkili olan NK266. Bu moleküller çok düşük dozlarda neredeyse tamamıyla USP7’yi ortadan kaldırabiliyordu ve izleyen deneyler etkinin hedeflenen atık-imhası yoluna bağlı olduğunu doğruladı. Hassas testler, özellikle NK250’nin USP7 ve VHL ile kararlı bir üçlü kompleks oluşturduğunu göstererek hızlı etkisini açıkladı.
Hücre içindeki değişikliklere yakından bakmak
USP7 engellendiğinde veya yok edildiğinde hücrenin geri kalanında neler olduğunu görmek için bilim insanları gelişmiş kütle spektrometrisi kullanarak tedavi edilen kanser hücrelerinde binlerce proteini ölçtüler. Degrader’lar şaşırtıcı derecede odaklanmış bir yanıt üretti: USP7 ortadan kalktı ve özellikle Polycomb adı verilen gen susturma makinesinin bileşenleri olmak üzere sınırlı sayıda bilinen ortak protein her iki kanser türünde azaldı. Bu değişiklikler normalde susturulan belirli genlerin frenlerini gevşetti ve USP7’nin belirli gen susturma programlarını desteklediğini doğruladı. Önemli olarak, daha önce öne sürülen pek çok USP7 ortağı bu katı kanser hücrelerinde değişmedi; bu da USP7’nin rolünün hücre türleri arasında büyük farklılıklar gösterdiğini vurguluyor. 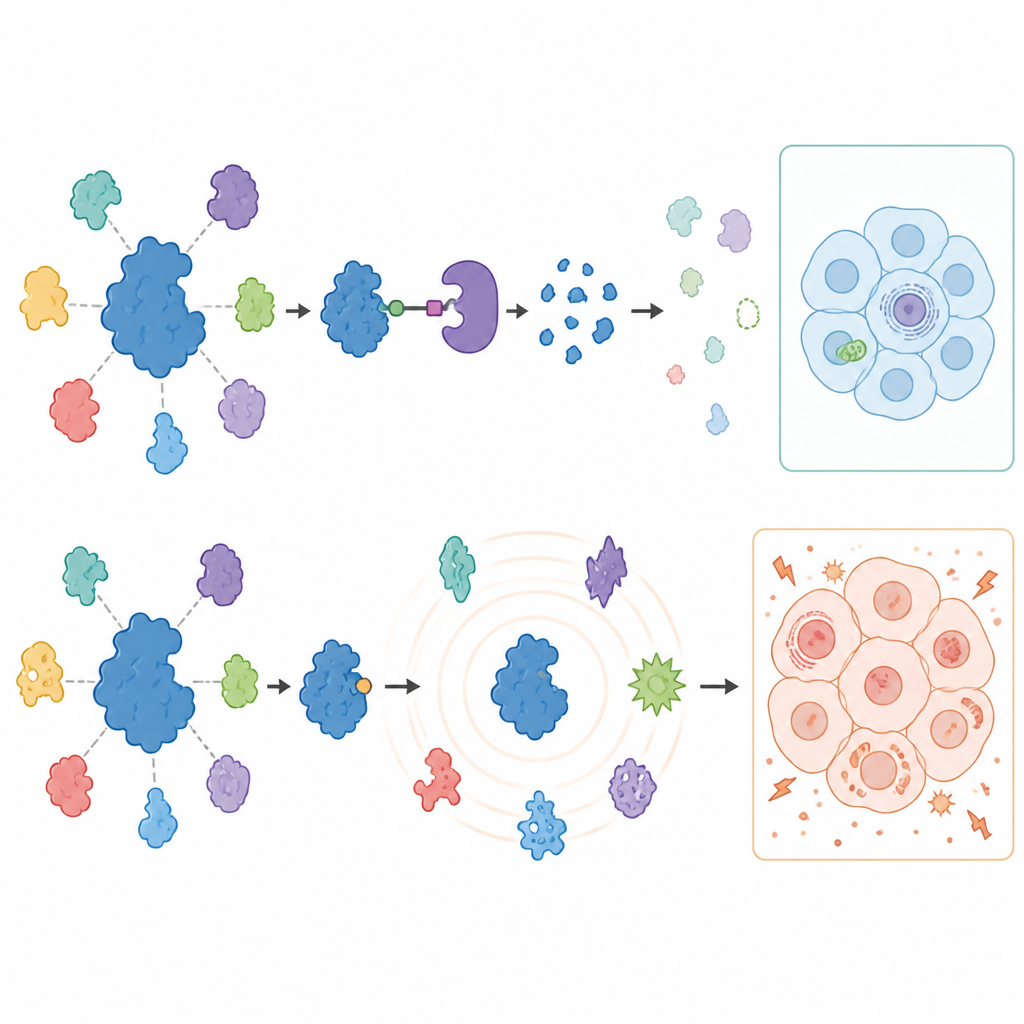
Engellemenin hedefin çok ötesine geçtiği durumlar
İnhibitörler daha uzun süreli uygulamalarda çok farklı bir tablo çizdi. İlk gün boyunca protein değişiklikleri paterni büyük ölçüde degrader’larda görülenleri yansıtıyordu ve bu gerçek USP7 işlevlerine işaret ediyordu. Ancak üç gün süren tedaviden sonra inhibitörler geniş ve bazen garip protein kaymaları dalgası tetikledi; bu durum bu kanserlerde genellikle bulunmayan yeni proteinlerin ortaya çıkmasını da içeriyordu. Hücreler ayrıca şeker kullanımına yoğun şekilde bağımlı hale geldi, mitokondrilerinde enerji üretme yetileri azaldı ve glukoz kısıtlandığında hücre ölümü eğilimi gösterdiler. Kritik olarak, bu metabolik bozukluklar gene düzenleme ile USP7’nin yok edildiği melanom hücrelerinde bile ortaya çıktı; bu da değişikliklerin USP7’den bağımsız, inhibitörlerin hedef dışı etkilerinden kaynaklandığını kanıtladı.
Gelecekteki kanser ilaçları için anlamı
Bu çalışma, dikkatle dizayn edilen degrader’ların USP7’yi yüksek hassasiyetle ortadan kaldırabileceğini ve katı kanserlerde gen kontrolü üzerinde gerçek, odaklanmış bir dizi aşağı akış etkisini ortaya koyduğunu gösteriyor. Buna karşılık, erken testlerde temiz görünen iyi karakterize inhibitörler bile daha uzun süre kullanıldıklarında yaygın ve USP7’e bağlı olmayan değişiklikler tetikleyebiliyor. Bilim insanları ve ilaç geliştiriciler için mesaj açık: degrader’lar tek bir proteinin farklı kanserlerde gerçekten ne yaptığını temiz biçimde çözümlemek için güçlü araçlardır; inhibitörler ise aktivitenin kısa süreli testleri için daha uygundur. Birlikte, bu tamamlayıcı araçlar USP7 ve ilişkili proteinleri kanser tedavisinde anlamak ve nihayetinde yararlanmak için daha net bir yol açıyor.
Atıf: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Anahtar kelimeler: USP7, PROTAC degrader, kanser hücreleri, protein inhibisyonu, hücre metabolizması