Clear Sky Science · it
Degradazione mirata di USP7 nelle cellule di tumore solido rivela effetti distinti tra degradatori e inibitori della deubiquitinasi
Perché degradare una proteina conta nel cancro
I trattamenti antitumorali spesso mirano a bloccare l’attività di proteine dannose, ma un’idea emergente è rimuovere quelle proteine dalle cellule del tutto. Questo studio esamina una proteina chiamata USP7, che protegge altre proteine dalla degradazione naturale, e pone una domanda semplice ma dalle grandi conseguenze: è meglio disattivare temporaneamente USP7 o eliminarla completamente? Confrontando queste due strategie in cellule di tumori solidi provenienti da cancro del pancreas e melanoma, i ricercatori scoprono differenze importanti per la progettazione di farmaci più sicuri e più precisi. 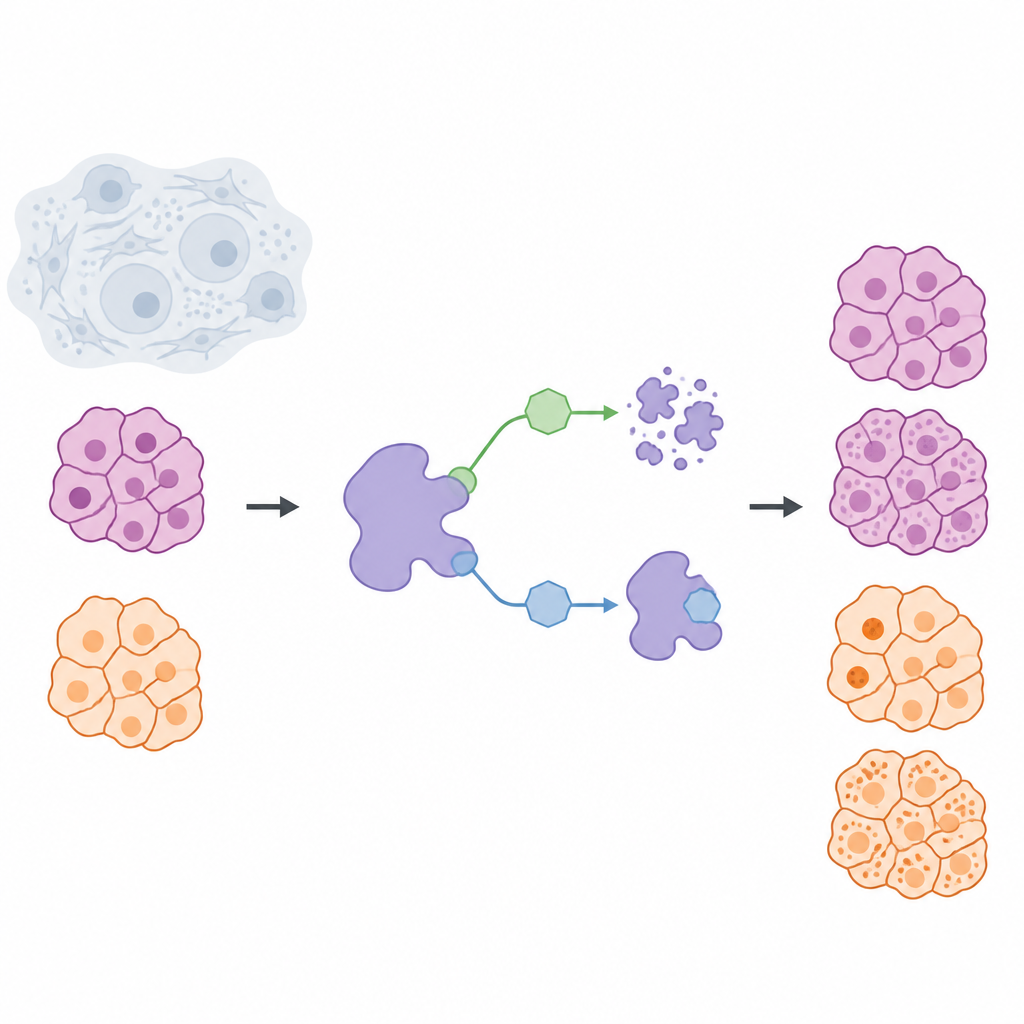
Due strumenti diversi per controllare lo stesso bersaglio
Il gruppo ha costruito una cassetta di strumenti chimica per modulare USP7 nelle cellule vive in due modi distinti. Un insieme di molecole, chiamate inibitori, si lega a USP7 e ne blocca l’attività, lasciando però la proteina al suo posto. Il secondo insieme, chiamato degradatori, agisce come tag di rimozione guidata: avvicina USP7 alla macchina di smaltimento cellulare in modo che la proteina venga degradata ed eliminata. Per rendere il confronto equo, gli scienziati hanno prima progettato un inibitore altamente selettivo, NK192, che si lega saldamente a USP7 e tocca raramente altre proteine. A partire da questo scaffold hanno poi sviluppato una serie di degradatori in grado sia di riconoscere USP7 sia di reclutare un sistema di smaltimento cellulare noto come VHL, permettendo di rimuovere USP7 dalle cellule tumorali in modo efficiente.
Rimuoventi su misura per diversi tipi di cancro
Quando i ricercatori hanno testato la libreria di degradatori in linee cellulari di pancreas e melanoma, hanno scoperto che la forma e la rigidità del linker tra la parte che lega USP7 e quella che recluta VHL influenzavano fortemente le prestazioni. Dopo diversi cicli di progettazione e test, sono emersi due degradatori di punta: NK250, più efficace nelle cellule del cancro pancreatico, e NK266, più attivo nelle cellule di melanoma. Queste molecole sono state in grado di rimuovere quasi completamente USP7 a dosi molto basse, e esperimenti di follow-up hanno confermato che l’effetto dipendeva dalla via di smaltimento prevista. Con saggi sensibili, il team ha dimostrato che NK250 in particolare forma un complesso stabile a tre componenti con USP7 e VHL, spiegando la sua azione rapida.
Un dettaglio su cosa cambia dentro la cellula
Per vedere cosa succede al resto della cellula quando USP7 viene bloccata o rimossa, gli scienziati hanno misurato migliaia di proteine nelle cellule tumorali trattate utilizzando spettrometria di massa avanzata. I degradatori hanno prodotto una risposta sorprendentemente mirata: USP7 scompariva e un insieme limitato di partner noti, in particolare componenti di una macchina di silenziamento genico chiamata complesso Polycomb, diminuiva in entrambi i tipi di cancro. Questi cambiamenti hanno allentato i freni su alcuni geni normalmente tenuti silenziosi, confermando che USP7 sostiene specifici programmi di repressione genica. Importante, molti partner di USP7 precedentemente suggeriti non cambiavano in queste cellule di tumori solidi, sottolineando che il ruolo di USP7 varia fortemente tra tipi cellulari. 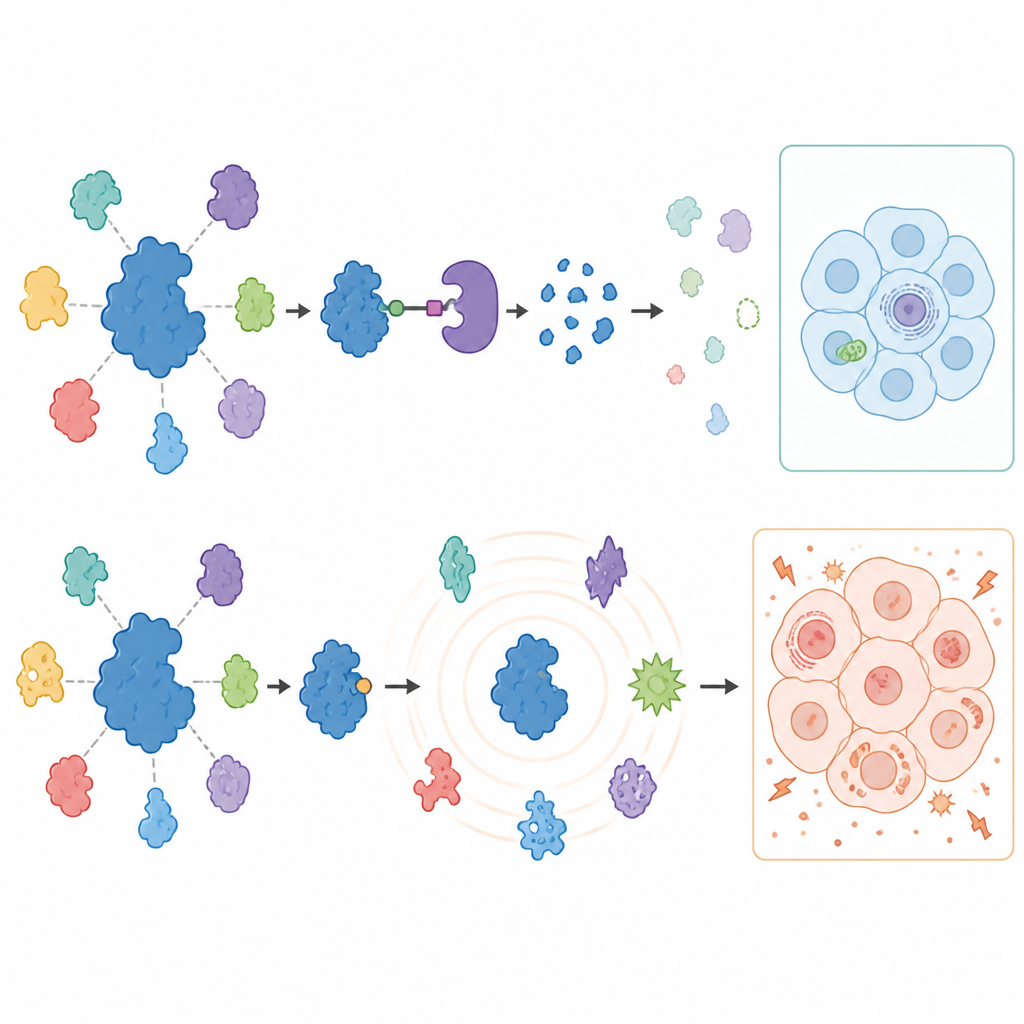
Quando il blocco va oltre il bersaglio
Gli inibitori raccontano una storia molto diversa sui tempi lunghi. Per la prima giornata, il modello di cambiamenti proteici rispecchiava in gran parte ciò che si vedeva con i degradatori, indicando funzioni genuine di USP7. Ma dopo tre giorni di trattamento, gli inibitori provocarono un’ondata di ampie e talvolta insolite variazioni proteiche, inclusa la comparsa di proteine non tipicamente presenti in questi tumori. Le cellule iniziarono inoltre a dipendere pesantemente dallo zucchero, mostrarono ridotta capacità di generare energia nei mitocondri e divennero più suscettibili alla morte cellulare quando il glucosio era limitato. Crucialmente, queste perturbazioni metaboliche si verificarono anche in cellule di melanoma in cui USP7 era stata rimossa mediante editing genetico, dimostrando che erano causate da azioni off-target degli inibitori e non da USP7 stessa.
Cosa significa per i futuri farmaci antitumorali
Questo lavoro mostra che degradatori accuratamente progettati possono rimuovere USP7 con elevata precisione, rivelando un insieme mirato di veri effetti a valle sul controllo genico nei tumori solidi. Al contrario, anche inibitori ben caratterizzati che appaiono puliti nei test iniziali possono scatenare cambiamenti diffusi e indipendenti da USP7 se usati per periodi prolungati. Per scienziati e sviluppatori di farmaci, il messaggio è chiaro: i degradatori sono strumenti potenti per analizzare in modo pulito cosa fa realmente una singola proteina in diversi tumori, mentre gli inibitori sono più adatti per test di attività a breve termine. Insieme, questi strumenti complementari aprono una via più chiara per comprendere e infine sfruttare USP7 e proteine correlate nella terapia oncologica.
Citazione: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Parole chiave: USP7, PROTAC degrader, cellule tumorali, inibizione proteica, metabolismo cellulare