Clear Sky Science · ja
固形がん細胞におけるUSP7の標的分解は脱ユビキチン化酵素のデグレーダーと阻害剤で異なる影響を明らかにする
なぜ一つのタンパク質を分解することが重要なのか
がん治療はしばしば有害なタンパク質の活性を阻害することを目指しますが、近年の考え方の一つにそのタンパク質自体を細胞から取り除くという選択肢があります。本研究は、他のタンパク質の自然な分解を防ぐ働きを持つUSP7というタンパク質に注目し、単純だが重大な問いを投げかけます:USP7を一時的にオフにするのと、完全に除去するのとではどちらが良いのか?膵臓がんおよびメラノーマ由来の固形腫瘍細胞でこの二つの戦略を比較することで、より安全で精密な薬剤設計に重要な違いが明らかになりました。 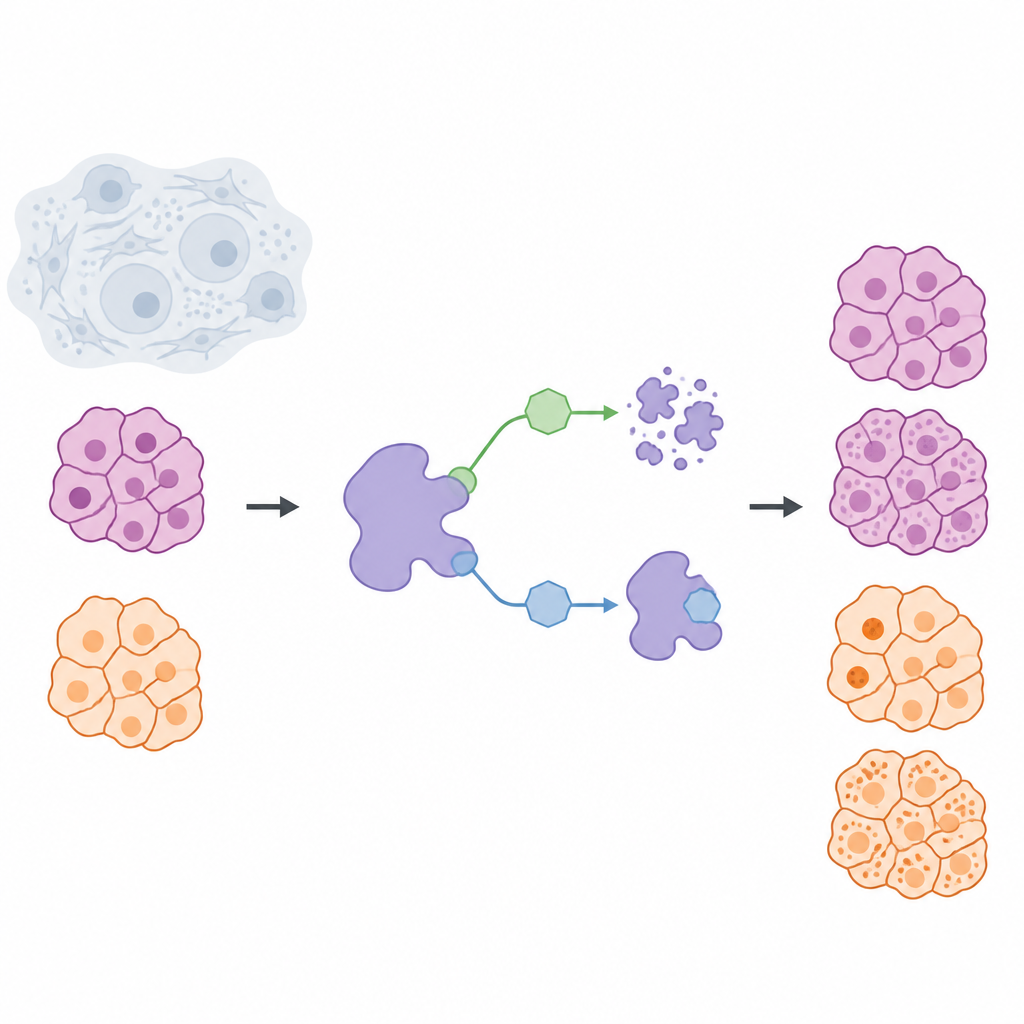
同じ標的を制御する二つの異なる道具
研究チームは、生細胞内でUSP7を二通りの方法で制御するための化学ツールボックスを構築しました。一方は阻害剤と呼ばれる分子群で、USP7に結合してその活性を止めますが、タンパク質自体は細胞内に残ります。もう一方はデグレーダーと呼ばれる分子で、標的除去タグのように働き、USP7を細胞の廃棄機構に引き合わせて分解・除去させます。この比較を公平にするため、研究者らはまず高選択的な阻害剤NK192を設計し、USP7に強く結合し他のタンパク質にはほとんど作用しないことを確認しました。その骨格を基にして、USP7を認識すると同時にVHLとして知られる細胞の廃棄システムを呼び寄せられる一連のデグレーダー分子を設計し、がん細胞から効率的にUSP7を除去できるようにしました。
異なるがん細胞向けに作られた専用の除去剤
デグレーダーライブラリを膵臓とメラノーマの細胞株で評価したところ、USP7結合部位とVHLリクルート部位の間のリンカーの形状や剛性が性能に大きく影響することがわかりました。設計と試験を何度か繰り返した結果、膵臓がん細胞で最も有効なNK250と、メラノーマ細胞でより効果を示すNK266という2つの優れたデグレーダーが得られました。これらは非常に低用量でほぼ完全にUSP7を除去でき、追試実験はその効果が意図した廃棄経路に依存することを確認しました。感度の高いアッセイでは、特にNK250がUSP7とVHLの三者複合体を安定に形成し、それが迅速な作用を説明していることが示されました。
細胞内で何が変わるかを拡大して見る
USP7を阻害したり除去したりしたときに細胞内で他に何が起きるかを調べるため、研究者らは高度な質量分析を用いて処理したがん細胞中の何千ものタンパク質を測定しました。デグレーダーは驚くほど焦点の絞られた反応を引き起こしました:USP7は消失し、既知の限られた相互作用相手、特にPolycombと呼ばれる遺伝子サイレンシング機構の構成要素が両がん種で減少しました。これらの変化は通常抑えられているいくつかの遺伝子のブレーキを緩め、USP7が特定の遺伝子サイレンシングプログラムを支持していることを裏付けます。重要なのは、以前にUSP7の相互作用相手とされていた多くがこれらの固形がん細胞では変化しなかったことで、USP7の役割が細胞種間で大きく異なることが強調されました。 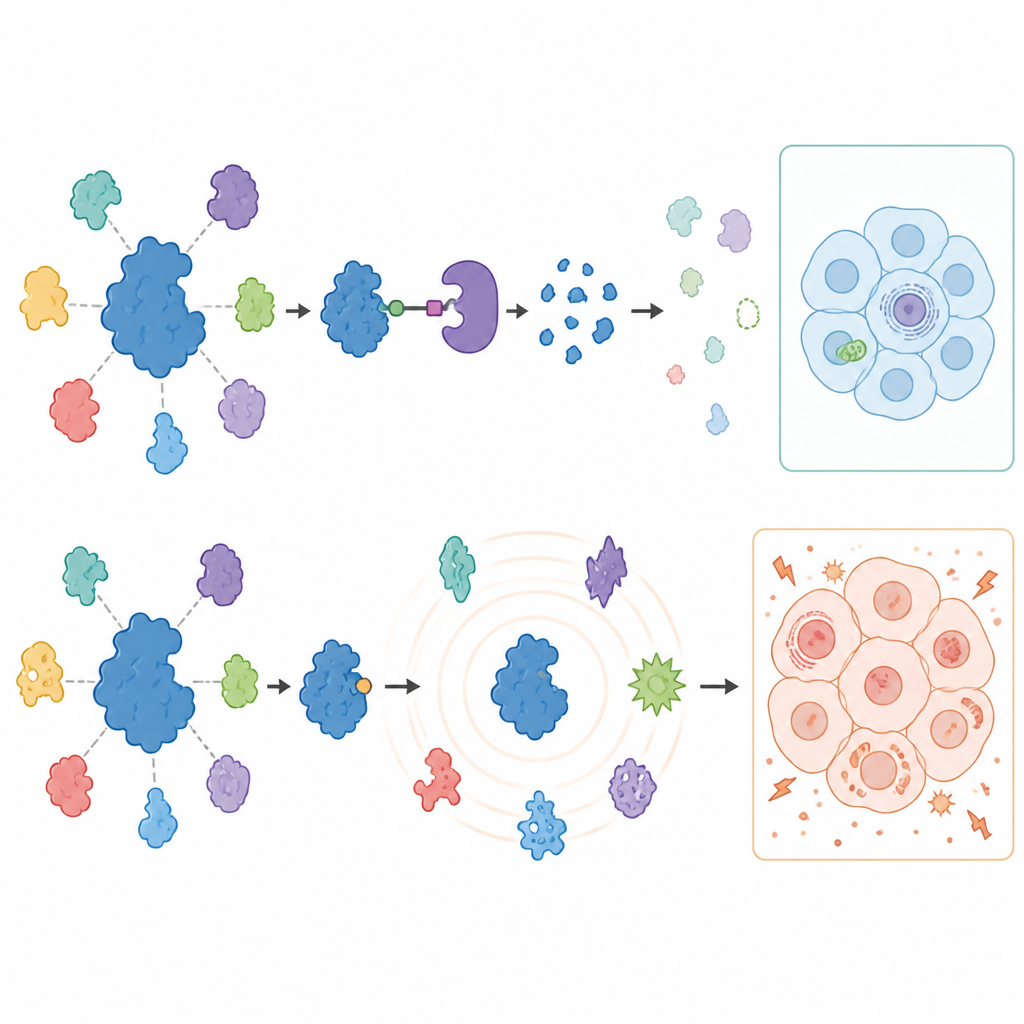
阻害がターゲットを超えて広がるとき
阻害剤は長期的には全く異なる様相を示しました。初日の変化パターンは主にデグレーダーで見られたものと一致し、真のUSP7機能を反映していることが示されました。しかし3日間の処理後には、阻害剤は広範で時に奇妙なタンパク質変動の波を引き起こし、これまでにそのがんで通常見られないタンパク質が出現することもありました。細胞は糖に大きく依存するようになり、ミトコンドリアでのエネルギー産生能力が低下し、グルコースが制限されると細胞死に陥りやすくなりました。重要な点は、これらの代謝異常は遺伝子編集でUSP7が除去されたメラノーマ細胞でも依然として起きたため、これらはUSP7自体ではなく阻害剤のオフターゲット作用によって引き起こされていることが証明されたことです。
今後のがん薬にとっての意味
本研究は、慎重に設計されたデグレーダーが高い精度でUSP7を除去でき、固形がんにおける遺伝子制御に関する真の下流効果の焦点化されたセットを明らかにすることを示しています。対照的に、初期試験ではクリーンに見えるよく特徴付けられた阻害剤でも、長期使用では広範でUSP7に依存しない変化を引き起こし得ます。科学者や薬剤開発者へのメッセージは明快です:デグレーダーは単一タンパク質が異なるがんで実際に何をするかを明確に解析する強力なツールであり、阻害剤は活性の短期評価に適しています。これら二つの補完的な道具は、USP7や関連タンパク質をがん治療で理解し活用するためのより明瞭な道筋を開きます。
引用: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
キーワード: USP7, PROTACデグレーダー, がん細胞, タンパク質阻害, 細胞代謝