Clear Sky Science · ru
Целенаправленное разрушение USP7 в клетках солидных опухолей выявляет разные эффекты деградеров and ингибиторов дебубиквитиназ
Почему разрушение одного белка имеет значение для борьбы с раком
В терапии рака часто стремятся блокировать активность вредных белков, но появилась идея: полностью удалить эти белки из клетки. В этом исследовании рассматривается белок USP7, который помогает другим белкам избегать естественного разрушения, и задаётся простой, но важный вопрос: что лучше — временно отключить USP7 или избавиться от него насовсем? Сравнивая эти две стратегии в клетках солидных опухолей поджелудочной железы и меланомы, авторы выявляют существенные различия, важные для разработки более безопасных и точных лекарств. 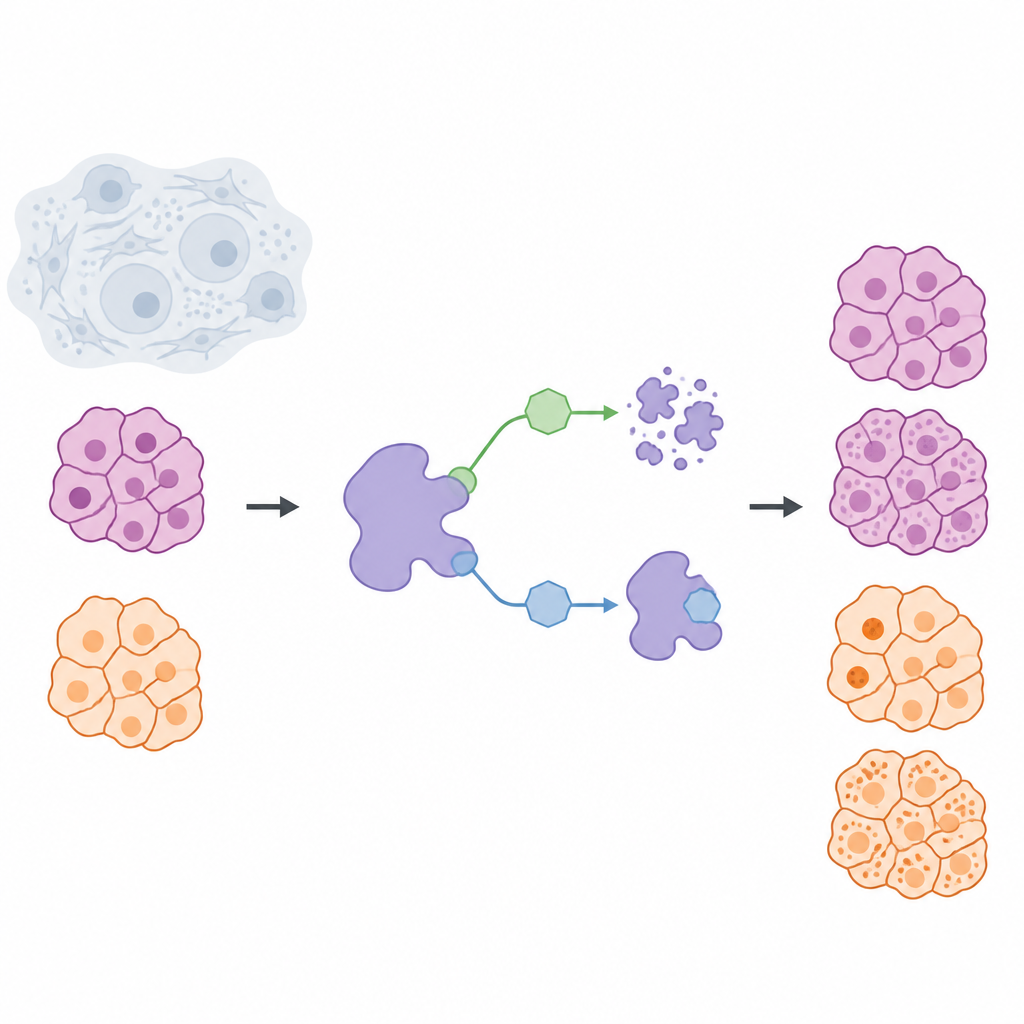
Два разных инструмента воздействия на одну цель
Команда создала химическую «панель» для управления USP7 в живых клетках двумя разными способами. Один класс молекул, называемых ингибиторами, связывается с USP7 и останавливает его активность, при этом сам белок остаётся в клетке. Второй класс, деградеры, действует как метки для удаления: они сводят USP7 с клеточным «мусороперерабатывающим» механизмом, в результате чего белок расщепляется и утилизируется. Чтобы сравнение было честным, учёные сначала разработали высокоселективный ингибитор NK192, который сильно связывается с USP7 и редко затрагивает другие белки. На основе этой структуры они затем сконструировали серию деградирующих молекул, которые одновременно распознают USP7 и привлекают систему утилизации VHL, что позволяет эффективно выводить USP7 из раковых клеток.
Индивидуально подобранные средства удаления для разных типов рака
При испытаниях библиотеки деградёров в клеточных линиях поджелудочной железы и меланомы исследователи обнаружили, что форма и жёсткость линкера между частью, связывающей USP7, и частью, привлекающей VHL, существенно влияют на эффективность. После нескольких раундов проектирования и тестирования они выделили два выдающихся деградерa: NK250, который лучше работает в клетках поджелудочной железы, и NK266, более эффективный в клетках меланомы. Эти молекулы могли почти полностью удалить USP7 при очень низких дозах, а последующие эксперименты подтвердили, что эффект зависит от задуманного пути утилизации. Чувствительные тесты показали, что NK250 в частности образует стабильный трёхкомпонентный комплекс с USP7 и VHL, что объясняет его быструю активность.
Что меняется внутри клетки
Чтобы понять, что происходит с остальной частью клетки при блокировании или удалении USP7, учёные измеряли тысячи белков в обработанных раковых клетках с помощью продвинутой масс‑спектрометрии. Деградёры вызвали удивительно сфокусированный ответ: USP7 исчезал, а ограниченный набор известных партнёров, особенно компоненты машины генного заглушения, называемой комплексом Polycomb, снижался в обоих типах рака. Эти изменения ослабляли торможение определённых генов, которые обычно молчат, подтверждая, что USP7 поддерживает специфические программы генного подавления. Важно, что многие ранее предложенные партнёры USP7 не изменялись в этих клетках солидных опухолей, что подчёркивает сильную вариативность роли USP7 в разных типах клеток. 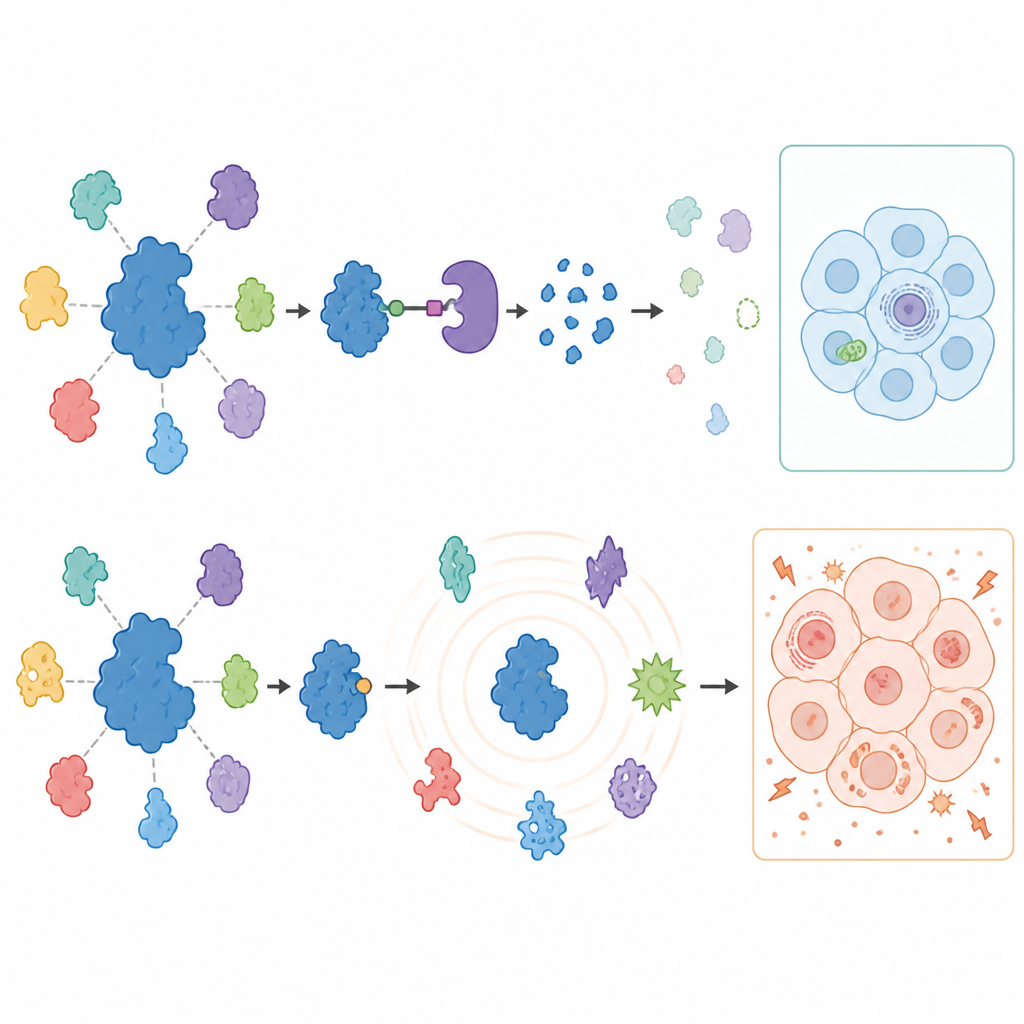
Когда блокирование выходит далеко за пределы цели
Ингибиторы рассказали совершенно иную историю при длительном применении. В первые сутки картина изменений белков в целом отражала эффект деградёров, указывая на подлинные функции USP7. Но через три дня лечения ингибиторы вызвали волну широких и иногда странных сдвигов в протеоме, включая появление белков, обычно не встречающихся в этих типах рака. Клетки также стали сильнее зависеть от сахара, показали сниженный потенциал генерации энергии в митохондриях и приобрели склонность к гибели при ограничении глюкозы. Критично, эти метаболические нарушения сохранялись в клетках меланомы, где USP7 был удалён с помощью редактирования генома, что доказывает: нарушения вызваны офф‑таргетными действиями ингибиторов, а не отсутствием USP7.
Что это значит для будущих противораковых препаратов
Эта работа показывает, что тщательно сконструированные деградёры могут с высокой точностью удалять USP7, выявляя сфокусированный набор истинных последующих эффектов на контроль генов в солидных опухолях. Напротив, даже хорошо охарактеризованные ингибиторы, кажущиеся «чистыми» в ранних тестах, при длительном применении могут вызывать широкие изменения, не связанные с USP7. Для учёных и разработчиков лекарств послание ясно: деградёры — мощный инструмент для чистого выяснения функций отдельного белка в разных раках, тогда как ингибиторы полезны для кратковременных проверок активности. В совокупности эти дополняющие друг друга инструменты открывают более ясный путь к пониманию и, в перспективе, использованию USP7 и родственных белков в терапии рака.
Цитирование: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Ключевые слова: USP7, PROTAC деградер, раковые клетки, ингибиция белков, клеточный метаболизм