Clear Sky Science · fr
La dégradation ciblée de USP7 dans des cellules de cancers solides révèle des effets distincts des dégradeurs et des inhibiteurs de déubiquitinase
Pourquoi la dégradation d’une seule protéine compte en cancérologie
Les traitements contre le cancer visent souvent à bloquer l’activité de protéines nuisibles, mais une idée émergente consiste à éliminer ces protéines des cellules entièrement. Cette étude porte sur une protéine nommée USP7, qui protège d’autres protéines de la dégradation naturelle, et pose une question simple aux conséquences majeures : vaut‑il mieux désactiver USP7 temporairement ou l’éliminer complètement ? En comparant ces deux stratégies dans des tumeurs solides issues de cancers du pancréas et du mélanome, les chercheurs mettent au jour des différences importantes pour la conception de médicaments plus sûrs et plus précis. 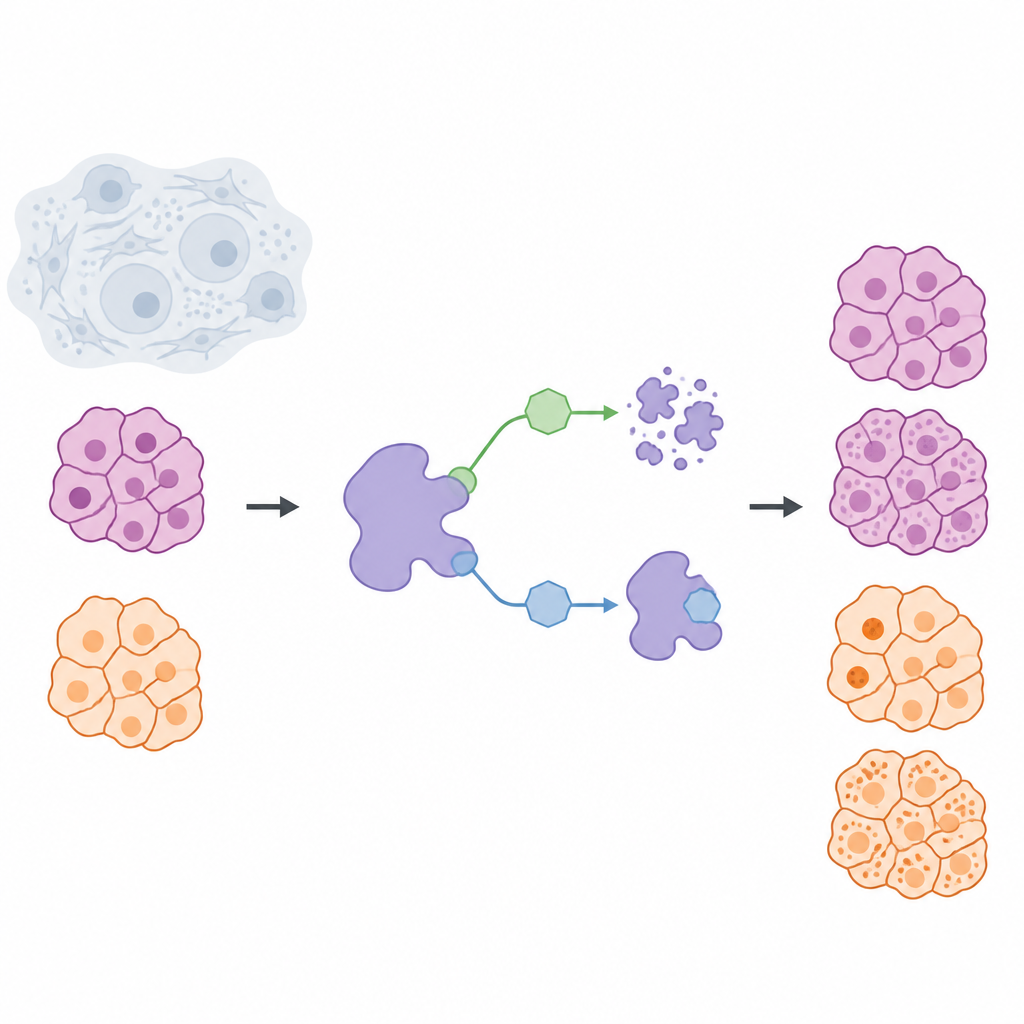
Deux outils différents pour cibler la même protéine
L’équipe a construit une boîte à outils chimique pour contrôler USP7 dans des cellules vivantes de deux manières distinctes. Un ensemble de molécules, appelées inhibiteurs, se lient à USP7 et bloquent son activité tout en laissant la protéine en place. Le second ensemble, appelé dégradeurs, agit plutôt comme des étiquettes de retrait guidées : ils rapprochent USP7 de la machinerie d’élimination cellulaire afin que la protéine soit dégradée et éliminée. Pour rendre la comparaison équitable, les scientifiques ont d’abord conçu un inhibiteur hautement sélectif, NK192, qui se lie fortement à USP7 et touche rarement d’autres protéines. À partir de ce noyau, ils ont ensuite élaboré une série de dégradeurs capables à la fois de reconnaître USP7 et de recruter un système d’élimination cellulaire connu sous le nom de VHL, leur permettant d’éliminer USP7 efficacement des cellules cancéreuses.
Des agents sur mesure pour différents types de cancer
En testant leur bibliothèque de dégradeurs dans des lignées cellulaires pancréatiques et mélanomes, les chercheurs ont découvert que la forme et la rigidité du lien entre la partie qui se lie à USP7 et celle qui recrute VHL influençaient fortement la performance. Après plusieurs cycles de conception et d’essais, ils sont parvenus à deux dégradeurs remarquables : NK250, qui fonctionne le mieux dans les cellules de cancer du pancréas, et NK266, plus efficace dans les cellules de mélanome. Ces molécules pouvaient quasiment éliminer USP7 à très faibles doses, et des expériences complémentaires ont confirmé que l’effet dépendait de la voie d’élimination visée. Grâce à des tests sensibles, l’équipe a montré que NK250 forme en particulier un complexe stable à trois composants avec USP7 et VHL, ce qui explique son action rapide.
Regarder de près ce qui change à l’intérieur de la cellule
Pour observer les conséquences du blocage ou de la suppression de USP7 sur le reste de la cellule, les scientifiques ont mesuré des milliers de protéines dans des cellules cancéreuses traitées par spectrométrie de masse avancée. Les dégradeurs ont produit une réponse étonnamment ciblée : USP7 a disparu, et un ensemble limité de partenaires connus, en particulier des composants d’une machine de répression génique appelée complexe Polycomb, a diminué dans les deux types de cancer. Ces changements ont levé les freins sur certains gènes normalement silencieux, confirmant que USP7 soutient des programmes spécifiques de répression génique. Fait important, de nombreux partenaires de USP7 suggérés précédemment n’ont pas changé dans ces cancers solides, soulignant que le rôle de USP7 varie fortement selon le type cellulaire. 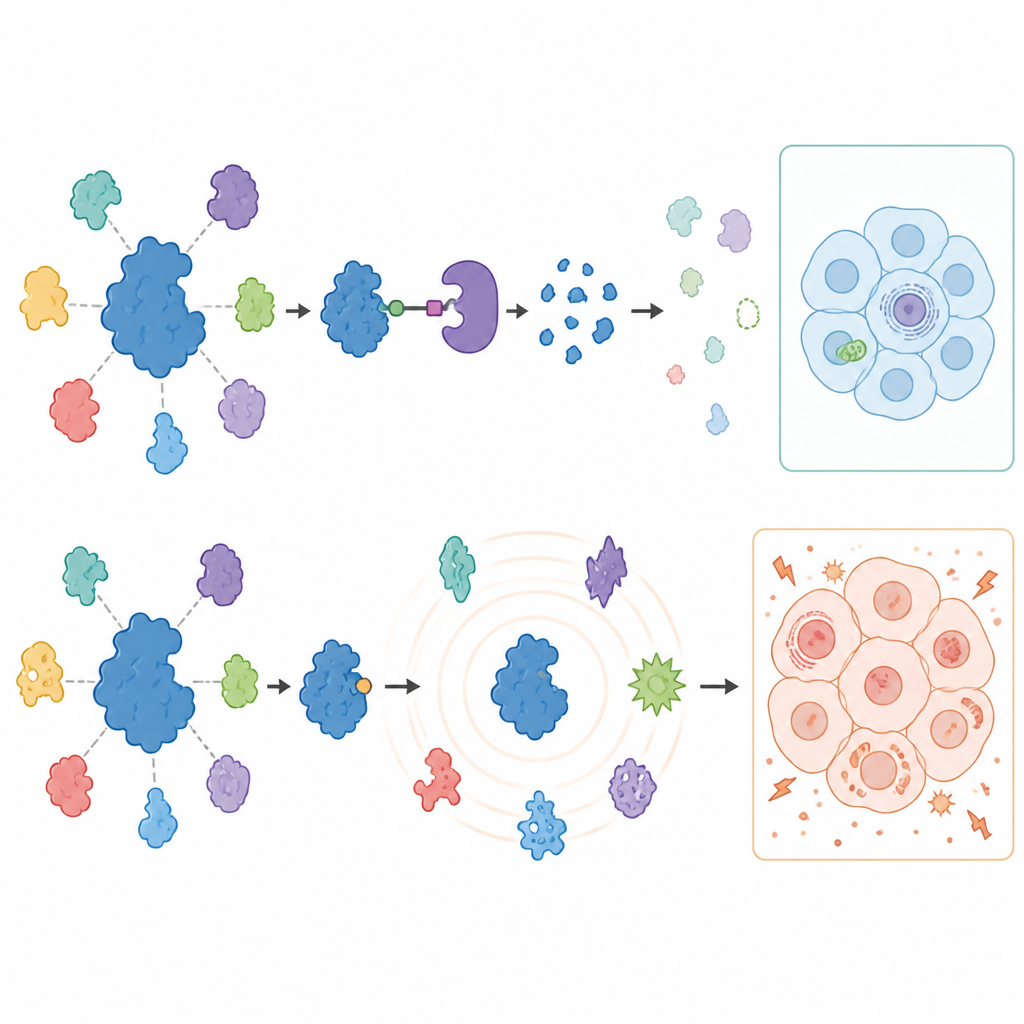
Quand le blocage dépasse trop la cible
Les inhibiteurs racontent une histoire très différente sur le long terme. Durant la première journée, le profil de changements protéiques reflétait largement ce qui avait été observé avec les dégradeurs, pointant vers des fonctions authentiques de USP7. Mais après trois jours de traitement, les inhibiteurs ont déclenché une vague de modifications protéiques larges et parfois inattendues, incluant l’apparition de protéines habituellement absentes de ces cancers. Les cellules sont aussi devenues fortement dépendantes du sucre, ont montré une capacité réduite à produire de l’énergie dans leurs mitochondries et se sont montrées plus susceptibles de mourir quand le glucose venait à manquer. Crucialement, ces perturbations métaboliques ont également été observées dans des cellules de mélanome où USP7 avait été supprimé par édition génique, prouvant qu’elles étaient causées par des actions hors cible des inhibiteurs et non par l’absence de USP7.
Implications pour les médicaments anticancéreux futurs
Ce travail montre que des dégradeurs soigneusement conçus peuvent éliminer USP7 avec une grande précision, révélant un ensemble ciblé d’effets en aval réels sur le contrôle génique dans les cancers solides. En revanche, même des inhibiteurs bien caractérisés et propres en tests précoces peuvent déclencher des changements étendus, indépendants de USP7, lorsqu’ils sont utilisés sur des périodes plus longues. Pour les scientifiques et les développeurs de médicaments, le message est clair : les dégradeurs sont des outils puissants pour disséquer proprement la fonction d’une protéine unique dans différents cancers, tandis que les inhibiteurs restent utiles pour des évaluations d’activité à court terme. Ensemble, ces outils complémentaires ouvrent une voie plus nette pour comprendre et, à terme, exploiter USP7 et des protéines apparentées en thérapie anticancéreuse.
Citation: Klink, N., Urban, S., Seier, J.A. et al. Targeted degradation of USP7 in solid cancer cells reveals distinct effects of deubiquitinase degraders and inhibitors. Nat Commun 17, 4331 (2026). https://doi.org/10.1038/s41467-026-72295-x
Mots-clés: USP7, dégradeur PROTAC, cellules cancéreuses, inhibition de protéine, métabolisme cellulaire