Clear Sky Science · zh
I型干扰素驱动中枢神经系统对淀粉样β的T细胞反应
为何大脑对斑块的免疫反应至关重要
阿尔茨海默病常被描述为大脑中有毒蛋白沉积的问题,但同样重要的是免疫系统如何应对由此产生的损伤。本研究探讨了免疫系统中由I型干扰素信号驱动的特定分支,如何引导T细胞朝向淀粉样β斑块并随时间重塑脑内炎症。理解这一不断变化的免疫“舞台调度”可能有助于解释为何疾病后期脑损伤加速,并为更合时宜的治疗指明方向。
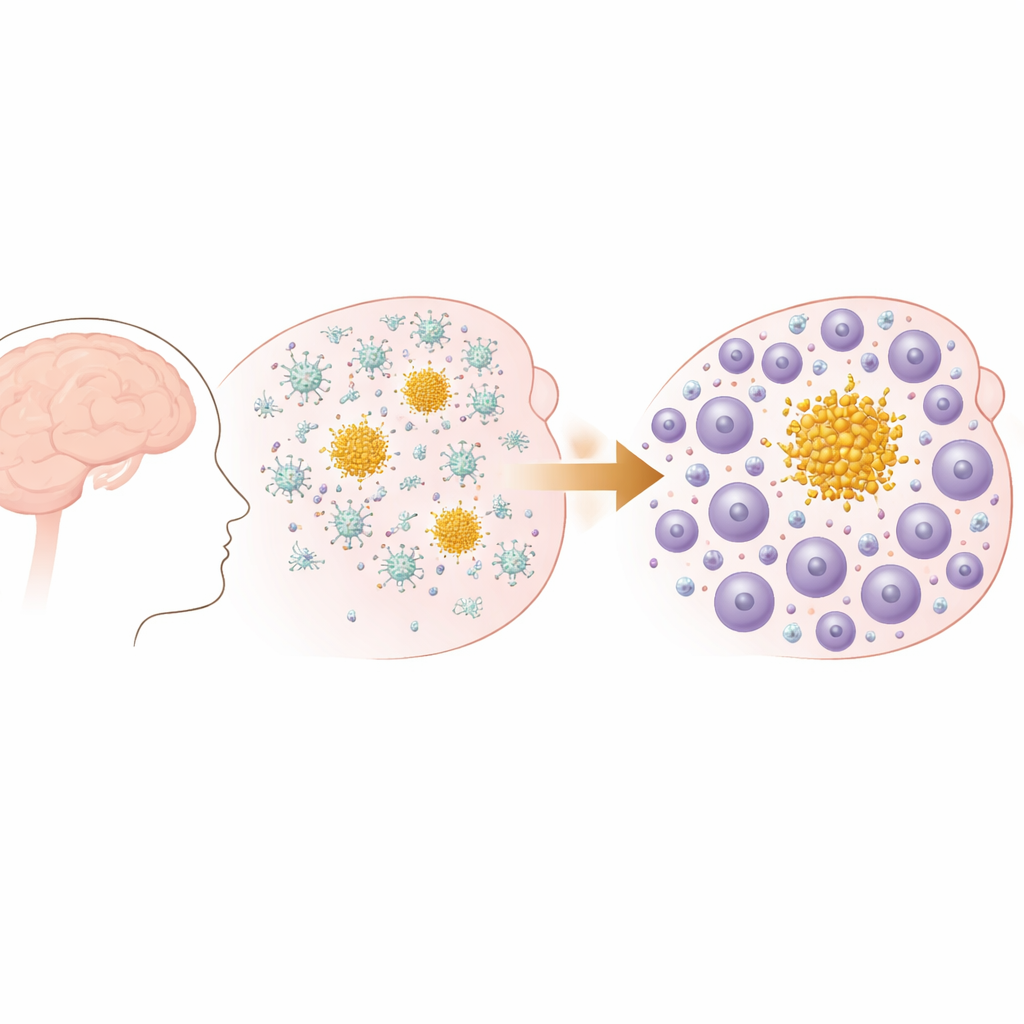
从早期斑块到变化的免疫角色
研究人员使用了一种小鼠模型,该模型在大脑中逐渐形成淀粉样β斑块,类似于阿尔茨海默病和脑淀粉样血管病中观察到的情形。生命早期,这些小鼠在大脑外层形成小沉积,随后斑块扩散并增多,尤其累及与记忆相关的区域。行为学测试证实,随着斑块随年龄累积,小鼠在日常功能(如筑巢)上出现可测量的衰退,类似于人类痴呆的渐进性功能丧失。重要的是,该模型具有淀粉样斑块但无缠结病理,使研究团队能专注于免疫系统如何针对淀粉样蛋白沉积作出反应。
当脑内守护者让位给侵入的步兵
起初,对斑块的免疫反应以小胶质细胞为主,它们是大脑的常驻免疫细胞。通过单细胞RNA测序,作者显示在疾病早期这些小胶质细胞进入特殊的疾病相关状态,并上调与吞噬碎屑和脂质处理相关的基因。但随着疾病进展,免疫格局发生转变。脑内T细胞数量尤其是CD8 T细胞显著增加,与淋巴细胞激活和迁移相关的通路变得更为突出。空间分析证实这并非随机侵入:T细胞在脑组织中紧密聚集于淀粉样斑块周围,尤其是更大的“实质性”斑块而非血管内斑块,并且它们的数量与斑块负担同步增加。
一种召唤增援的特化T细胞亚群
更仔细地观察这些T细胞,研究团队鉴定出一类特殊的CD8 T细胞亚群,它们启动了一整套通常由I型干扰素诱导的基因——I型干扰素是一类抗病毒和自身免疫信号分子。这些“干扰素刺激”T细胞在疾病晚期尤其丰富,并分布于斑块附近。它们产生趋化因子CXCL10,这是一种与其他T细胞表面受体CXCR3结合的小型蛋白信号。空间转录组学显示,干扰素响应基因和CXCL10在斑块邻域显著富集,且产生CXCL10的T细胞处于能够影响周围其他免疫细胞的位置。体外迁移实验确认T细胞会朝CXCL10信号移动,阻断CXCR3则显著降低其趋化能力,这支持了一种模型:斑块相关的、由干扰素驱动的T细胞有助于吸引更多T细胞进入大脑。
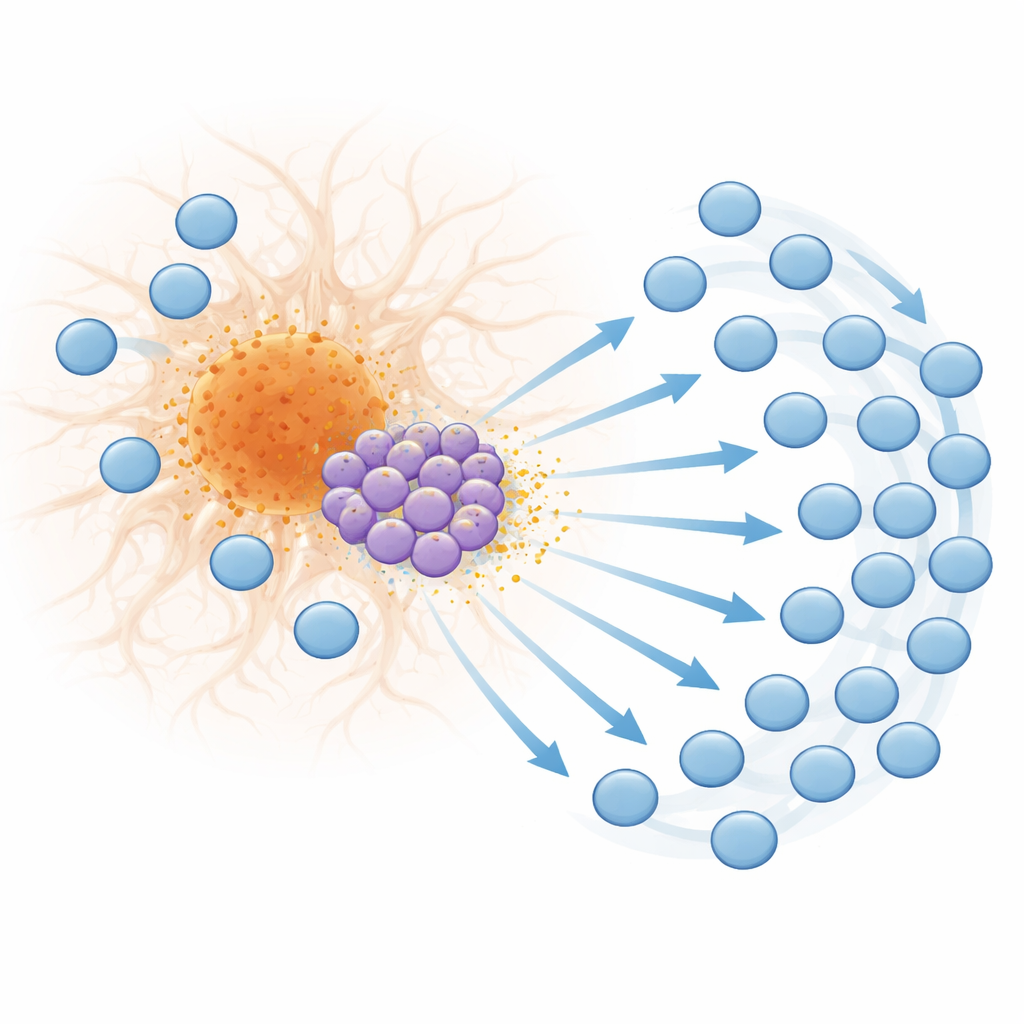
从活化到在斑块边缘的耗竭
T细胞的涌入不仅体现在数量上,质量也发生变化。在疾病晚期,许多斑块周围的CD8 T细胞显示出高活化、细胞毒潜能和克隆扩增的标记——这些迹象表明它们在反复响应特定刺激。同时,这些细胞开始表现出耗竭的特征,即长期刺激下T细胞效能下降并表达抑制性分子如PD-1。空间定位显示,这些耗竭的T细胞直接积聚在斑块边缘,提示由斑块相关信号引发的强烈、持续刺激将它们推向衰竭状态。在人类阿尔茨海默病大脑组织的斑块附近也发现了类似的干扰素响应基因、CXCL10、T细胞活化标记和PD-1的模式,表明这一来源于小鼠的机制很可能对人类具有相关性。
这对未来阿尔茨海默病治疗意味着什么
总体而言,该研究描绘了一幅淀粉样疾病中脑内炎症的时序图:早期以小胶质细胞主导反应,但随着斑块增长和持续存在,一种特化的CD8 T细胞亚群成为I型干扰素信号传导和T细胞募集的主要驱动者。这种演变中的免疫反应可能促成持续的神经元损伤,并可能与去除斑块的抗体疗法相互作用,影响与血管性炎症相关的副作用。对普通读者而言,核心信息是:在阿尔茨海默病中,不仅斑块本身重要,免疫系统如何以及何时对它们作出反应也同样关键。在恰当的疾病阶段针对干扰素通路或CXCL10–CXCR3信号轴,可能有助于抑制有害炎症,同时不完全抑制大脑的防御功能。
引用: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
关键词: 阿尔茨海默病, 淀粉样β, T细胞, 神经炎症, 干扰素信号