Clear Sky Science · es
Interferón tipo I impulsa las respuestas de células T frente a la beta amiloide en el sistema nervioso central
Por qué importa la respuesta inmune del cerebro a las placas
La enfermedad de Alzheimer suele describirse como un problema de acumulación de proteínas tóxicas en el cerebro, pero una parte igualmente importante de la historia es cómo reacciona el sistema inmunitario ante ese daño. Este estudio explora cómo una rama específica del sistema inmune, impulsada por señales de interferón tipo I, guía a las células T hacia las placas de beta amiloide y remodela la inflamación cerebral a lo largo del tiempo. Comprender esta coreografía inmune cambiante puede ayudar a explicar por qué el daño cerebral se acelera en fases más avanzadas de la enfermedad y señalar tratamientos mejor dosificados.
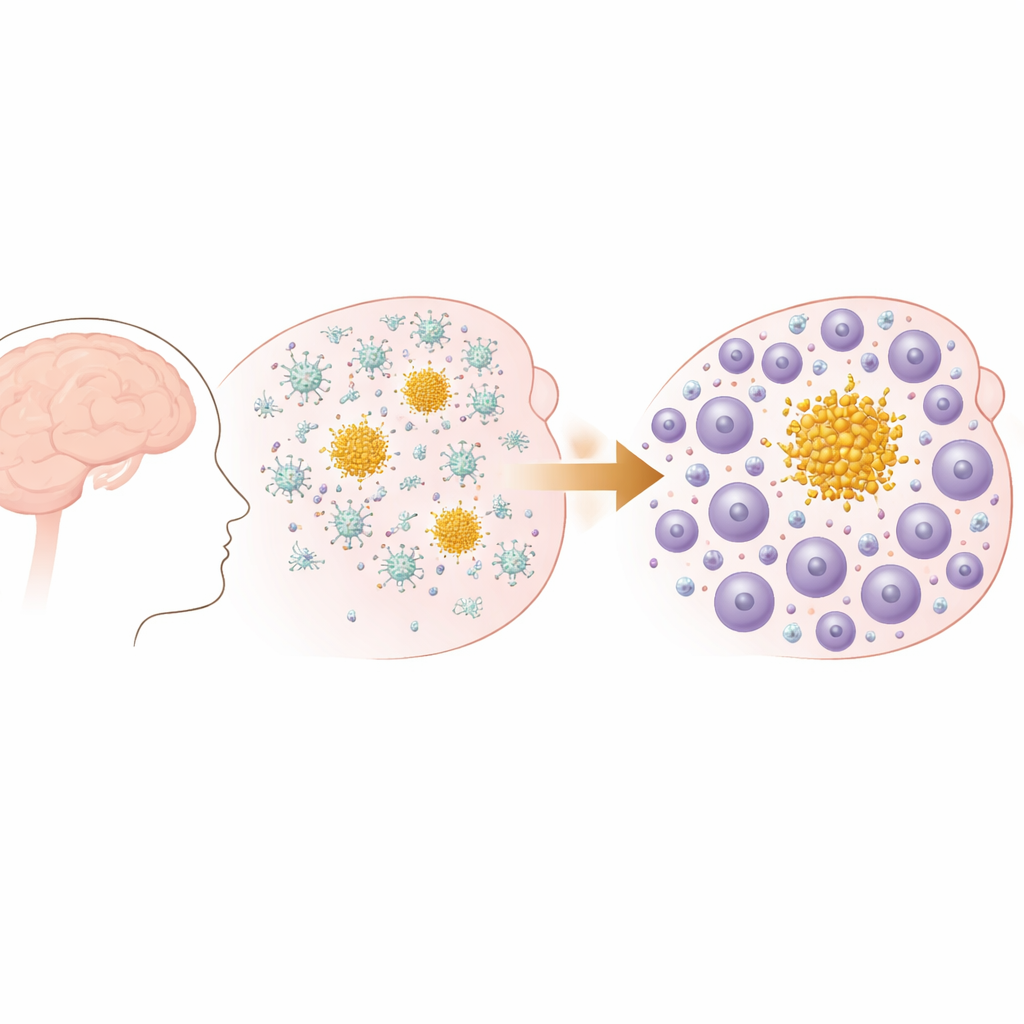
De las placas tempranas a un elenco inmune en transformación
Los investigadores usaron un modelo murino que desarrolla placas progresivas de beta amiloide en el cerebro, similar a las observadas en la enfermedad de Alzheimer y en la angiopatía amiloide cerebral. Al principio de la vida, estos ratones forman pequeños depósitos en las capas externas del cerebro, que más tarde se extienden y aumentan en número, especialmente en regiones relacionadas con la memoria. Pruebas de comportamiento confirmaron que, a medida que las placas se acumulaban con la edad, los ratones mostraban declives medibles en funciones cotidianas como la construcción de nidos, reflejando el tipo de pérdida funcional gradual observada en la demencia humana. Es importante señalar que este modelo presenta placas amiloides pero no patología de ovillos neurofibrilares, lo que permitió al equipo centrarse en cómo responde el sistema inmune específicamente a la acumulación de amiloide.
Cuando los guardianes del cerebro ceden paso a soldados invasores
Al principio, la respuesta inmune a las placas está dominada por las microglías, las células inmunitarias residentes del cerebro. Mediante secuenciación de ARN a célula única, los autores mostraron que en fases tempranas de la enfermedad estas microglías adoptan estados asociados a la enfermedad y aumentan la expresión de genes vinculados a la fagocitosis de restos y al manejo de lípidos. Pero conforme avanza la enfermedad, el panorama inmune cambia. El número de células T en el cerebro, especialmente las CD8, aumenta bruscamente, y las vías relacionadas con la activación y el movimiento de linfocitos se vuelven más prominentes. Análisis espaciales confirmaron que no es una invasión aleatoria: las células T se agrupan en torno a las placas de beta amiloide en el tejido cerebral, en particular alrededor de grandes placas “parenquimatosas” en lugar de las que están en vasos sanguíneos, y su número crece en consonancia con la carga de placas.
Un subconjunto especializado de células T que llama refuerzos
Al examinar más de cerca estas células T, el equipo identificó un subconjunto distinto de CD8 que activa un conjunto de genes normalmente inducidos por interferones tipo I, una familia de moléculas de señalización antiviral y autoinmune. Estas células T “estimuladas por interferón” se vuelven especialmente abundantes en fases tardías de la enfermedad y se localizan junto a las placas. Producen la quimiocina CXCL10, una pequeña proteína señal que se une al receptor CXCR3 en otras células T. La transcriptómica espacial mostró que tanto los genes sensibles al interferón como CXCL10 están fuertemente enriquecidos en los vecindarios de las placas, y que las células T productoras de CXCL10 están posicionadas para influir en otras células inmunes próximas. Experimentos de migración en laboratorio confirmaron que las células T se desplazan hacia señales de CXCL10 y que desactivar CXCR3 reduce drásticamente su capacidad de seguir estas señales, apoyando un modelo en el que las células T asociadas a placas y mediadas por interferón ayudan a atraer más células T al cerebro.
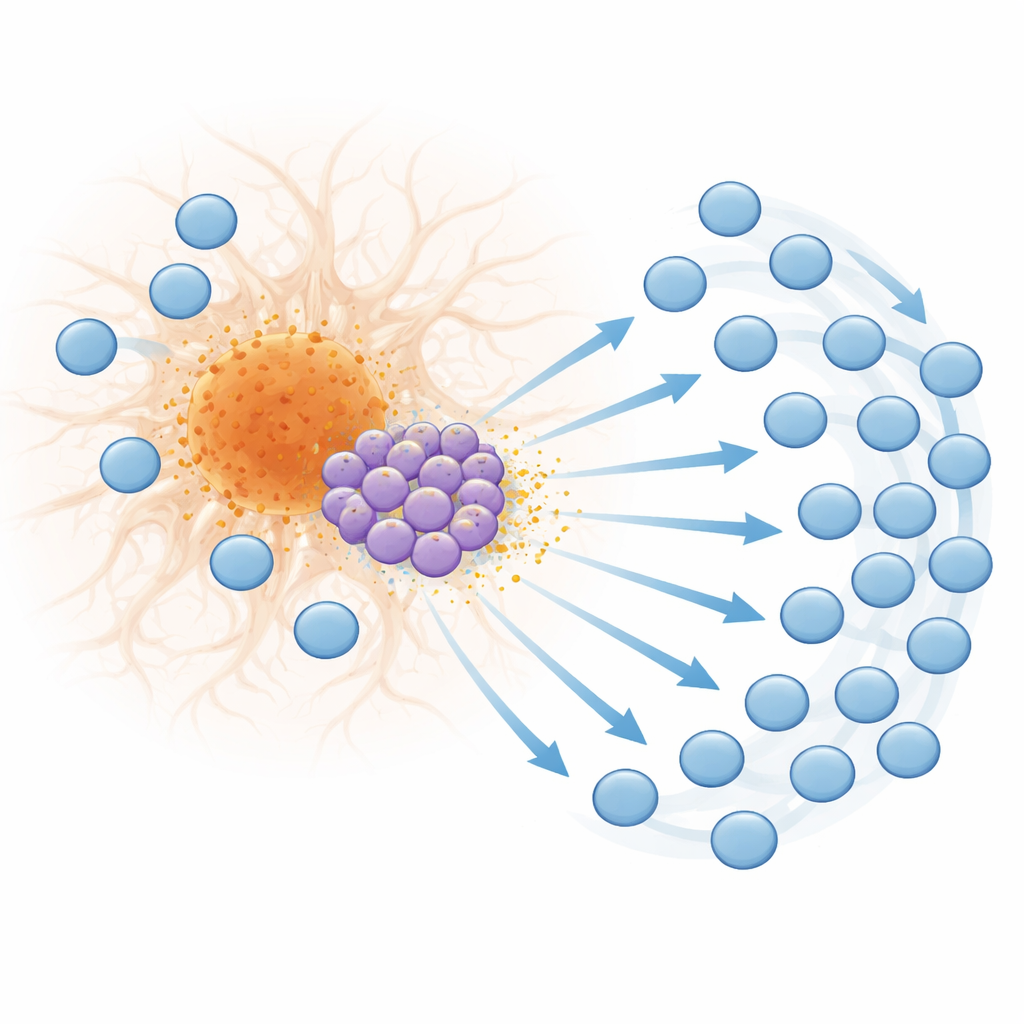
De la activación al agotamiento en el borde de la placa
La afluencia de células T no es solo cuantitativa; también cambia en calidad. En estadios tardíos de la enfermedad, muchas células CD8 alrededor de las placas muestran marcadores de alta activación, potencial citotóxico y expansión clonal —señales de que responden repetidamente a desencadenantes específicos. Al mismo tiempo, estas células comienzan a exhibir rasgos de agotamiento, un estado en el que las células T estimuladas crónicamente pierden eficacia y expresan moléculas inhibitorias como PD-1. El mapeo espacial reveló que estas células T agotadas se acumulan justo en el borde de las placas, lo que sugiere que la estimulación intensa y sostenida por señales asociadas a las placas las empuja a un estado de desgaste. Se hallaron patrones similares de genes sensibles al interferón, CXCL10, marcadores de activación de células T y PD-1 cerca de placas en tejido cerebral humano con Alzheimer, lo que indica que este mecanismo descrito en ratones probablemente sea relevante en personas.
Qué significa esto para futuros tratamientos del Alzheimer
En conjunto, el estudio dibuja una imagen en lapso de tiempo de la inflamación cerebral en la enfermedad amiloide: al principio, las microglías dominan la respuesta, pero a medida que las placas crecen y persisten, un subconjunto especializado de células T CD8 asume el papel principal en la señalización por interferón tipo I y en el reclutamiento de células T. Esta respuesta inmune en evolución puede contribuir al daño neuronal continuo y podría interactuar con tratamientos basados en anticuerpos que eliminan placas, influyendo potencialmente en efectos secundarios relacionados con la inflamación vascular. Para un lector general, el mensaje clave es que en la enfermedad de Alzheimer no solo importan las propias placas, sino también cómo —y cuándo— el sistema inmune responde a ellas. Dirigir las vías de interferón o el eje de señalización CXCL10–CXCR3 en la fase adecuada de la enfermedad podría ayudar a calmar la inflamación perjudicial sin silenciar por completo las defensas del cerebro.
Cita: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Palabras clave: Enfermedad de Alzheimer, beta amiloide, Células T, neuroinflamación, señalización por interferón