Clear Sky Science · pl
Interferon typu I napędza odpowiedź limfocytów T na amyloid beta w ośrodkowym układzie nerwowym
Dlaczego reakcja immunologiczna mózgu na płytki ma znaczenie
Chorobę Alzheimera często opisuje się jako problem związany z toksycznym nagromadzeniem białek w mózgu, ale równie ważnym elementem tej historii jest to, jak układ odpornościowy reaguje na te uszkodzenia. W tym badaniu analizowano, jak określony odgałęzienie układu odpornościowego, napędzane sygnałami interferonu typu I, kieruje limfocyty T w stronę złogów amyloidu beta i przekształca zapalenie mózgu w czasie. Zrozumienie tej zmiennej immunologicznej choreografii może pomóc wyjaśnić, dlaczego uszkodzenia mózgu przyspieszają w późniejszych stadiach choroby i może wskazać lepiej dobrane terminy interwencji.
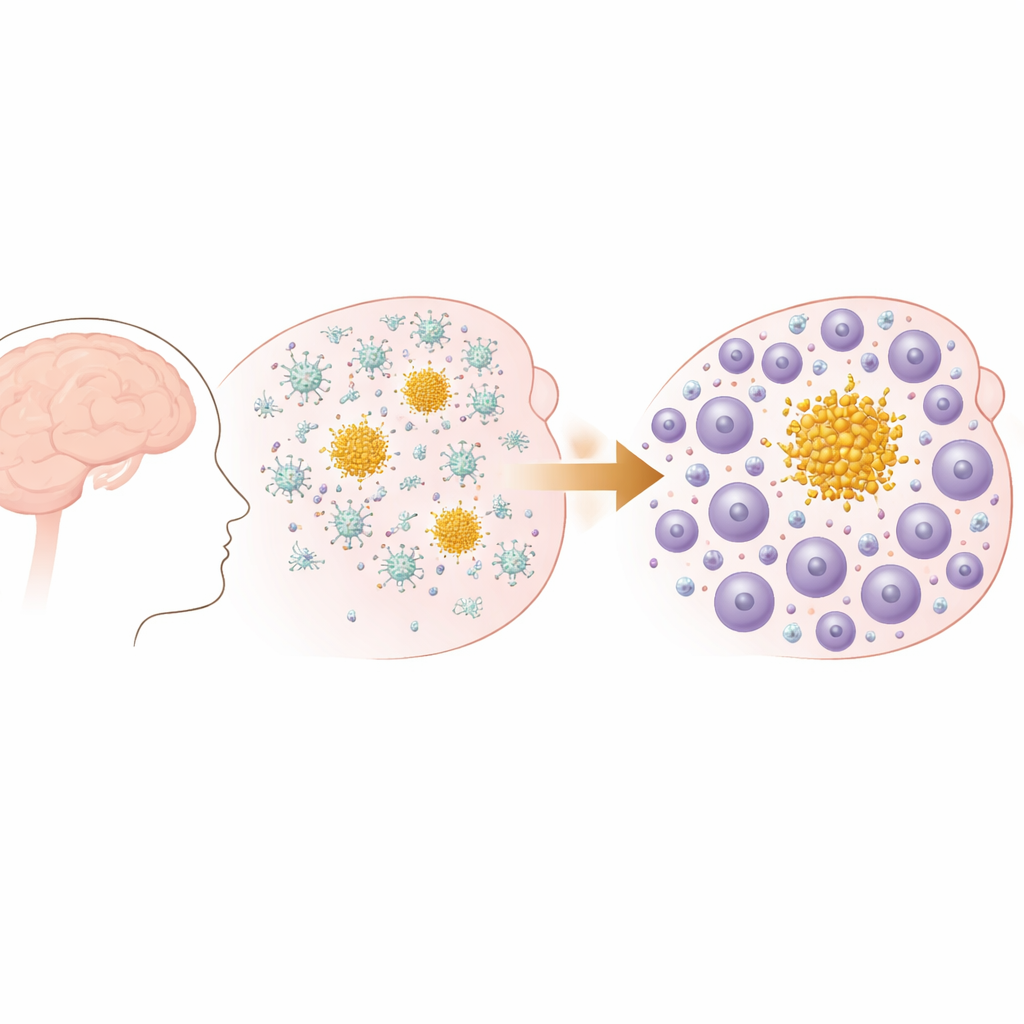
Od wczesnych płytek do zmieniającego się składu odpornościowego
Naukowcy wykorzystali model myszy, który rozwija postępujące złogi amyloidu beta w mózgu, podobne do tych obserwowanych w chorobie Alzheimera i amyloidowej angiopatii mózgowej. We wczesnym okresie życia myszy te tworzą małe depozyty w zewnętrznych warstwach mózgu, które później się rozprzestrzeniają i zwiększają liczebność, szczególnie w obszarach związanych z pamięcią. Testy zachowania potwierdziły, że wraz z narastaniem płytek z wiekiem myszy rozwijały mierzalne pogorszenie codziennych funkcji, takich jak umiejętność budowania gniazda, odzwierciedlając rodzaj stopniowej utraty funkcji widocznej w ludzkiej demencji. Co ważne, w tym modelu występują złogi amyloidu, ale brak jest patologii splotów neurofibrylarnych, co pozwoliło zespołowi skupić się na tym, jak układ odpornościowy reaguje specyficznie na nagromadzenie amyloidu.
Gdy strażnicy mózgu ustępują miejsca nacierającym żołnierzom
Początkowo odpowiedź immunologiczna na płytki jest zdominowana przez mikroglejowe komórki rezydualne mózgu. Na podstawie sekwencjonowania pojedynczych komórek RNA autorzy wykazali, że we wczesnej chorobie mikroglej przyjmuje specyficzne stany związane z chorobą i zwiększa ekspresję genów związanych z fagocytozą i metabolizmem lipidów. Jednak w miarę postępu choroby krajobraz immunologiczny się zmienia. Liczba limfocytów T w mózgu, zwłaszcza CD8, gwałtownie rośnie, a szlaki związane z aktywacją i ruchem limfocytów stają się bardziej wyraźne. Analizy przestrzenne potwierdziły, że nie jest to przypadkowa inwazja: limfocyty T ciasno skupiają się wokół złogów amyloidu w tkance mózgowej, szczególnie przy dużych złogach „parenchymalnych” a nie naczyniowych, i ich liczba wzrasta równolegle z obciążeniem płytek.
Specjalna podgrupa limfocytów T, która wzywa posiłki
Bliższa analiza tych limfocytów ujawniła odrębną podgrupę komórek CD8, która uruchamia zestaw genów zwykle aktywowanych przez interferony typu I — rodzinę cząsteczek sygnałowych związanych z odpowiedzią przeciwwirusową i autoimmunologiczną. Te „stymulowane interferonem” limfocyty T stają się szczególnie liczne w późnej chorobie i znajdują się w pobliżu płytków. Wytwarzają chemokinę CXCL10, niewielkie białko sygnałowe, które wiąże się z receptorem CXCR3 na innych limfocytach T. Transkryptomika przestrzenna wykazała, że zarówno geny odpowiedzialne na interferon, jak i CXCL10 są silnie wzbogacone w sąsiedztwie płytek, a limfocyty produkujące CXCL10 są rozmieszczone tak, by wpływać na pobliskie komórki odpornościowe. Eksperymenty migracyjne in vitro potwierdziły, że limfocyty T przemieszczają się w kierunku sygnałów CXCL10, a unieruchomienie CXCR3 znacząco zmniejsza ich zdolność do podążania za tymi wskazówkami, wspierając model, w którym limfocyty związane z płytkami i napędzane interferonem pomagają sprowadzać kolejne limfocyty do mózgu.
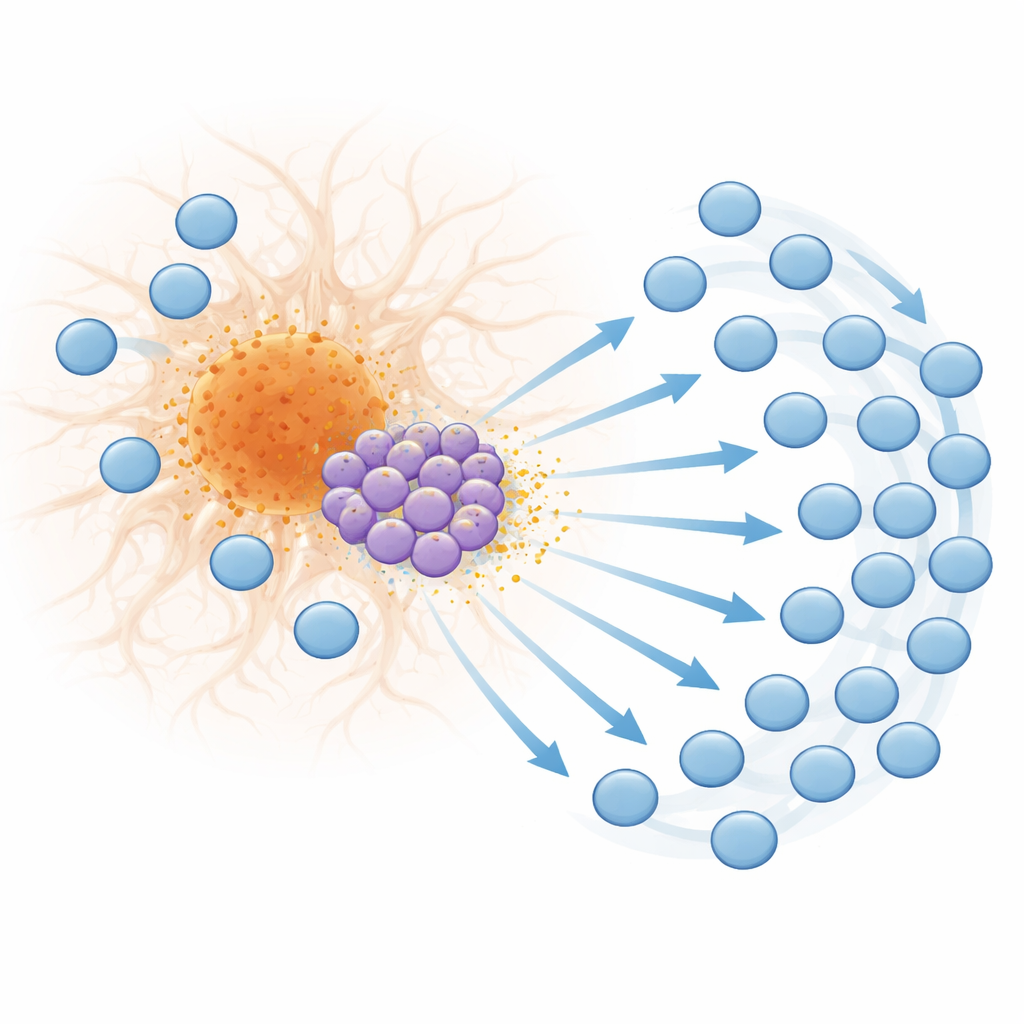
Od aktywacji do wyczerpania na krawędzi płytki
Napływ limfocytów T nie dotyczy tylko liczby; zmienia się też ich jakość. W późnym stadium choroby wiele komórek CD8 wokół płytek wykazuje markery silnej aktywacji, potencjał cytotoksyczny i ekspansję klonalną — oznaki wielokrotnej reakcji na określone bodźce. Jednocześnie te komórki zaczynają wykazywać cechy wyczerpania, stanu, w którym przewlekle stymulowane limfocyty tracą skuteczność i eksponują cząsteczki hamujące, takie jak PD-1. Mapowanie przestrzenne wykazało, że wyczerpane limfocyty kumulują się dokładnie na granicy płytki, co sugeruje, że intensywne, ciągłe pobudzenie przez sygnały związane z płytką prowadzi je do wyczerpania. Podobne wzorce genów odpowiedzi na interferon, CXCL10, markerów aktywacji limfocytów T i PD-1 znaleziono w pobliżu złogów w ludzkiej tkance mózgowej chorych na Alzheimera, co wskazuje, że mechanizm opisany na modelu myszy prawdopodobnie ma znaczenie również u ludzi.
Co to oznacza dla przyszłych terapii choroby Alzheimera
Ogólnie rzecz biorąc, badanie kreśli sekwencję zapalenia mózgu w chorobie związanej z amyloidem: na początku odpowiedź dominuje mikroglej, lecz w miarę wzrostu i utrzymywania się płytek wyspecjalizowana podgrupa komórek CD8 przejmuje rolę głównego napędzacza sygnalizacji interferonu typu I i rekrutacji limfocytów T. Ta ewoluująca odpowiedź immunologiczna może przyczyniać się do trwałego uszkodzenia neuronów i wchodzić w interakcje z terapiami opartymi na przeciwciałach usuwających płytki, potencjalnie wpływając na działania niepożądane związane z zapaleniem naczyń. Dla czytelnika ogólnego kluczowy przekaz brzmi: w chorobie Alzheimera ważne są nie tylko same płytki, ale także to, jak — i kiedy — układ odpornościowy na nie reaguje. Celowanie w szlaki interferonowe lub oś CXCL10–CXCR3 na odpowiednim etapie choroby może pomóc uspokoić szkodliwe zapalenie bez całkowitego wyciszania obrony mózgu.
Cytowanie: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Słowa kluczowe: Choroba Alzheimera, amyloid beta, limfocyty T, neurozapalenie, sygnalizacja interferonowa