Clear Sky Science · sv
Typ I-interferon driver T-cell-responser mot amyloid-beta i centrala nervsystemet
Varför hjärnans immunsvar på plack spelar roll
Alzheimers sjukdom beskrivs ofta som ett problem med giftig proteinuppsamlings i hjärnan, men en lika viktig del av berättelsen är hur immunsystemet reagerar på den skadan. Den här studien undersöker hur en särskild del av immunsystemet, driven av typ I‑interferonsignaler, hjälper till att rikta T‑celler mot amyloid‑beta‑plack och omformar hjärnans inflammation över tid. Att förstå denna föränderliga immundans kan bidra till att förklara varför nervskador accelererar i senare sjukdomsstadier och kan peka ut bättre tidpunkter för behandling.
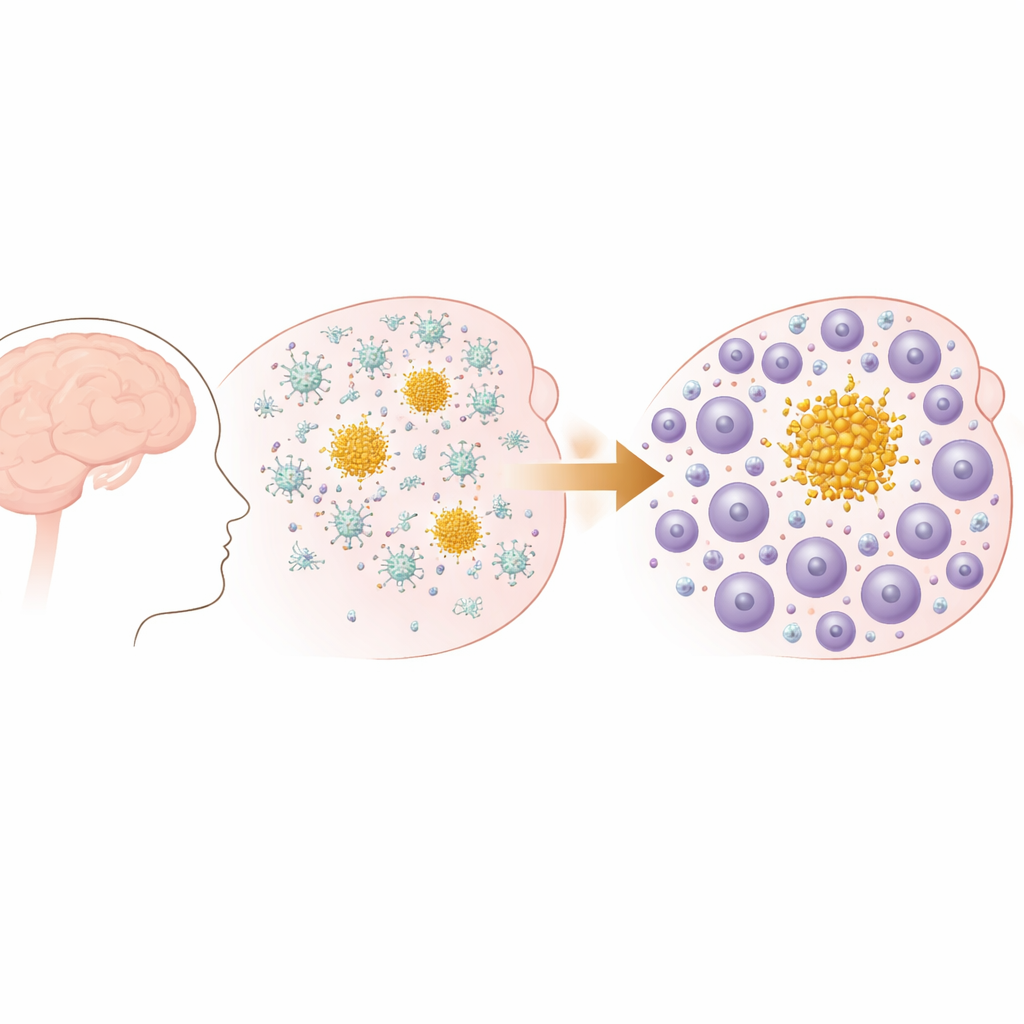
Från tidiga plack till ett förändrat immun‑rollbesättning
Forskarna använde en musmodell som utvecklar progressiva amyloid‑beta‑plack i hjärnan, liknande dem som ses vid Alzheimers sjukdom och cerebral amyloidangiopati. Tidigt i livet bildar dessa möss små avlagringar i hjärnans yttre lager, som senare sprider sig och ökar i antal, särskilt i minnesrelaterade områden. Beteendetester bekräftade att när placken ackumulerades med åldern utvecklade mössen mätbara försämringar i vardagliga funktioner som nästningsbeteende, vilket speglar den gradvisa funktionsförlust som ses vid mänsklig demens. Viktigt är att modellen har amyloidplack men ingen tau‑tangle‑patologi, vilket låter teamet fokusera på hur immunsystemet svarar specifikt på amyloidansamling.
När hjärnans väktare ger vika för invaderande fotsoldater
I början domineras immunsvaret på placken av mikroglia, hjärnans egna immunceller. Med singelcells‑RNA‑sekvensering visade författarna att mikroglia i tidig sjukdom antar särskilda sjukdomsassocierade tillstånd och uppreglerar gener kopplade till att uppta skräp och hantera lipider. Men när sjukdomen fortskrider förändras det immunologiska landskapet. Antalet T‑celler i hjärnan, särskilt CD8‑T‑celler, ökar kraftigt, och vägar relaterade till lymfocytaktivering och rörelse blir mer framträdande. Rumsbaserade analyser bekräftade att detta inte är en slumpmässig invasion: T‑celler klustrar tätt runt amyloidplack i hjärnvävnad, särskilt kring stora parenkymala plack snarare än de i blodkärl, och deras antal ökar i takt med plackbördan.
En specialiserad T‑cellsgrupp som kallar in förstärkningar
När man granskar dessa T‑celler närmare identifierade teamet en distinkt undergrupp av CD8‑T‑celler som aktiverar en rad gener som normalt triggas av typ I‑interferoner, en familj antivirala och autoimmuna signalmolekyler. Dessa "interferon‑stimulerade" T‑celler blir särskilt många i sen sjukdom och finns nära plack. De producerar kemokinen CXCL10, ett litet proteinsignal som binder receptorn CXCR3 på andra T‑celler. Rumsbaserad transkriptomik visade att både interferonresponderande gener och CXCL10 är starkt berikade i plackgrannskap, och att CXCL10‑producerande T‑celler är placerade för att påverka andra närliggande immunceller. Laboratoriemigrationsexperiment bekräftade att T‑celler rör sig mot CXCL10‑signaler och att inaktivering av CXCR3 kraftigt minskar deras förmåga att följa dessa signaler, vilket stöder en modell där placksassocierade interferon‑drivna T‑celler hjälper till att dra in ytterligare T‑celler i hjärnan.
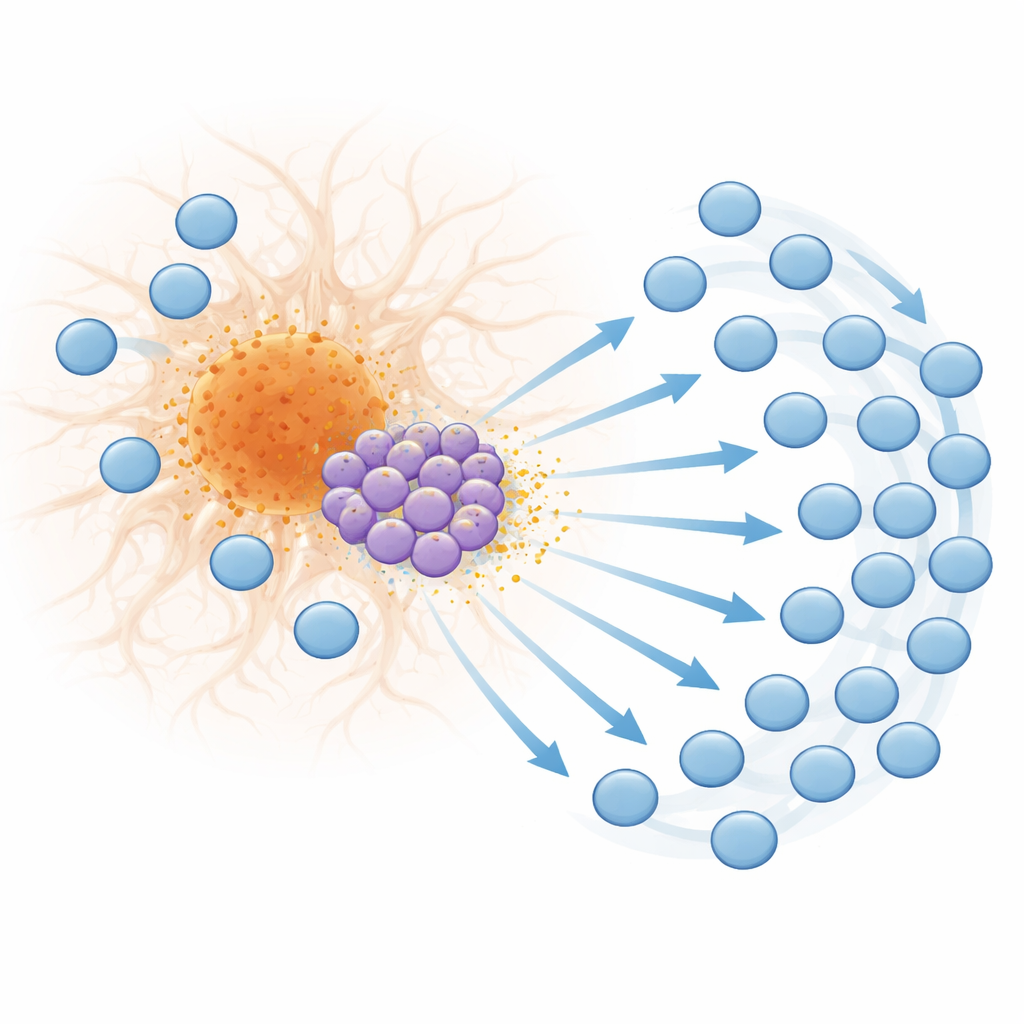
Från aktivering till utmattning vid plackkanten
T‑cellsinfluxen är inte bara numerisk; den förändrar också kvaliteten. I sena sjukdomsstadier visar många CD8‑T‑celler runt plack tecken på hög aktivering, cytotoxisk kapacitet och klonal expansion — tecken på att de upprepade gånger svarar på specifika triggers. Samtidigt börjar dessa celler uppvisa kännetecken för utmattning, ett tillstånd där kroniskt stimulerade T‑celler förlorar effektivitet och uttrycker inhibitoriska molekyler som PD‑1. Rumsbaserad kartläggning visade att dessa utmattade T‑celler ackumuleras precis i gränsen till placken, vilket tyder på att intensiv, pågående stimulans av placksassocierade signaler driver dem i ett utslitet tillstånd. Liknande mönster av interferon‑responsgener, CXCL10, T‑cellsaktiveringsmarkörer och PD‑1 hittades nära plack i mänsklig Alzheimers hjärnvävnad, vilket indikerar att denna musbaserade mekanism sannolikt är relevant för människor.
Vad detta betyder för framtida behandlingar mot Alzheimers
Sammanfattningsvis målar studien upp en time‑lapsebild av hjärnans inflammation vid amyloidsjukdom: tidigt dominerar mikroglia svaret, men när placken växer och kvarstår tar en specialiserad undergrupp av CD8‑T‑celler över som huvuddrivare av typ I‑interferon‑signalering och T‑cellsrekrytering. Detta föränderliga immunsvar kan bidra till fortlöpande nervcellsskada och kan samspela med antikroppsbaserade behandlingar som tar bort plack, vilket potentiellt påverkar biverkningar kopplade till vaskulär inflammation. För en allmän läsare är huvudbudskapet att vid Alzheimers sjukdom är det inte bara placken i sig som spelar roll, utan också hur — och när — immunsystemet reagerar på dem. Att rikta interferonvägar eller CXCL10–CXCR3‑signaleringen i rätt sjukdomsstadium kan hjälpa till att dämpa skadlig inflammation utan att helt tysta hjärnans försvar.
Citering: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Nyckelord: Alzheimers sjukdom, amyloid-beta, T‑celler, neuroinflammation, interferonsignalering