Clear Sky Science · de
Typ-I-Interferon steuert T‑Zellantworten auf Amyloid‑Beta im zentralen Nervensystem
Warum die Immunantwort des Gehirns auf Plaques wichtig ist
Die Alzheimer‑Krankheit wird oft als Problem toxischer Proteinablagerungen im Gehirn beschrieben, doch ebenso bedeutsam ist, wie das Immunsystem auf diese Schäden reagiert. Diese Studie untersucht, wie ein bestimmter Zweig des Immunsystems, gesteuert durch Typ‑I‑Interferon‑Signale, T‑Zellen in Richtung Amyloid‑Beta‑Plaques lenkt und die Gehirnentzündung im Laufe der Zeit umgestaltet. Das Verständnis dieses sich verändernden immunologischen Zusammenspiels könnte helfen zu erklären, warum die Hirnschädigung in späteren Krankheitsstadien beschleunigt und könnte auf besser getimte Behandlungsansätze hinweisen.
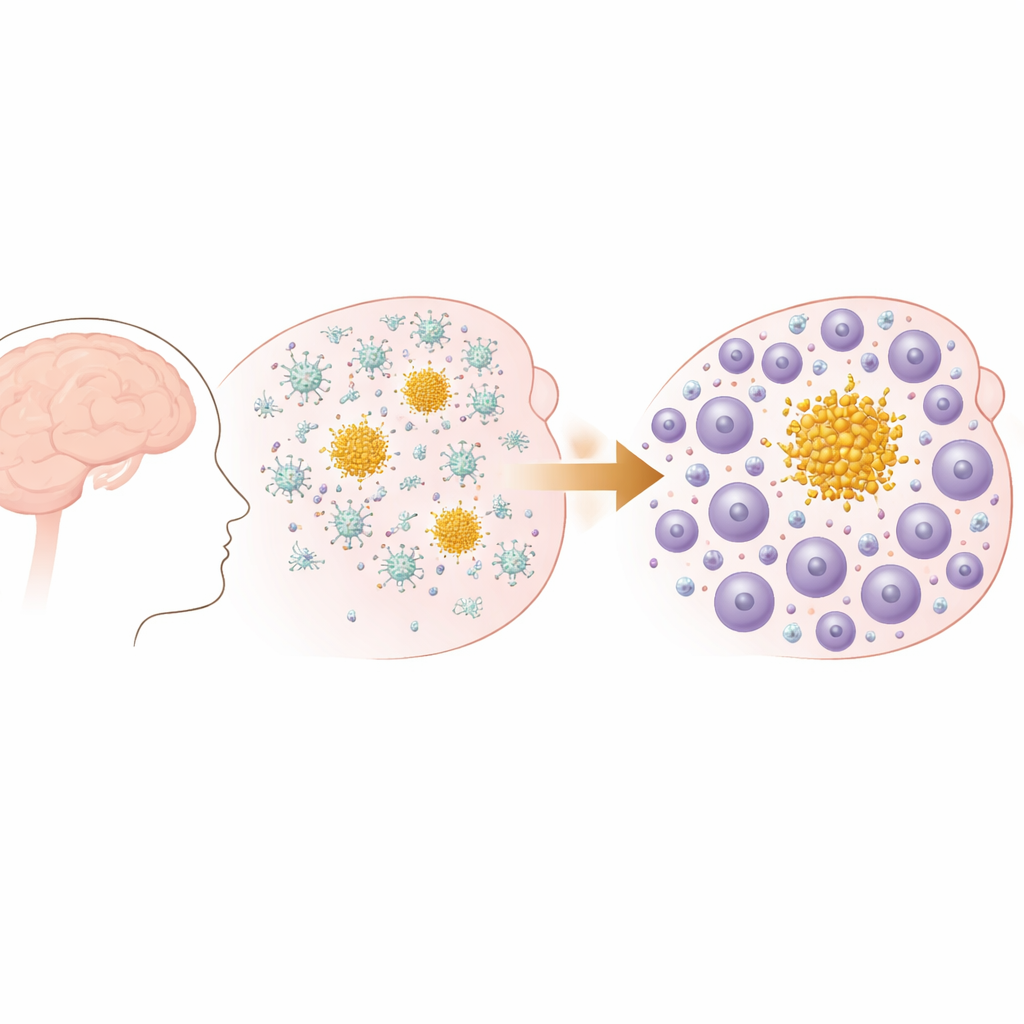
Von frühen Plaques zu einem wechselnden Immunensemble
Die Forschenden verwendeten ein Mausmodell, das progressive Amyloid‑Beta‑Plaques im Gehirn ausbildet, ähnlich denen, die bei Alzheimer und zerebraler Amyloidangiopathie zu sehen sind. Früh im Leben bilden diese Mäuse kleine Ablagerungen in den äußeren Schichten des Gehirns, die später ausbreiten und besonders in gedächtnisrelevanten Regionen an Zahl zunehmen. Verhaltenstests bestätigten, dass mit zunehmender Plaquebildung auch messbare Einbußen in alltäglichen Funktionen wie Nestbau auftraten, was dem schrittweisen Funktionsverlust beim Menschen ähnelt. Wichtig ist, dass dieses Modell Plaques, aber keine Tau‑Verfilzungen aufweist, sodass das Team gezielt untersuchen konnte, wie das Immunsystem speziell auf Amyloid‑Ablagerungen reagiert.
Wenn die Wächter des Gehirns Platz machen für eindringende Soldaten
Zunächst dominiert die Reaktion auf Plaques die Mikroglia, die residenten Immunzellen des Gehirns. Mit Einzelzell‑RNA‑Sequenzierung zeigten die Autorinnen und Autoren, dass Mikroglia in frühen Stadien krankheitsassoziierte Zustände annehmen und Gene hochregulieren, die mit dem Aufräumen von Zelltrümmern und Fettstoffwechsel zu tun haben. Mit Fortschreiten der Erkrankung verändert sich jedoch die immunologische Landschaft. Die Zahl der T‑Zellen im Gehirn, insbesondere der CD8‑T‑Zellen, steigt stark an, und Signalwege, die mit Lymphozytenaktivierung und ‑migration zusammenhängen, werden prominenter. Räumliche Analysen bestätigten, dass es sich nicht um eine zufällige Invasion handelt: T‑Zellen sammeln sich eng um Amyloid‑Plaques im Gehirngewebe, insbesondere um große parenchymale Plaques statt um solche in Blutgefäßen, und ihre Zahl wächst im Einklang mit der Plaquelast.
Eine spezialisierte T‑Zell‑Untergruppe, die Verstärkung herbeiruft
Bei genauerer Betrachtung identifizierte das Team eine distincte Untergruppe von CD8‑T‑Zellen, die eine Reihe von Genen hochfährt, die normalerweise durch Typ‑I‑Interferone ausgelöst werden — eine Familie antiviraler und autoimmuner Signalstoffe. Diese „Interferon‑stimulierenden“ T‑Zellen werden besonders in späten Krankheitsstadien zahlreich und befinden sich in Plaquenähe. Sie produzieren die Chemokin CXCL10, ein kleines Signalprotein, das an den Rezeptor CXCR3 auf anderen T‑Zellen bindet. Räumliche Transkriptomik zeigte, dass sowohl interferon‑ansprechende Gene als auch CXCL10 in Plaquenachbarschaften stark angereichert sind und dass CXCL10‑produzierende T‑Zellen so positioniert sind, dass sie benachbarte Immunzellen beeinflussen können. Laborbasierte Migrationsversuche bestätigten, dass T‑Zellen auf CXCL10‑Signale zuwandern und dass die Deaktivierung von CXCR3 ihre Fähigkeit, diesen Signalen zu folgen, deutlich reduziert — was ein Modell stützt, in dem interferongetriebene, plaque‑assoziierte T‑Zellen weitere T‑Zellen ins Gehirn ziehen.
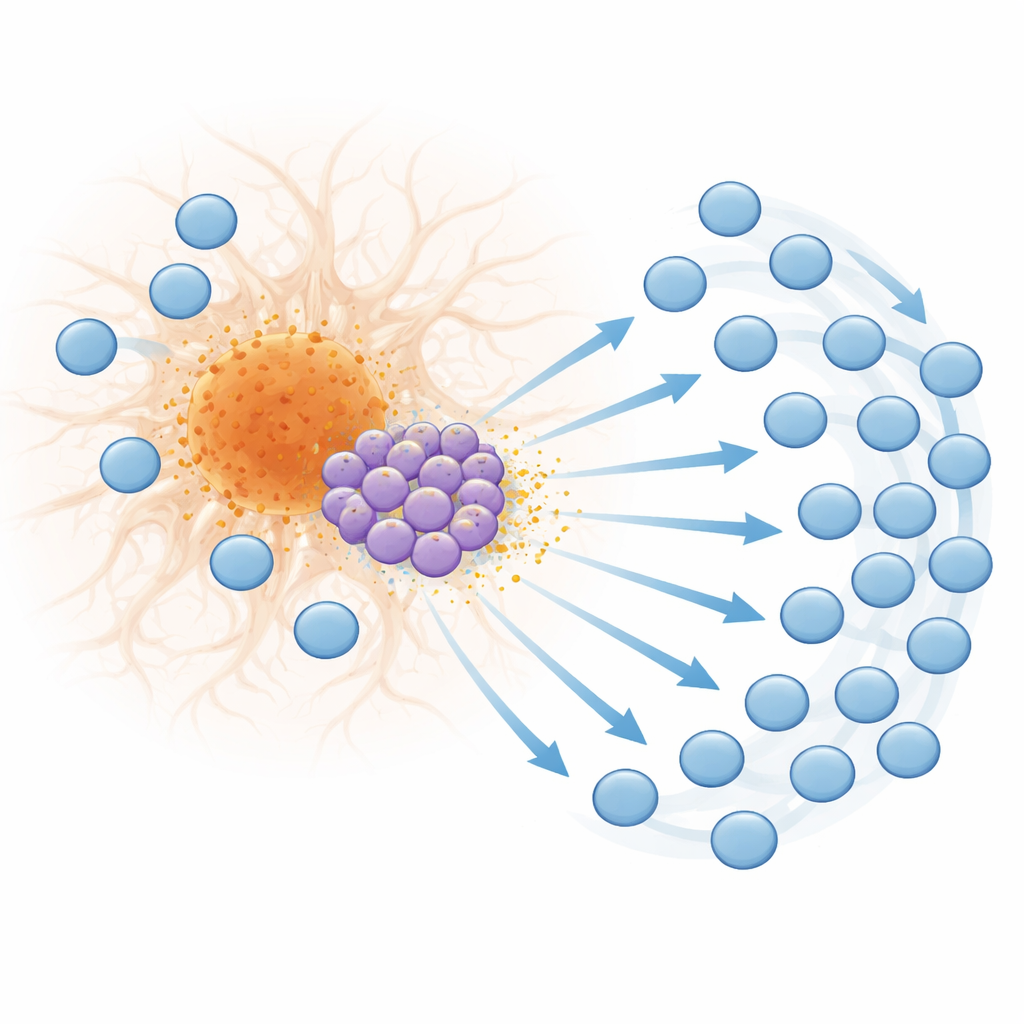
Von Aktivierung zu Erschöpfung am Plaquerand
Der Zustrom von T‑Zellen betrifft nicht nur die Zahl, sondern auch die Qualität. In späten Krankheitsstadien zeigen viele CD8‑T‑Zellen um Plaques Marker hoher Aktivierung, zytotoxisches Potenzial und klonale Expansion — Zeichen dafür, dass sie wiederholt auf spezifische Reize reagieren. Zugleich beginnen diese Zellen, Merkmale der Erschöpfung zu zeigen, einem Zustand, in dem chronisch stimulierte T‑Zellen an Effektivität verlieren und inhibitorische Moleküle wie PD‑1 exprimieren. Räumliche Kartierungen zeigten, dass diese erschöpften T‑Zellen sich direkt am Rand der Plaques ansammeln, was darauf hindeutet, dass intensive, andauernde Stimulation durch plaque‑assoziierte Signale sie in einen ausgebrannten Zustand treibt. Ähnliche Muster interferon‑responsiver Gene, CXCL10, T‑Zell‑Aktivierungsmarker und PD‑1 wurden auch in der Nähe von Plaques im Gehirngewebe von Menschen mit Alzheimer gefunden, was darauf hindeutet, dass der in Mäusen beschriebene Mechanismus vermutlich für den Menschen relevant ist.
Was das für künftige Alzheimer‑Therapien bedeutet
Insgesamt zeichnet die Studie ein Zeitrafferbild der Gehirnentzündung bei Amyloid‑Erkrankung: Zu Beginn dominieren Mikroglia die Antwort, doch mit dem Wachstum und dem Fortbestehen von Plaques übernimmt eine spezialisierte Untergruppe von CD8‑T‑Zellen die Hauptrolle bei Typ‑I‑Interferon‑Signalgebung und der Rekrutierung weiterer T‑Zellen. Diese sich wandelnde Immunantwort könnte zu anhaltender Nervenzellschädigung beitragen und mit antibodybasierten Therapieansätzen, die Plaques entfernen, interagieren und so vaskulär bedingte Nebenwirkungen beeinflussen. Für die allgemeine Leserschaft ist die Kernbotschaft, dass bei Alzheimer nicht nur die Plaques selbst entscheidend sind, sondern auch wie — und wann — das Immunsystem auf sie reagiert. Die gezielte Modulation von Interferon‑Wegen oder der CXCL10–CXCR3‑Achse im richtigen Krankheitsstadium könnte helfen, schädliche Entzündungsreaktionen zu dämpfen, ohne die Abwehrfunktionen des Gehirns vollständig zu unterdrücken.
Zitation: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Schlüsselwörter: Alzheimer‑Krankheit, Amyloid‑Beta, T‑Zellen, Neuroinflammation, Interferon‑Signalgebung