Clear Sky Science · fr
Les interférons de type I pilotent les réponses des cellules T contre le bêta-amyloïde dans le système nerveux central
Pourquoi la réponse immunitaire du cerveau aux plaques est importante
La maladie d’Alzheimer est souvent décrite comme un problème d’accumulation de protéines toxiques dans le cerveau, mais une autre partie tout aussi importante de l’histoire est la manière dont le système immunitaire réagit à ces lésions. Cette étude examine comment une branche spécifique du système immunitaire, sous la conduite des signaux des interférons de type I, oriente les cellules T vers les plaques de bêta-amyloïde et reconfigure l’inflammation cérébrale au fil du temps. Comprendre cette chorégraphie immunitaire évolutive peut aider à expliquer pourquoi les lésions cérébrales s’accélèrent aux stades avancés de la maladie et pourrait indiquer des traitements mieux synchronisés.
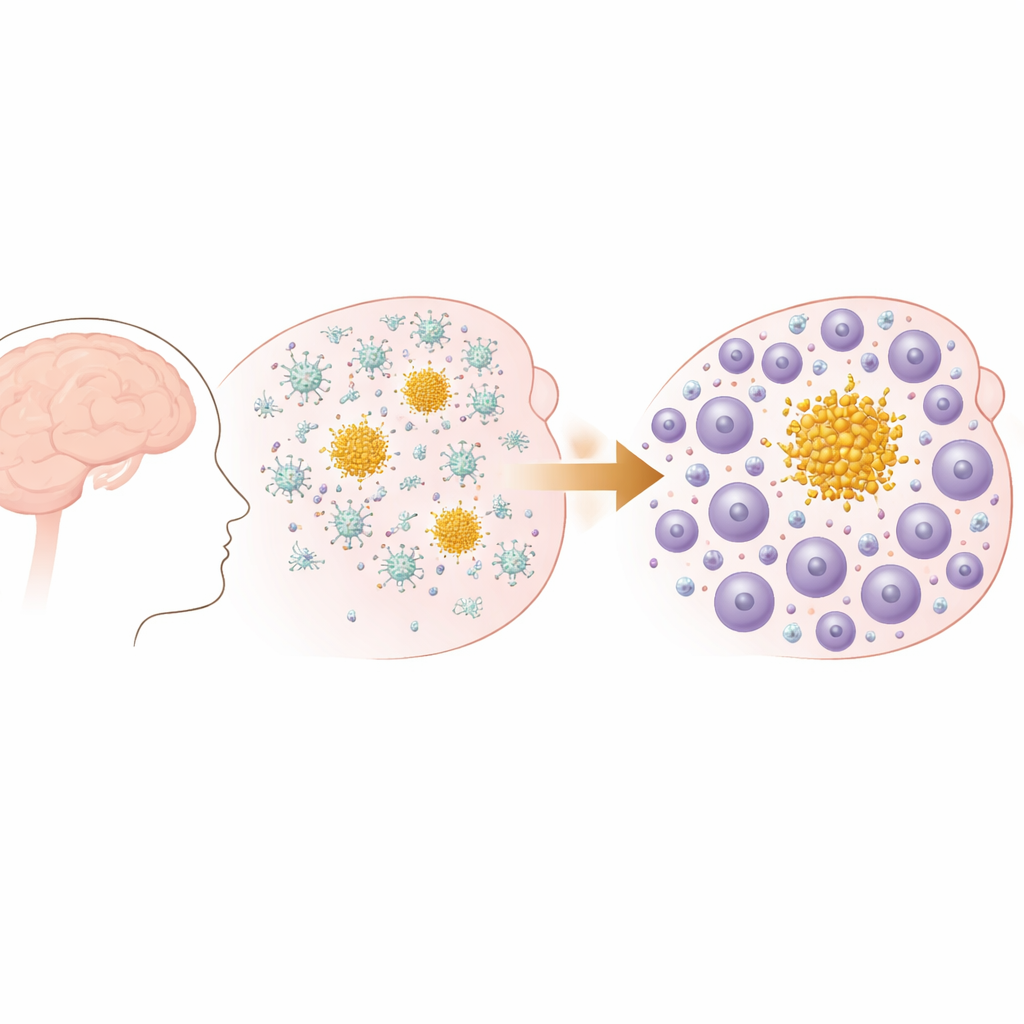
Des premières plaques à une distribution immunitaire changeante
Les chercheurs ont utilisé un modèle murin qui développe des plaques progressives de bêta-amyloïde dans le cerveau, semblables à celles observées dans la maladie d’Alzheimer et l’angiopathie amyloïde cérébrale. Tôt dans la vie, ces souris forment de petits dépôts dans les couches externes du cerveau, qui se propagent et augmentent en nombre avec le temps, en particulier dans les régions liées à la mémoire. Des tests comportementaux ont confirmé que, à mesure que les plaques s’accumulaient avec l’âge, les souris présentaient des déclins mesurables des fonctions quotidiennes comme la construction de nids, reflétant le type de perte fonctionnelle progressive observée dans la démence humaine. Fait important, ce modèle présente des plaques amyloïdes sans pathologie de dégénérescence en enchevêtrements, ce qui a permis à l’équipe de se concentrer sur la réponse immunitaire spécifiquement ciblée sur l’accumulation d’amyloïde.
Quand les gardiens du cerveau cèdent la place à des soldats envahisseurs
Au début, la réponse immunitaire aux plaques est dominée par les microglies, cellules immunitaires résidentes du cerveau. Grâce au séquençage ARN unicellulaire, les auteurs ont montré que, en phase précoce de la maladie, ces microglies adoptent des états associés à la pathologie et augmentent l’expression de gènes liés à l’élimination de débris et à la gestion des lipides. Mais à mesure que la maladie progresse, le paysage immunitaire change. Le nombre de cellules T dans le cerveau, en particulier des CD8, augmente fortement, et les voies associées à l’activation et à la migration des lymphocytes deviennent plus marquées. Des analyses spatiales ont confirmé qu’il ne s’agit pas d’une invasion aléatoire : les cellules T se regroupent étroitement autour des plaques amyloïdes dans le tissu cérébral, notamment autour de grandes plaques « parenchymateuses » plutôt que de celles des vaisseaux sanguins, et leur nombre croît en parallèle avec la charge en plaques.
Un sous-ensemble spécialisé de cellules T qui appelle des renforts
En examinant de plus près ces cellules T, l’équipe a identifié un sous-ensemble distinct de CD8 qui active un ensemble de gènes normalement induits par les interférons de type I, une famille de molécules de signalisation antivirales et impliquées dans l’auto-immunité. Ces cellules T « stimulées par les interférons » deviennent particulièrement abondantes aux stades tardifs et se trouvent à proximité des plaques. Elles produisent la chimiokine CXCL10, un petit signal protéique qui se lie au récepteur CXCR3 sur d’autres cellules T. La transcriptomique spatiale a montré que les gènes répondant aux interférons et CXCL10 sont fortement enrichis dans les voisinages des plaques, et que les cellules T productrices de CXCL10 sont placées de façon à influencer d’autres cellules immunitaires à proximité. Des expériences de migration en laboratoire ont confirmé que les cellules T se déplacent vers les signaux CXCL10 et que la désactivation de CXCR3 réduit nettement leur capacité à suivre ces repères, soutenant un modèle dans lequel les cellules T associées aux plaques et guidées par les interférons aident à attirer des cellules T supplémentaires dans le cerveau.
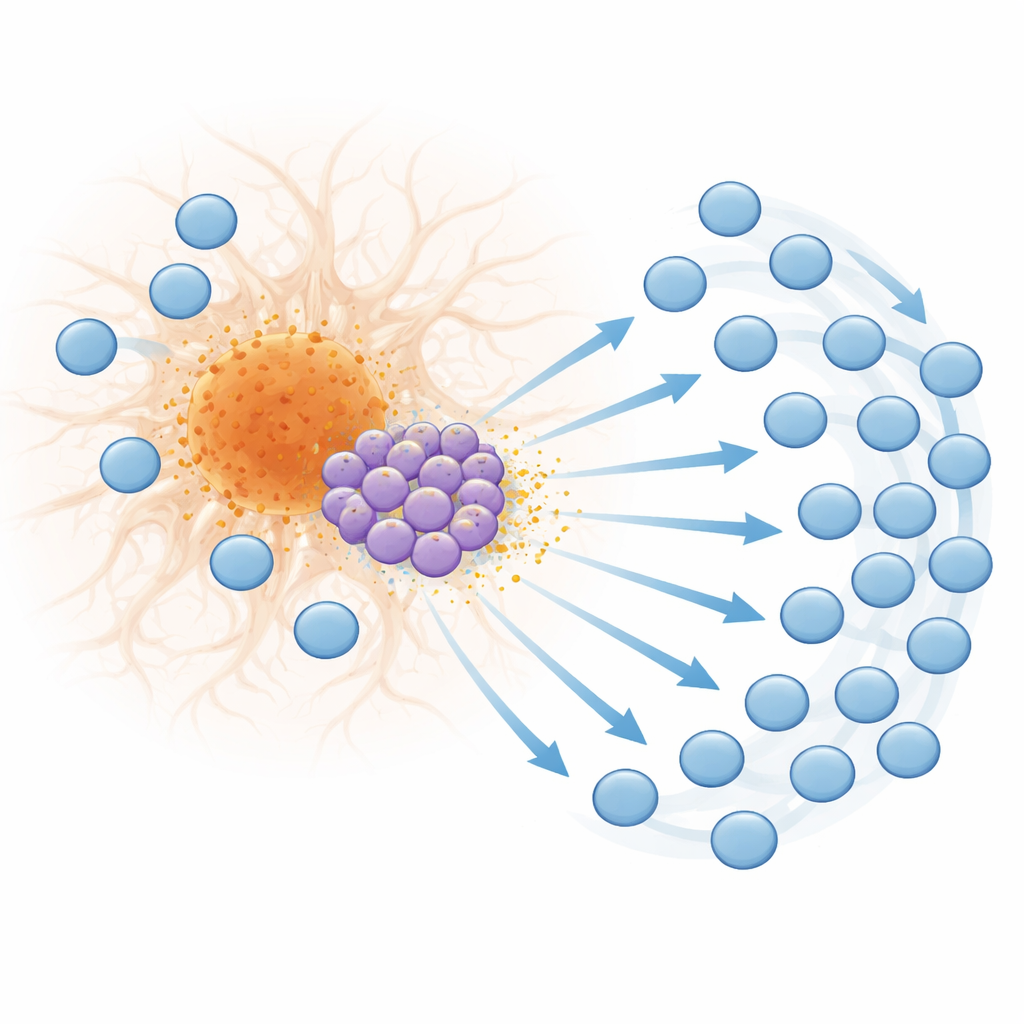
De l’activation à l’épuisement au bord des plaques
L’afflux de cellules T n’est pas qu’une question de nombre ; il change aussi leur nature. Aux stades avancés de la maladie, de nombreuses cellules T CD8 autour des plaques montrent des marqueurs d’activation élevée, un potentiel cytotoxique et une expansion clonale — des signes qu’elles répondent de façon répétée à des déclencheurs spécifiques. En même temps, ces cellules commencent à présenter des caractéristiques d’épuisement, un état dans lequel des cellules T stimulées de façon chronique perdent de leur efficacité et expriment des molécules inhibitrices telles que PD-1. Le cartographie spatiale a révélé que ces cellules T épuisées s’accumulent juste à la bordure des plaques, suggérant qu’une stimulation intense et continue par des signaux associés aux plaques les conduit à cet état de fatigue. Des schémas similaires de gènes répondant aux interférons, de CXCL10, de marqueurs d’activation des cellules T et de PD-1 ont été retrouvés près des plaques dans des tissus cérébraux d’humains atteints d’Alzheimer, indiquant que ce mécanisme identifié chez la souris est probablement pertinent chez l’homme.
Ce que cela implique pour les futurs traitements de l’Alzheimer
Globalement, l’étude dresse un tableau en accéléré de l’inflammation cérébrale dans la maladie amyloïde : au départ, les microglies dominent la réponse, mais à mesure que les plaques croissent et persistent, un sous-ensemble spécialisé de cellules T CD8 devient le principal moteur de la signalisation par les interférons de type I et du recrutement des cellules T. Cette réponse immunitaire évolutive pourrait contribuer aux dommages neuronaux continus et interagir avec les traitements à base d’anticorps qui éliminent les plaques, influençant potentiellement des effets secondaires liés à l’inflammation vasculaire. Pour le lecteur général, le message clé est que, dans la maladie d’Alzheimer, ce ne sont pas seulement les plaques qui comptent, mais aussi comment — et quand — le système immunitaire y répond. Cibler les voies des interférons ou l’axe de signalisation CXCL10–CXCR3 au bon stade de la maladie pourrait aider à calmer une inflammation nocive sans étouffer complètement les défenses cérébrales.
Citation: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Mots-clés: Maladie d’Alzheimer, bêta-amyloïde, cellules T, neuroinflammation, signalisation par les interférons