Clear Sky Science · ja
I型インターフェロンは中枢神経系におけるアミロイドβに対するT細胞応答を駆動する
なぜ脳のプラークに対する免疫応答が重要なのか
アルツハイマー病はしばしば脳内での毒性タンパク質の蓄積の問題として語られますが、同じくらい重要なのはその損傷に対して免疫系がどのように反応するかです。本研究は、I型インターフェロンシグナルに駆動される免疫の特定の枝が、どのようにしてT細胞をアミロイドβプラークへ誘導し、時間とともに脳内の炎症反応を再構築するかを探ります。この変化する免疫の振る舞いを理解することは、疾病の後期に神経障害が加速する理由を説明し、より適切な時期の治療を示唆するかもしれません。
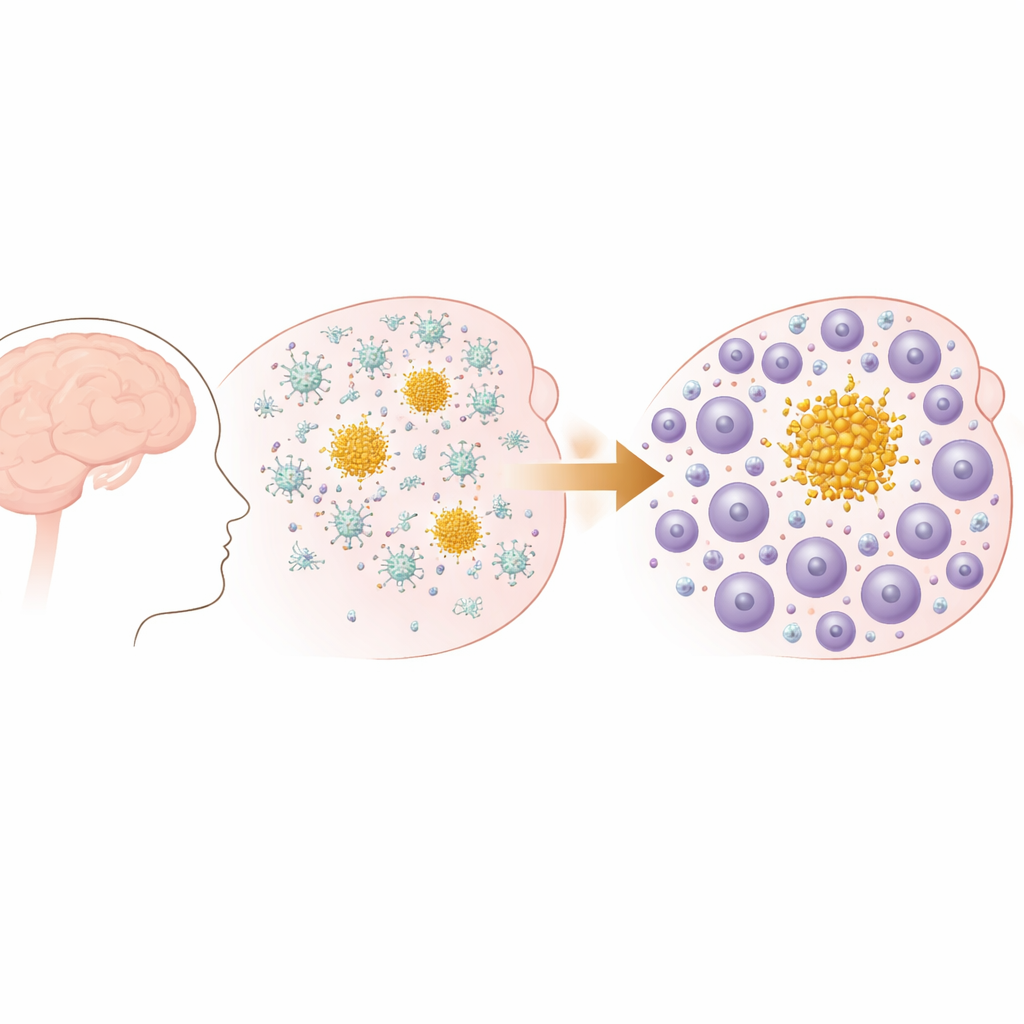
初期プラークから変化する免疫の顔ぶれへ
研究者たちは、アルツハイマー病や脳アミロイド血管症で見られるものと類似した進行性のアミロイドβプラークを脳内に生じるマウスモデルを用いました。若齢期にはこれらのマウスは大脳皮質の外層に小さな沈着を形成し、年を追うごとに特に記憶に関わる領域で広がり数を増やします。行動試験により、プラークが蓄積するにつれて巣作りといった日常的機能が年齢とともに低下することが確認され、人間の認知症で見られる漸進的な機能喪失を反映しています。重要なのは、このモデルはアミロイドプラークは示すもののタングル病理を伴わないため、研究チームがアミロイド蓄積に対する免疫応答に特化して焦点を当てられる点です。
脳の守り手が退き、侵入する歩兵たちが現れるとき
初期段階では、プラークに対する免疫応答は脳常在の免疫細胞であるミクログリアが主導します。単一細胞RNAシーケンシングを用いて、著者らは初期病期のミクログリアが特有の疾患関連状態を取り、破片の取り込みや脂質代謝に関連する遺伝子を増強することを示しました。しかし病気が進行するにつれて免疫の景観は変わります。脳内のT細胞数、特にCD8 T細胞が急増し、リンパ球の活性化や移動に関わる経路がより顕著になります。空間的解析はこれがランダムな侵入ではないことを確認しました:T細胞は脳組織中のアミロイドプラークの周囲に密集しており、とくに血管内のプラークよりも“実質性(パレンキマル)”の大きなプラークの周辺に集まり、その数はプラーク負荷に合わせて増加します。
援軍を呼び寄せる特殊なT細胞サブセット
これらのT細胞を詳しく調べると、I型インターフェロンによって通常誘導される一群の遺伝子を発現する、特異的なCD8 T細胞サブセットが同定されました。これらの「インターフェロン応答」T細胞は病気の後期に特に豊富になり、プラークの近傍に局在しています。彼らはケモカインCXCL10を産生し、これは他のT細胞上の受容体CXCR3に結合する小さなシグナル分子です。空間トランスクリプトミクスは、インターフェロン応答遺伝子とCXCL10がプラーク周辺で強く濃縮していることを示し、CXCL10を産生するT細胞が近傍の他の免疫細胞に影響を与え得る位置にいることを示しました。実験室での走化性(移動)実験では、T細胞がCXCL10シグナルに向かって移動すること、そしてCXCR3を無効にするとそれらがこの誘導に従う能力が著しく低下することが確認され、プラークに関連するインターフェロン駆動のT細胞が追加のT細胞を脳内へ引き寄せるモデルを支持します。
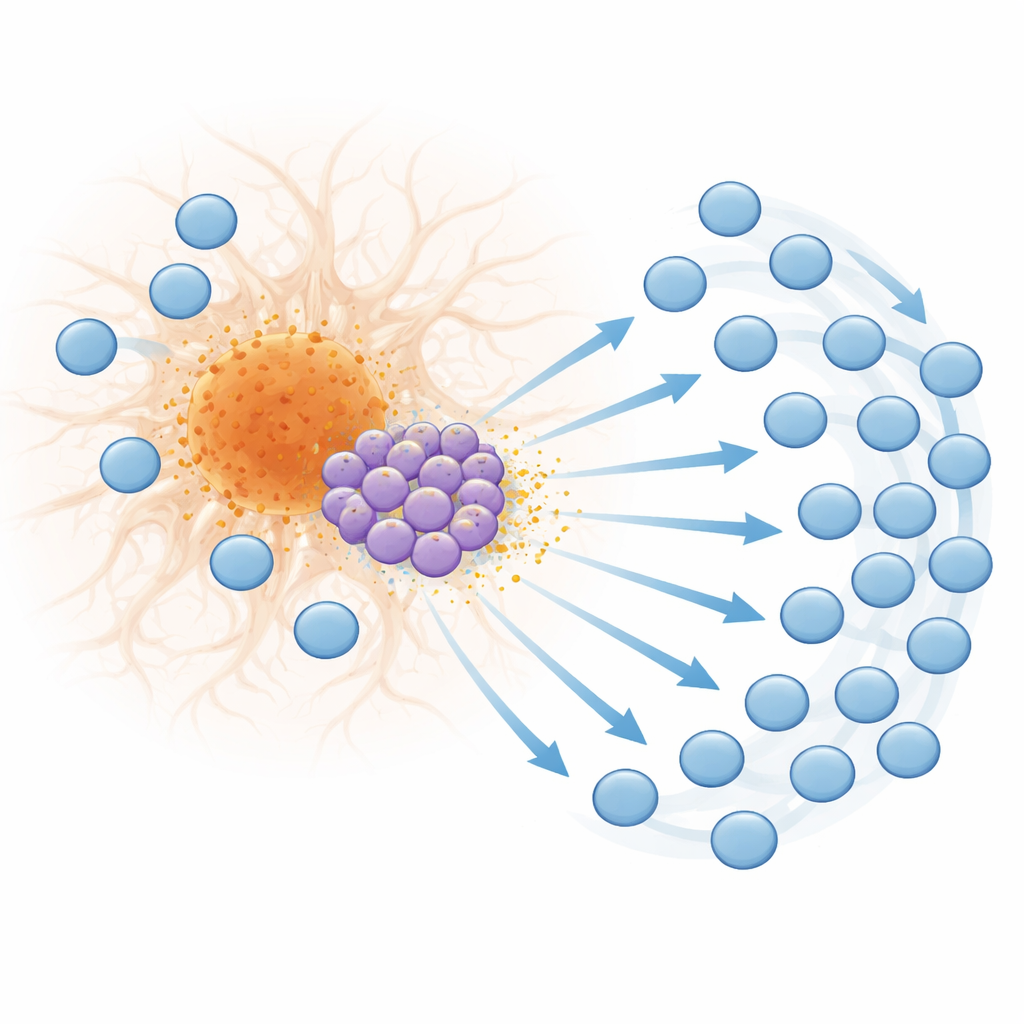
プラーク縁での活性化から疲弊へ
T細胞の流入は単に数の増加だけでなく質的な変化ももたらします。病気後期には、プラーク周辺の多くのCD8 T細胞が高度な活性化、細胞傷害性の潜在力、クローン性拡大のマーカーを示し—これはそれらが特定の刺激に繰り返し反応している兆候です。同時に、これらの細胞は疲弊(エグゾースト)という特徴も示し始めます。疲弊とは慢性的に刺激されたT細胞が効果を失い、PD-1などの抑制分子を発現する状態です。空間マッピングは、こうした疲弊したT細胞がプラークのちょうど境界部に蓄積することを明らかにし、プラークに伴う強く持続的な刺激がそれらを疲弊状態へ追い込むことを示唆します。ヒトのアルツハイマー脳組織でも、プラーク近傍で同様のインターフェロン応答遺伝子、CXCL10、T細胞活性化マーカー、PD-1のパターンが見られ、このマウス由来のメカニズムが人にも関連性がある可能性を示しています。
将来のアルツハイマー治療にとっての意味
全体として、本研究はアミロイド疾患における脳内炎症のタイムラプス的な図を描きます:初期にはミクログリアが応答を主導しますが、プラークが成長し持続するにつれて、I型インターフェロンシグナル伝達とT細胞動員の主要な駆動者として特殊なCD8 T細胞サブセットが台頭します。この進化する免疫応答は継続的な神経細胞損傷に寄与し得るほか、プラークを除去する抗体治療と相互作用し、血管性炎症に関連した副作用に影響を与える可能性があります。一般読者への要点は、アルツハイマー病において重要なのはプラーク自体だけでなく、免疫系がそれに“どう、いつ”反応するかであるということです。適切な病期でインターフェロン経路やCXCL10–CXCR3シグナル軸を標的にすることは、脳の防御機構を完全に遮断することなく有害な炎症を抑える助けとなる可能性があります。
引用: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
キーワード: アルツハイマー病, アミロイドβ, T細胞, 神経炎症, インターフェロンシグナル伝達