Clear Sky Science · nl
Type I-interferon stuurt T-celresponsen tegen amyloïde bèta in het centraal zenuwstelsel
Waarom de immuunreactie van de hersenen op plaques ertoe doet
De ziekte van Alzheimer wordt vaak beschreven als een probleem van toxische eiwitophoping in de hersenen, maar even belangrijk is hoe het immuunsysteem op die schade reageert. Deze studie onderzoekt hoe een specifieke tak van het immuunsysteem, aangestuurd door Type I-interferonsignalen, T-cellen naar amyloïde bèta-plaque leidt en de hersenontsteking in de loop van de tijd herstructureert. Inzicht in dit verschuivende immuunchoreografie kan helpen verklaren waarom hersenschade in latere ziektefasen versnelt en kan wijzen op behandelingen met een beter tijdvenster.
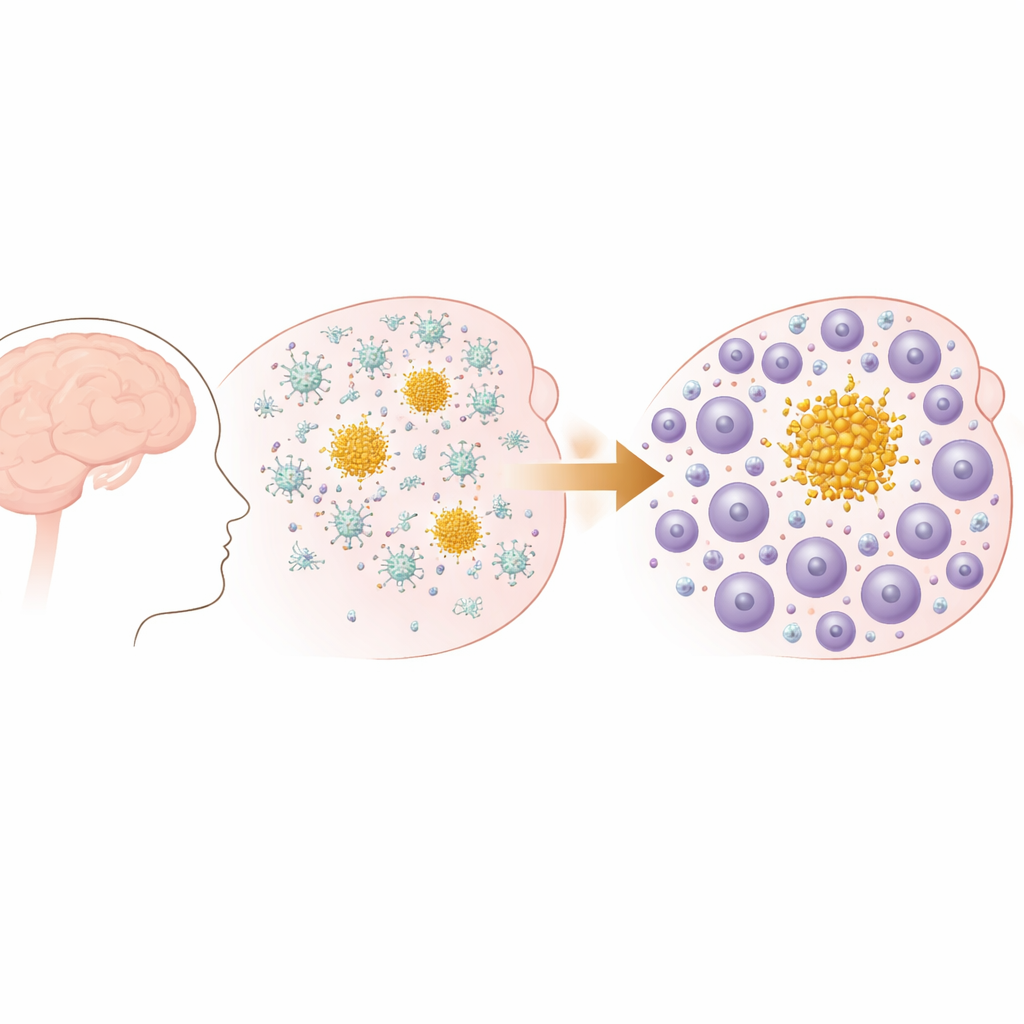
Van vroege plaques naar een veranderend immuencast
De onderzoekers gebruikten een muismodel dat progressieve amyloïde bèta-plaques in de hersenen ontwikkelt, vergelijkbaar met die bij de ziekte van Alzheimer en cerebrale amyloïde angiopathie. Vroeg in het leven vormen deze muizen kleine afzettingen in de buitenlagen van de hersenen, die later uitspreiden en in aantal toenemen, vooral in geheugen-gerelateerde gebieden. Gedragstests bevestigden dat naarmate plaques zich ophoopten met de leeftijd, de muizen meetbare achteruitgang in alledaagse functies ontwikkelden, zoals het nestelen, wat lijkt op het geleidelijke functieverlies bij menselijke dementie. Belangrijk is dat dit model amyloïde plaques heeft maar geen tangelpathologie, waardoor het team zich specifiek kon richten op hoe het immuunsysteem reageert op amyloïde-ophoping.
Wanneer hersenbeschermers wijken voor binnenvallende voetvolk
In eerste instantie wordt de immuunreactie op plaques gedomineerd door microglia, de residente immuuncellen van de hersenen. Met single-cell RNA-sequencing lieten de auteurs zien dat deze microglia in de vroege ziekte speciale, ziektegeassocieerde toestanden aannemen en genen activeren die betrokken zijn bij het opnemen van afval en het verwerken van lipiden. Naarmate de ziekte echter vordert, verschuift het immuunlandschap. Het aantal T-cellen in de hersenen, met name CD8-T-cellen, neemt sterk toe, en routes gerelateerd aan lymfocytactivatie en -beweging worden prominenter. Ruimtelijke analyses bevestigden dat dit geen willekeurige invasie is: T-cellen klonteren dicht rond amyloïde plaques in hersenweefsel, met name rond grote 'parenchymale' plaques in plaats van vaatgebonden plaques, en hun aantallen stijgen gelijktijdig met de plaquebelasting.
Een gespecialiseerde T-celsubset die versterking inroept
Bij nadere beschouwing identificeerde het team een onderscheidende subset van CD8-T-cellen die een reeks genen activeert die normaal door Type I-interferons worden aangestuurd, een familie van antivirale en auto-immuun signaleringsmoleculen. Deze 'interferon-gestimuleerde' T-cellen worden vooral talrijk in de late ziekte en worden nabij plaques gevonden. Ze produceren de chemokine CXCL10, een klein eiwitsignaal dat bindt aan de receptor CXCR3 op andere T-cellen. Ruimtelijke transcriptomica toonde aan dat zowel interferon-responsieve genen als CXCL10 sterk verrijkt zijn in plaque-omgevingen, en dat CXCL10-producerende T-cellen gepositioneerd zijn om invloed uit te oefenen op andere nabije immuuncellen. Laboratoriummigratie-experimenten bevestigden dat T-cellen naar CXCL10-signalen toe bewegen en dat het uitschakelen van CXCR3 hun vermogen om deze signalen te volgen scherp vermindert, wat een model ondersteunt waarbij plaque-geassocieerde, interferon-gedreven T-cellen helpen extra T-cellen naar de hersenen te lokken.
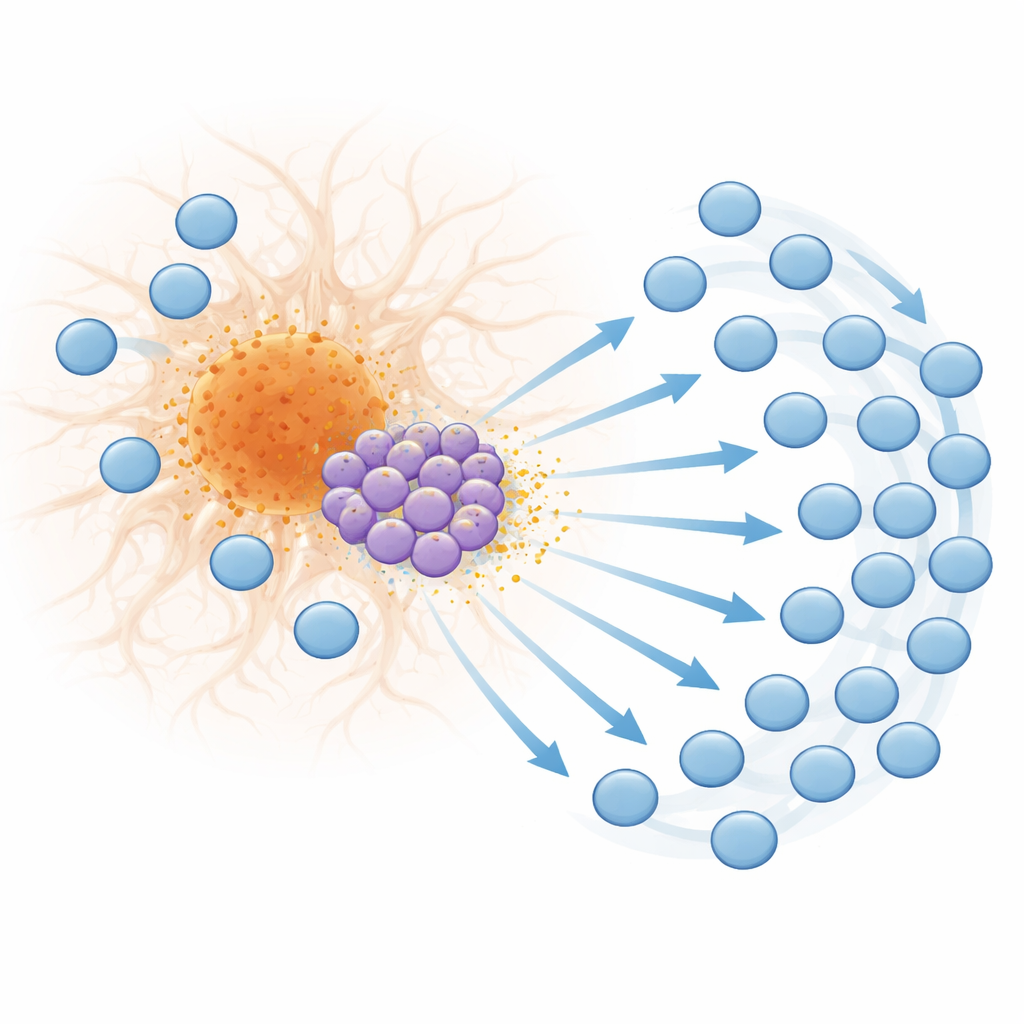
Van activatie naar uitputting aan de rand van de plaque
De toestroom van T-cellen is niet alleen numeriek; ook kwalitatief verandert er veel. In de late ziekte tonen veel CD8-T-cellen rond plaques markers van sterke activatie, cytotoxisch potentieel en klonale expansie—tekens dat ze herhaaldelijk op specifieke triggers reageren. Tegelijkertijd beginnen deze cellen kenmerken van uitputting te vertonen, een toestand waarin chronisch gestimuleerde T-cellen effectiviteit verliezen en remmende moleculen zoals PD-1 tot expressie brengen. Ruimtelijke kaartlegging onthulde dat deze uitgeputte T-cellen zich precies ophopen aan de rand van plaques, wat suggereert dat intense, aanhoudende stimulatie door plaque-geassocieerde signalen hen in een afgeleefde toestand drijft. Vergelijkbare patronen van interferon-responsieve genen, CXCL10, T-celactivatiemarkers en PD-1 werden nabij plaques gevonden in menselijk Alzheimer-hersenweefsel, wat aangeeft dat dit muis-afgeleide mechanisme waarschijnlijk relevant is voor mensen.
Wat dit betekent voor toekomstige Alzheimer-behandelingen
Samengevat schetst de studie een time-lapse beeld van hersenontsteking bij amyloïdeziekte: in het begin domineren microglia de respons, maar naarmate plaques groeien en aanhouden, neemt een gespecialiseerde subset van CD8-T-cellen het over als de belangrijkste aanjager van Type I-interferonsignalering en T-celrecruitment. Deze evoluerende immuunreactie kan bijdragen aan voortdurende zenuwcelbeschadiging en kan interageren met antilichaamgebaseerde behandelingen die plaques verwijderen, mogelijk invloed uitoefenen op bijwerkingen gerelateerd aan vasculaire ontsteking. Voor een algemeen publiek is de kernboodschap dat bij de ziekte van Alzheimer niet alleen de plaques zelf van belang zijn, maar ook hoe — en wanneer — het immuunsysteem erop reageert. Het gericht remmen van interferonroutes of de CXCL10–CXCR3-signaleringsas in het juiste ziekte stadium kan helpen schadelijke ontsteking te kalmeren zonder de verdediging van de hersenen volledig uit te schakelen.
Bronvermelding: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Trefwoorden: Ziekte van Alzheimer, amyloïde bèta, T-cellen, neuro-inflammatie, interferon-signalering