Clear Sky Science · it
L’interferone di tipo I guida le risposte dei linfociti T verso l’amiloide beta nel sistema nervoso centrale
Perché la risposta immunitaria del cervello alle placche è importante
Il morbo di Alzheimer è spesso descritto come un problema di accumulo di proteine tossiche nel cervello, ma una parte altrettanto importante della storia è come il sistema immunitario reagisce a quel danno. Questo studio esplora come un ramo specifico del sistema immunitario, guidato dai segnali dell’interferone di tipo I, orienti i linfociti T verso le placche di amiloide beta e rimodelli l’infiammazione cerebrale nel tempo. Comprendere questa coreografia immunitaria in evoluzione può aiutare a spiegare perché il danno cerebrale accelera nelle fasi avanzate della malattia e potrebbe indicare trattamenti meglio temporizzati.
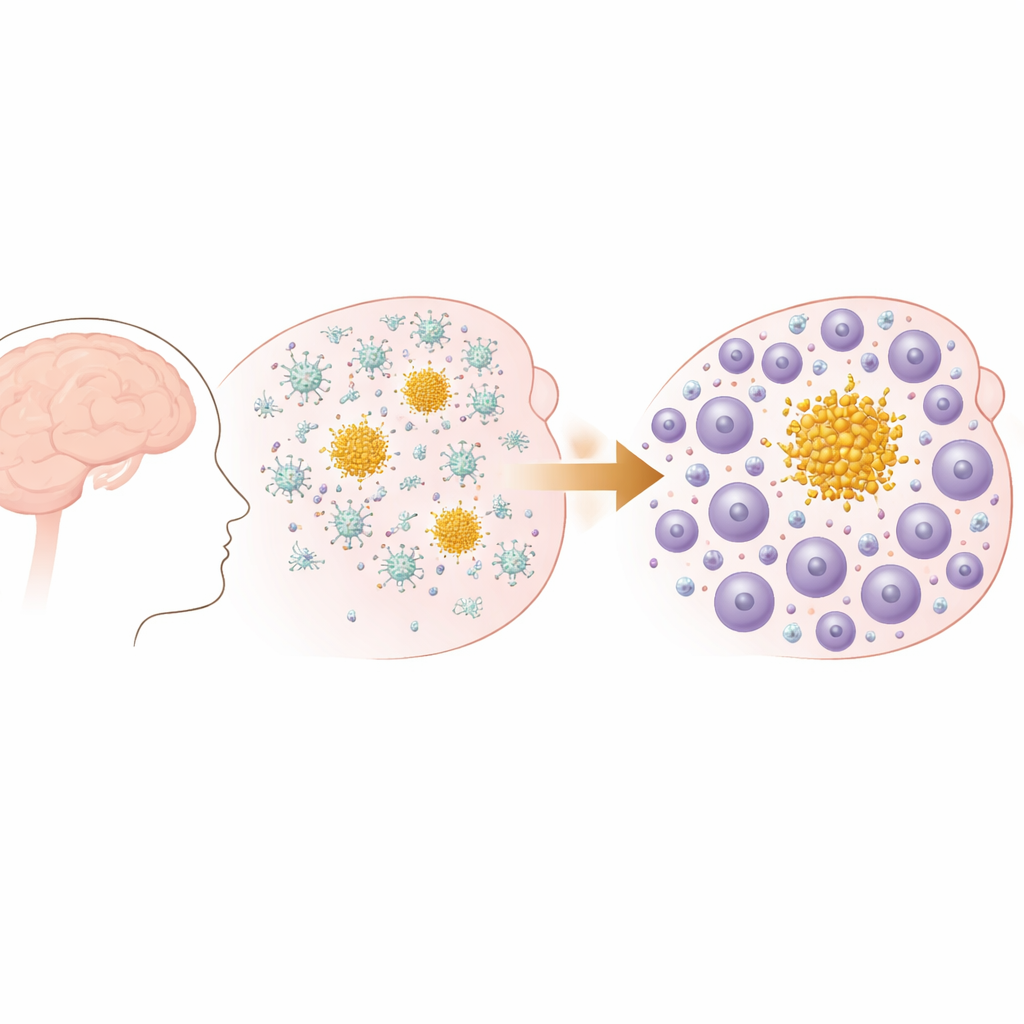
Dalle placche iniziali a un cast immunitario che cambia
I ricercatori hanno utilizzato un modello murino che sviluppa progressivamente placche di amiloide beta nel cervello, simili a quelle osservate nel morbo di Alzheimer e nell’angiopatia amiloide cerebrale. Nelle prime fasi di vita questi topi formano piccoli depositi negli strati esterni del cervello, che poi si diffondono e aumentano di numero, specialmente nelle regioni legate alla memoria. Test comportamentali hanno confermato che con l’accumulo delle placche i topi manifestano declini misurabili nelle funzioni quotidiane come il costruire il nido, rispecchiando il tipo di perdita funzionale graduale osservata nella demenza umana. È importante sottolineare che questo modello presenta placche amiloidi ma non patologia da grovigli, permettendo al gruppo di focalizzarsi su come il sistema immunitario risponde specificamente all’accumulo di amiloide.
Quando le guardie cerebrali lasciano spazio a soldati invasori
Inizialmente la risposta immunitaria alle placche è dominata dalle microglia, le cellule immunitarie residenti del cervello. Utilizzando il sequenziamento dell’RNA a singola cellula, gli autori hanno mostrato che nelle fasi iniziali della malattia queste microglia assumono stati associati alla patologia e aumentano l’espressione di geni legati alla fagocitosi e al metabolismo lipidico. Ma con l’avanzare della malattia il panorama immunitario cambia. Il numero di linfociti T nel cervello, in particolare i CD8, cresce notevolmente, e diventano più evidenti le vie biologiche relative all’attivazione e alla migrazione dei linfociti. Analisi spaziali hanno confermato che non si tratta di un’invasione casuale: i linfociti T si raggruppano strettamente attorno alle placche di amiloide nel tessuto cerebrale, in particolare attorno a grandi placche “parenchimali” piuttosto che a quelle nei vasi sanguigni, e il loro numero aumenta in parallelo con il carico di placche.
Un sottogruppo specializzato di linfociti T che chiama rinforzi
Analizzando più da vicino questi linfociti T, il team ha identificato un sottogruppo distinto di CD8 che attiva un insieme di geni normalmente indotti dagli interferoni di tipo I, una famiglia di molecole segnalatrici antivirali e coinvolte in patologie autoimmuni. Questi linfociti T “stimolati dall’interferone” diventano particolarmente abbondanti nelle fasi avanzate della malattia e si trovano in prossimità delle placche. Producono la chemochina CXCL10, un piccolo segnale proteico che si lega al recettore CXCR3 su altri linfociti T. La trascrittomica spaziale ha mostrato che sia i geni responsivi all’interferone sia CXCL10 sono fortemente arricchiti nei dintorni delle placche, e che i linfociti T produttori di CXCL10 sono posizionati per influenzare altre cellule immunitarie vicine. Esperimenti di migrazione in laboratorio hanno confermato che i linfociti T si muovono verso segnali di CXCL10 e che disattivare CXCR3 riduce nettamente la loro capacità di seguire questi segnali, a supporto di un modello in cui i linfociti T associati alle placche e guidati dall’interferone aiutano ad attirare ulteriori linfociti nel cervello.
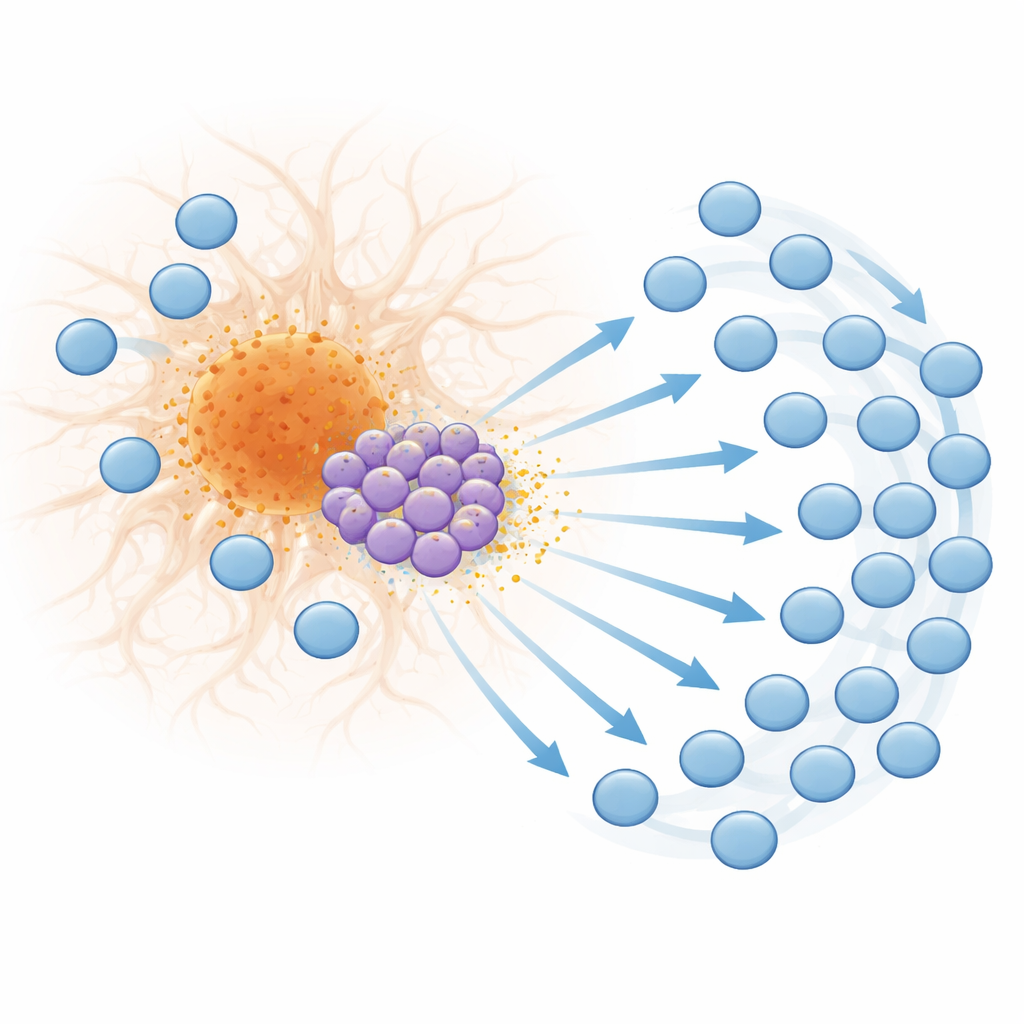
Dall’attivazione all’esaurimento al bordo della placca
L’afflusso di linfociti T non è solo numerico; cambia anche in qualità. Nelle fasi avanzate della malattia molti CD8 intorno alle placche mostrano marcatori di forte attivazione, potenziale citotossico ed espansione clonale—segni che rispondono ripetutamente a stimoli specifici. Allo stesso tempo queste cellule cominciano a esprimere i segni distintivi dell’esaurimento, uno stato in cui i linfociti T stimolati cronicamente perdono efficacia ed esprimono molecole inibitorie come PD-1. La mappatura spaziale ha rivelato che questi linfociti esausti si accumulano proprio al margine delle placche, suggerendo che uno stimolo intenso e persistente da segnali associati alla placca li conduca a uno stato di logoramento. Schemi simili di geni responsivi all’interferone, CXCL10, marcatori di attivazione dei linfociti T e PD-1 sono stati riscontrati vicino alle placche nel tessuto cerebrale umano affetto da Alzheimer, indicando che questo meccanismo osservato nei topi è probabilmente rilevante anche per le persone.
Cosa significa tutto questo per i futuri trattamenti dell’Alzheimer
Nel complesso, lo studio descrive un quadro in time-lapse dell’infiammazione cerebrale nella malattia da amiloide: all’inizio le microglia dominano la risposta, ma mano a mano che le placche crescono e persistono, un sottogruppo specializzato di CD8 assume il ruolo di principale promotore della segnalazione dell’interferone di tipo I e del reclutamento dei linfociti T. Questa risposta immunitaria in evoluzione può contribuire al danno neuronale continuo e potrebbe interagire con terapie a base di anticorpi che rimuovono le placche, influenzando potenzialmente gli effetti collaterali legati all’infiammazione vascolare. Per il lettore generale, il messaggio chiave è che nel morbo di Alzheimer non sono importanti solo le placche in sé, ma anche come — e quando — il sistema immunitario vi risponde. Mirare alle vie dell’interferone o all’asse di segnalazione CXCL10–CXCR3 nella fase giusta della malattia potrebbe contribuire a placare un’infiammazione dannosa senza spegnere del tutto le difese cerebrali.
Citazione: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Parole chiave: Morbo di Alzheimer, amiloide beta, linfociti T, neuroinfiammazione, segnalazione dell’interferone