Clear Sky Science · pt
Interferon tipo I direciona respostas de células T ao beta-amiloide no sistema nervoso central
Por que a resposta imune do cérebro às placas importa
A doença de Alzheimer costuma ser descrita como um problema de acúmulo tóxico de proteínas no cérebro, mas uma parte igualmente importante da história é como o sistema imunológico reage a esse dano. Este estudo investiga como um ramo específico do sistema imune, dirigido por sinais de interferon tipo I, ajuda a orientar células T em direção às placas de beta-amiloide e remodela a inflamação cerebral ao longo do tempo. Entender essa coreografia imune em mudança pode ajudar a explicar por que o dano cerebral acelera em estágios avançados da doença e pode apontar para tratamentos melhor cronometrados.
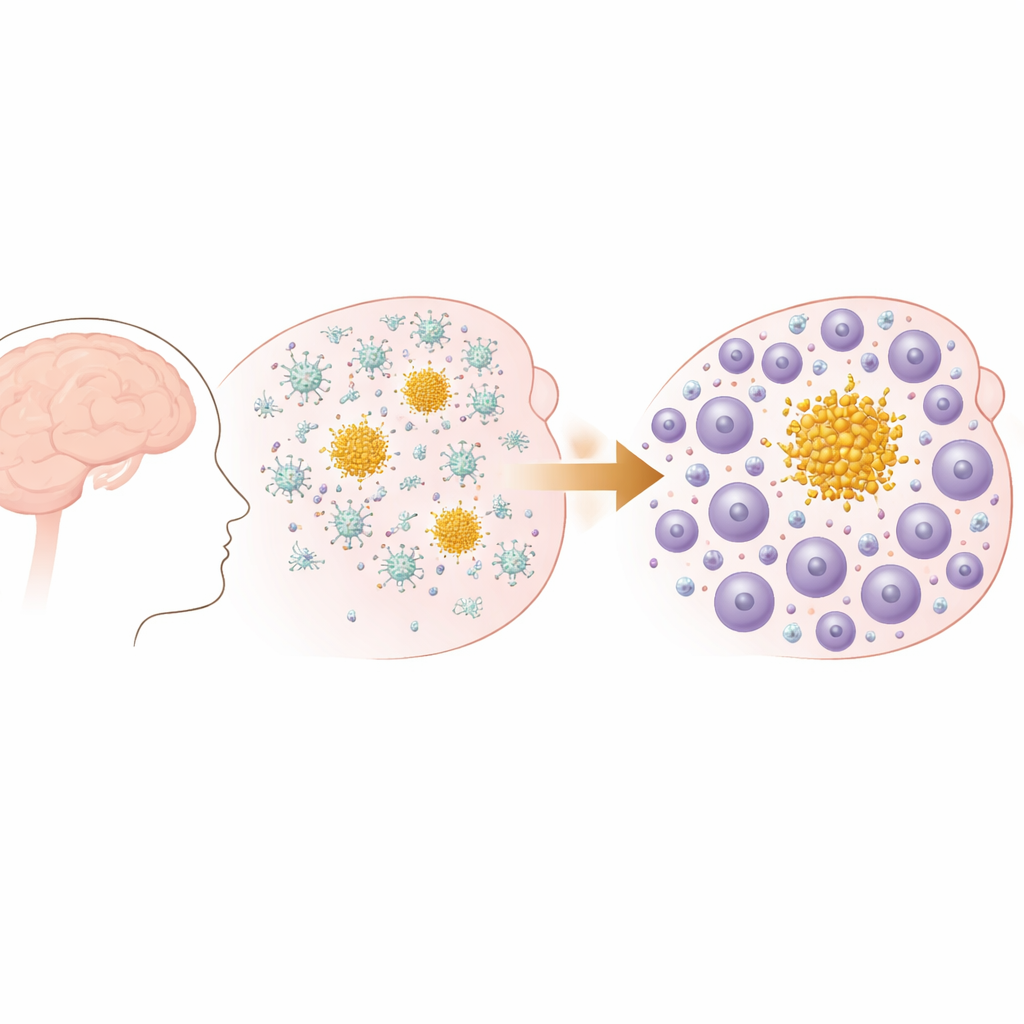
Das placas iniciais a um elenco imune em transformação
Os pesquisadores usaram um modelo de camundongo que desenvolve placas progressivas de beta-amiloide no cérebro, semelhantes às observadas na doença de Alzheimer e na angiopatia amiloide cerebral. No início da vida, esses animais formam pequenos depósitos nas camadas externas do cérebro, que depois se espalham e aumentam em número, especialmente em regiões relacionadas à memória. Testes comportamentais confirmaram que, à medida que as placas se acumulam com a idade, os camundongos apresentam declínios mensuráveis em funções cotidianas como a construção de ninhos, espelhando o tipo de perda funcional gradual vista na demência humana. Importante: esse modelo tem placas amiloides, mas não apresenta patologia de emaranhados, permitindo à equipe focar em como o sistema imune responde especificamente ao acúmulo de amiloide.
Quando os guardiões do cérebro dão lugar a soldados invasores
No começo, a resposta imune às placas é dominada pelos micróglias, as células imunes residentes do cérebro. Usando sequenciamento de RNA de célula única, os autores mostraram que, no estágio inicial da doença, essas micróglias assumem estados associados à doença e aumentam a expressão de genes ligados à fagocitose de detritos e ao manejo de lipídios. Mas, à medida que a doença avança, o cenário imune muda. O número de células T no cérebro, especialmente as CD8, cresce acentuadamente, e vias relacionadas à ativação e migração de linfócitos tornam-se mais proeminentes. Análises espaciais confirmaram que não se trata de uma invasão aleatória: as células T se agrupam ao redor das placas de beta-amiloide no tecido cerebral, particularmente ao redor de grandes placas “parenquimatosas” em vez daquelas em vasos sanguíneos, e seus números aumentam em consonância com a carga de placas.
Um subconjunto especializado de células T que chama reforços
Ao observar mais de perto essas células T, a equipe identificou um subconjunto distinto de CD8 que ativa um conjunto de genes normalmente desencadeados por interferons tipo I, uma família de moléculas sinalizadoras envolvidas em respostas antivirais e autoimunes. Essas células T “estimuladas por interferon” tornam-se especialmente abundantes em estágios tardios da doença e são encontradas perto das placas. Elas produzem a quimiocina CXCL10, uma pequena proteína sinalizadora que se liga ao receptor CXCR3 em outras células T. A transcriptômica espacial mostrou que tanto genes responsivos ao interferon quanto CXCL10 estão fortemente enriquecidos nas vizinhanças das placas, e que as células T produtoras de CXCL10 estão posicionadas para influenciar outras células imunes próximas. Experimentos de migração em laboratório confirmaram que células T se movem em direção a sinais de CXCL10 e que desabilitar CXCR3 reduz fortemente sua capacidade de seguir esses sinais, apoiando um modelo no qual células T associadas às placas e dirigidas por interferon ajudam a atrair mais células T para o cérebro.
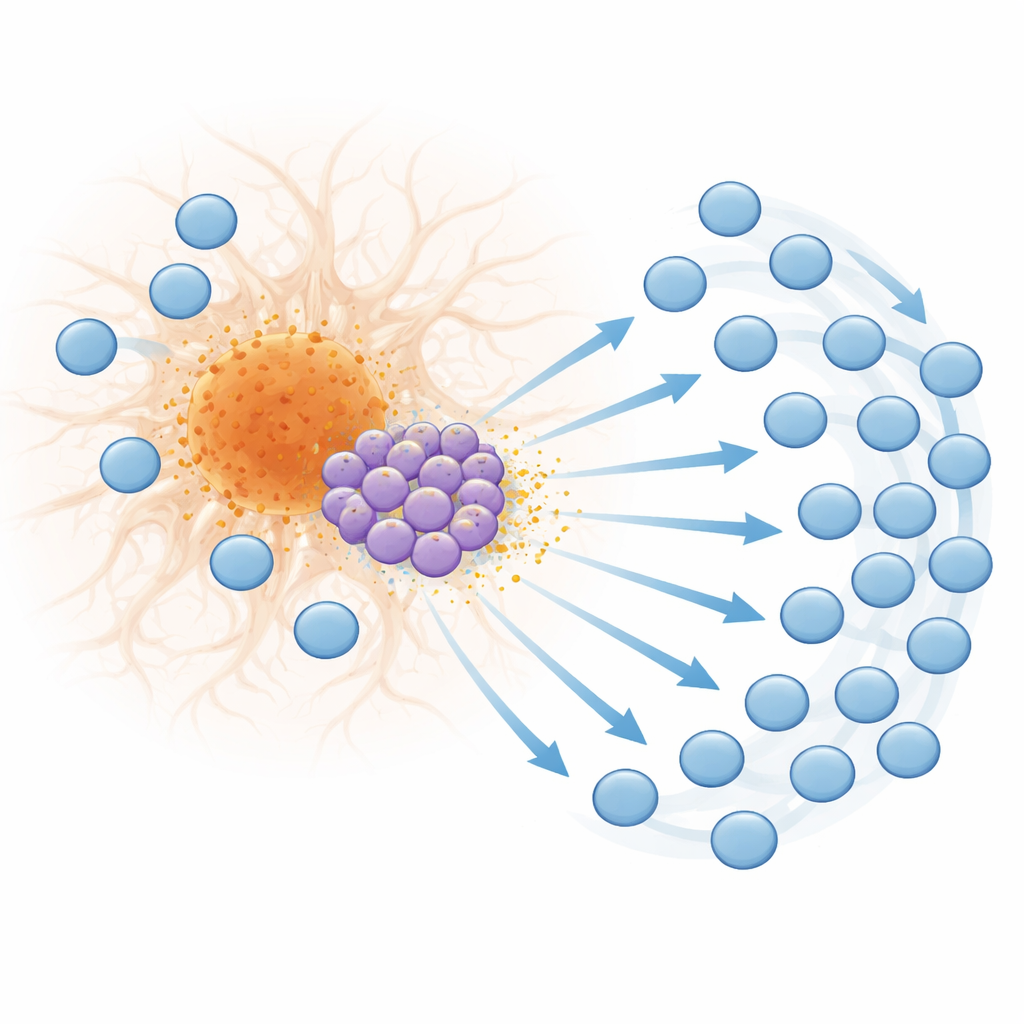
Da ativação ao esgotamento na borda da placa
O afluxo de células T não é apenas numérico; também muda em qualidade. Em doença em estágio tardio, muitas células T CD8 ao redor das placas exibem marcadores de alta ativação, potencial citotóxico e expansão clonal — sinais de que estão respondendo repetidamente a gatilhos específicos. Ao mesmo tempo, essas células começam a apresentar características de esgotamento, um estado em que células T cronicamente estimuladas perdem eficácia e expressam moléculas inibitórias como PD-1. O mapeamento espacial revelou que essas células T exauridas se acumulam exatamente na borda das placas, sugerindo que a estimulação intensa e contínua por sinais associados às placas as leva a um estado de desgaste. Padrões semelhantes de genes responsivos ao interferon, CXCL10, marcadores de ativação de células T e PD-1 foram encontrados perto de placas em tecido cerebral de humanos com Alzheimer, indicando que esse mecanismo observado nos camundongos provavelmente é relevante para pessoas.
O que isso significa para tratamentos futuros da doença de Alzheimer
No conjunto, o estudo traça uma imagem em lapso de tempo da inflamação cerebral na doença amiloide: no início, as micróglias dominam a resposta, mas, à medida que as placas crescem e persistem, um subconjunto especializado de células T CD8 assume como principal motor da sinalização por interferon tipo I e do recrutamento de células T. Essa resposta imune em evolução pode contribuir para o dano contínuo de neurônios e pode interagir com tratamentos baseados em anticorpos que removem placas, potencialmente influenciando efeitos colaterais ligados à inflamação vascular. Para um leitor geral, a mensagem-chave é que, na doença de Alzheimer, não são apenas as placas que importam, mas também como — e quando — o sistema imunológico responde a elas. Alvejar vias de interferon ou o eixo de sinalização CXCL10–CXCR3 no estágio correto da doença poderia ajudar a acalmar a inflamação prejudicial sem silenciar completamente as defesas do cérebro.
Citação: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Palavras-chave: Doença de Alzheimer, beta-amiloide, células T, neuroinflamação, sinalização por interferon