Clear Sky Science · ru
Интерферон типа I направляет T‑клеточные ответы на амилоид бета в центральной нервной системе
Почему имеет значение иммунный ответ мозга на бляшки
Болезнь Альцгеймера часто описывают как проблему накопления токсичных белков в мозге, но не менее важна и реакция иммунной системы на это повреждение. В этом исследовании рассматривается, как конкретное ответвление иммунитета, управляемое сигналами интерферона типа I, направляет T‑клетки к амилоидным бляшкам и со временем перестраивает воспалительную среду мозга. Понимание этой меняющейся иммунной «хореографии» может помочь объяснить, почему повреждение мозга ускоряется на поздних стадиях болезни, и указать на более подходящее по времени лечение.
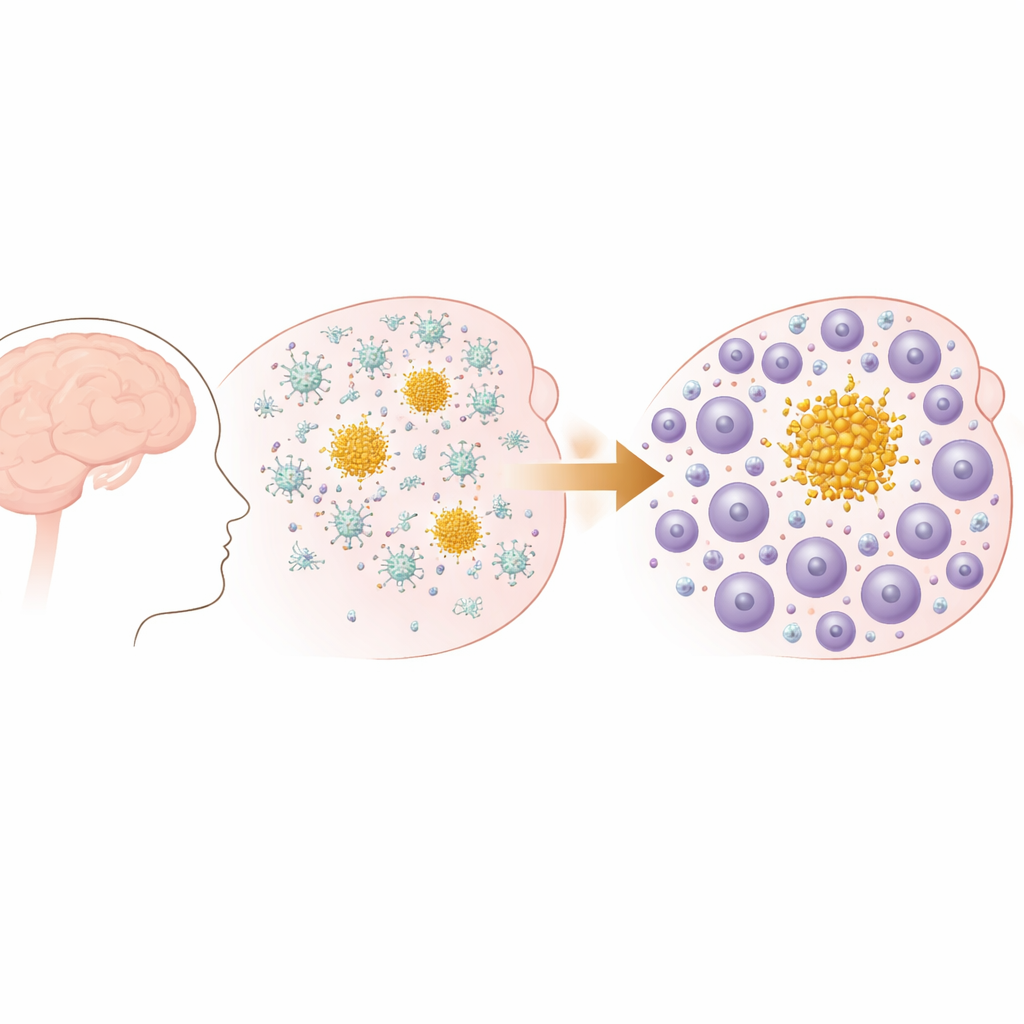
От ранних бляшек к меняющемуся иммунному ансамблю
Исследователи использовали модель мыши, у которой в мозге прогрессивно развиваются амилоидные бляшки, похожие на те, что наблюдаются при болезни Альцгеймера и церебральной амилоидной ангиопатии. Ранним этапом у этих мышей формируются небольшие отложения в наружных слоях мозга, которые затем распространяются и увеличиваются в числе, особенно в областях, связанных с памятью. Поведенческие тесты подтвердили, что по мере накопления бляшек у мышей возникают измеримые нарушения повседневных функций, таких как строительство гнезда, что отражает постепенную утрату функций, наблюдаемую при деменции у людей. Важно, что в этой модели есть амилоидные бляшки, но отсутствует патология нейрофибриллярных клубков, что позволило авторам сосредоточиться на том, как иммунная система отвечает именно на накопление амилоида.
Когда защитники мозга уступают место вторгающимся бойцам
Сначала ответ на бляшки доминируют микроглия — резидентные иммунные клетки мозга. С помощью одноклеточного РНК‑секвенирования авторы показали, что на ранних стадиях болезни микроглия переходит в особые состояния, связанные с заболеванием, и усиливает экспрессию генов, отвечающих за фагоцитоз и переработку липидов. Но по мере прогрессирования болезни иммунный ландшафт меняется. Число T‑клеток в мозге, особенно CD8+ T‑клеток, резко растёт, и пути, связанные с активацией и миграцией лимфоцитов, становятся более выраженными. Пространственные анализы подтвердили, что это не случайное вторжение: T‑клетки плотно скапливаются вокруг амилоидных бляшек в тканях мозга, особенно вокруг крупных паренхимальных бляшек, а не сосудистых отложений, и их число увеличивается пропорционально нагрузке бляшек.
Специализированный подтип T‑клеток, который призывает подкрепления
Более тщательный анализ T‑клеток выявил отдельный подтип CD8+ клеток, который включает набор генов, обычно индуцируемых интерферонами типа I — семейством сигналов, связанных с противовирусным и аутоиммунным ответом. Эти «интерферон-стимулированные» T‑клетки становятся особенно многочисленными на поздних стадиях болезни и локализуются рядом с бляшками. Они продуцируют хемокин CXCL10 — небольшой сигнальный белок, который связывается с рецептором CXCR3 на других T‑клетках. Пространственная транскриптомика показала, что гены, ответственные на интерферон, и CXCL10 сильно обогащены в окрестностях бляшек, а CXCL10‑производящие T‑клетки расположены так, чтобы влиять на соседние иммунные клетки. Лабораторные эксперименты по миграции подтвердили, что T‑клетки движутся к сигналам CXCL10 и что отключение CXCR3 резко уменьшает их способность следовать этим сигналам, что поддерживает модель, в которой интерферон‑зависимые T‑клетки, ассоциированные с бляшками, помогают привлекать дополнительные T‑клетки в мозг.
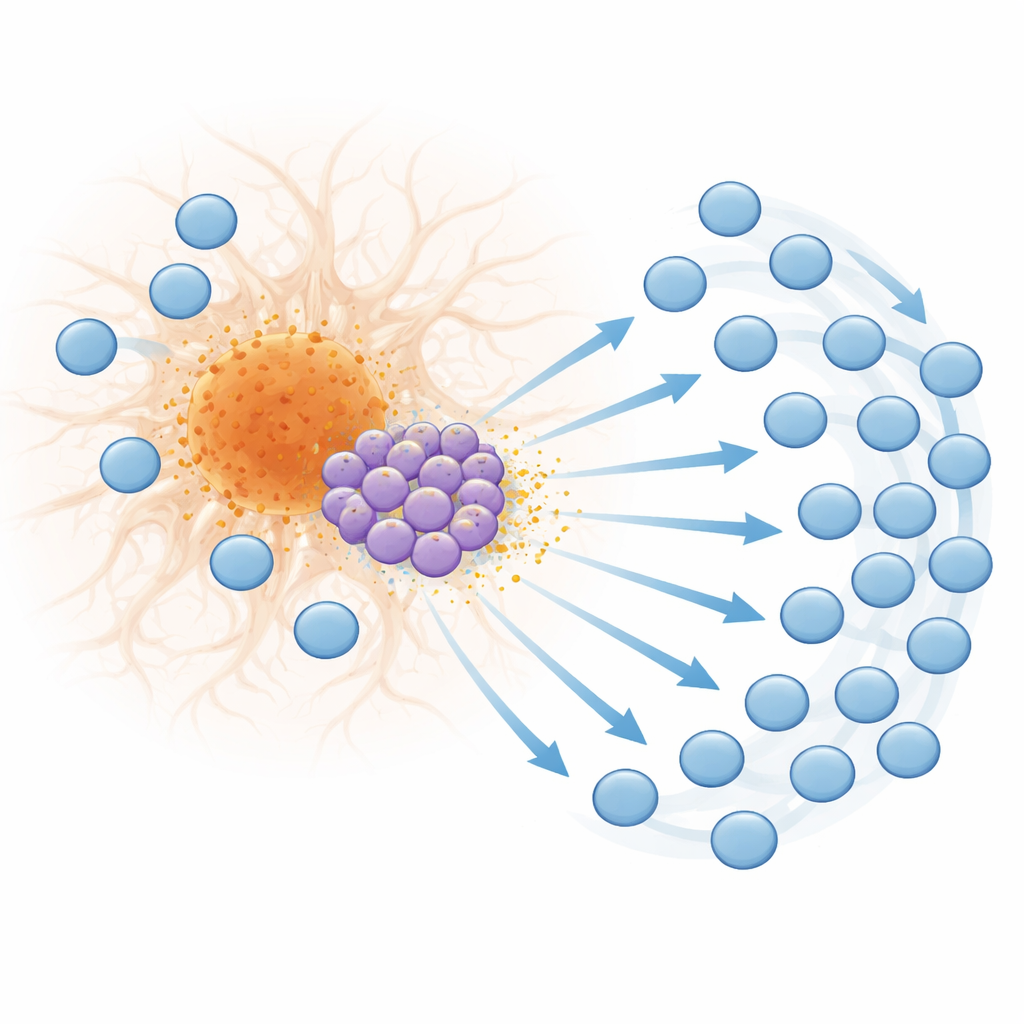
От активации до истощения на краю бляшки
Приток T‑клеток меняет не только их количество, но и характер. На поздних стадиях болезни многие CD8+ T‑клетки вокруг бляшек демонстрируют маркеры высокой активации, цитотоксический потенциал и клональное расширение — признаки того, что они неоднократно реагируют на определённые стимулы. В то же время эти клетки начинают проявлять признаки истощения — состояния, при котором хронически стимулированные T‑клетки теряют эффективность и экспрессируют ингибирующие молекулы, такие как PD‑1. Пространственное картирование показало, что эти «истощённые» T‑клетки накапливаются прямо на границе бляшек, что указывает на то, что интенсивная и продолжительная стимуляция сигналами, связанными с бляшками, ввергает их в утомлённое состояние. Похожие паттерны интерферон-ответных генов, CXCL10, маркеров активации T‑клеток и PD‑1 были обнаружены рядом с бляшками в тканях мозга людей с болезнью Альцгеймера, что говорит о том, что описанный на мышиной модели механизм, вероятно, имеет отношение и к людям.
Что это значит для будущих терапий при болезни Альцгеймера
В целом исследование рисует покадровую картину воспаления мозга при амилоидной патологии: на ранних стадиях ответ доминируют микроглия, но по мере роста и сохраняющейся присутствия бляшек специализированный подтип CD8+ T‑клеток становится основным драйвером сигнализации интерферона типа I и рекрутирования T‑клеток. Такая эволюция иммунного ответа может способствовать продолжающемуся повреждению нейронов и взаимодействовать с антителозависимыми терапиями, удаляющими бляшки, потенциально влияя на побочные эффекты, связанные с сосудистым воспалением. Для широкой аудитории главный вывод таков: при болезни Альцгеймера важны не только сами бляшки, но и то, как — и когда — на них реагирует иммунная система. Таргетирование интерфероновых путей или оси сигнализации CXCL10–CXCR3 на подходящей стадии болезни могло бы помочь смягчить вредное воспаление, не подавляя полностью защитные функции мозга.
Цитирование: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Ключевые слова: Болезнь Альцгеймера, амилоид бета, T‑клетки, нейровоспаление, сигнализация интерферона