Clear Sky Science · tr
Tip I interferonü santral sinir sisteminde amiloid beta’ya yönelik T hücresi yanıtlarını yönlendiriyor
Plaklara Karşı Beynin Bağışıklık Yanıtının Neden Önemli Olduğu
Alzheimer hastalığı sıklıkla beyinde toksik protein birikimi sorunu olarak tanımlanır, ancak hikâyenin eşit derecede önemli bir yanı da bağışıklık sisteminin bu hasara nasıl yanıt verdiğidir. Bu çalışma, Tip I interferon sinyalleriyle yönlendirilen bağışıklığın belirli bir kolunun, T hücrelerini amiloid beta plaklarına doğru nasıl yönlendirdiğini ve zaman içinde beyin iltihabını nasıl yeniden şekillendirdiğini araştırıyor. Bu değişen bağışıklık koreografisini anlamak, hastalığın ileri evrelerinde neden beyin hasarının hızlandığını açıklamaya yardımcı olabilir ve daha iyi zamanlanmış tedavilere işaret edebilir.
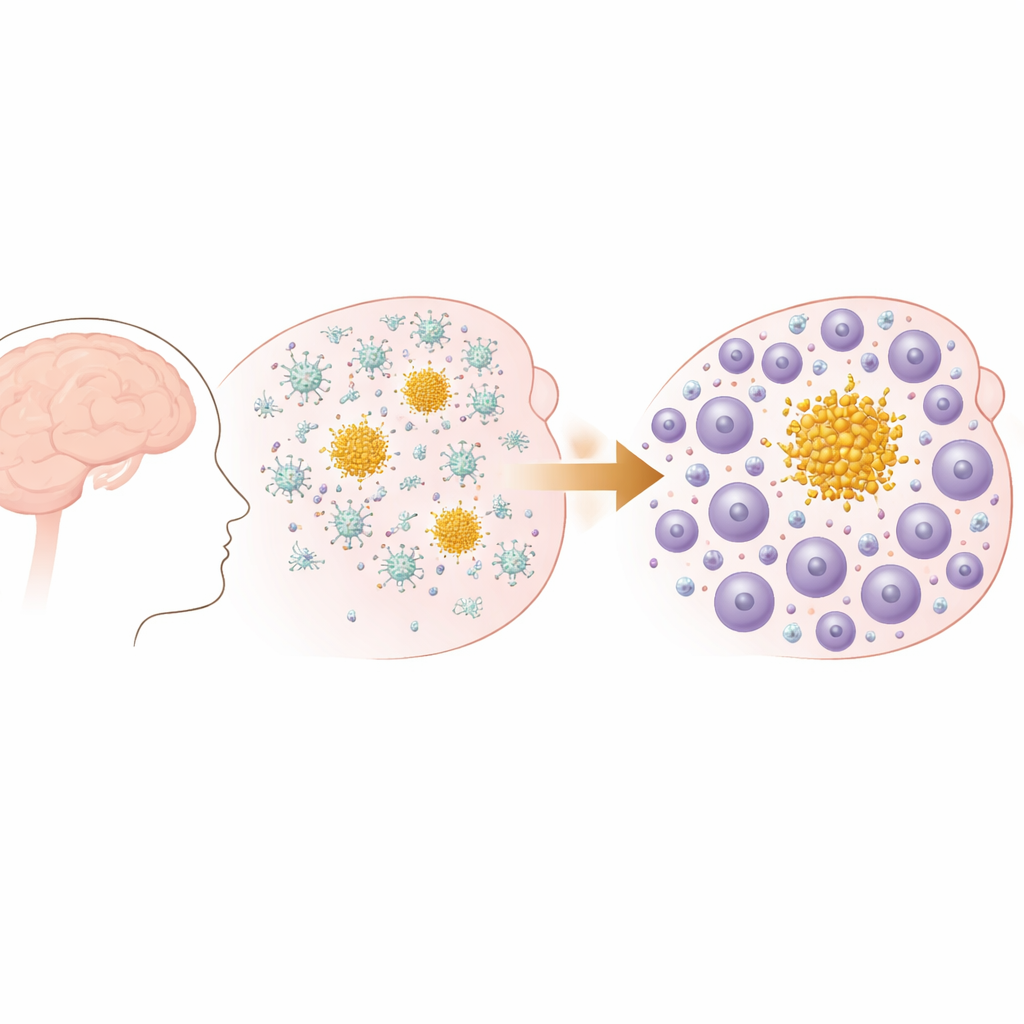
Erken Plaklardan Değişen Bir Bağışıklık Kadrosuna
Araştırmacılar, Alzheimer hastalığında ve serebral amiloid anjiyopatide görülenlere benzer şekilde beyinde ilerleyici amiloid beta plakları geliştiren bir fare modeli kullandılar. Erken dönemde bu fareler beynin dış katmanlarında küçük birikimler oluşturur; daha sonra bunlar yayılır ve özellikle hafıza ile ilişkili bölgelerde sayıca artar. Davranış testleri, plaklar yaşla birlikte biriktikçe farelerin yuva yapma gibi günlük işlevlerde ölçülebilir düşüşler geliştirdiğini doğruladı; bu, insan demansında görülen kademeli fonksiyon kaybını yansıtır. Önemli olarak, bu modelde tangle patolojisi yoktur; bu, ekibin bağışıklık sisteminin özellikle amiloid birikimine nasıl yanıt verdiğine odaklanmasını sağlar.
Beyin Bekçilerinin Yerini İşgalci Tüfekliler Aldığında
İlk etapta plaklara karşı bağışıklık yanıtı, beynin yerleşik bağışıklık hücreleri olan mikroglialar tarafından domine edilir. Tek hücreli RNA dizilemesi kullanarak yazarlar, erken hastalıkta bu mikrogliaların hastalığa özgü özel durumlar benimsediğini ve enkazı yutma ile lipid yönetimiyle ilişkili genleri artırdığını gösterdiler. Ancak hastalık ilerledikçe bağışıklık ortamı değişir. Beyindeki T hücresi sayısı, özellikle CD8 T hücreleri, keskin bir şekilde artar ve lenfosit aktivasyonu ve göçüyle ilişkili yollar daha belirgin hâle gelir. Mekânsal analizler bunun rastgele bir istila olmadığını doğruladı: T hücreleri beyin dokusunda özellikle büyük “parankimal” plakların etrafında yoğun şekilde kümelenir, damar içindeki plaklara kıyasla ve sayı olarak plak yüküyle paralel artış gösterirler.
Takviye Çağıran Özelleşmiş Bir T Hücresi Alt Kümesi
Bu T hücrelerine yakından baktıklarında ekip, Tip I interferonlar tarafından normalde tetiklenen bir dizi geni açan belirgin bir CD8 T hücresi alt kümesini tanımladı; Tip I interferonlar antiviral ve otoimmün sinyal molekülleridir. Bu “interferon-uyaştırılmış” T hücreleri ileri hastalıkta özellikle bol bulunur ve plakların yakınında yer alır. Bunlar, diğer T hücrelerinde bulunan CXCR3 reseptörüne bağlanan küçük bir protein sinyal olan kemokin CXCL10’u üretirler. Mekânsal transkriptomik veriler, interferon-donanımlı genlerin ve CXCL10’un plak mahallelerinde güçlü şekilde zenginleştiğini ve CXCL10 üreten T hücrelerinin yakınındaki diğer bağışıklık hücrelerini etkileme konumunda olduğunu gösterdi. Laboratuvar göç deneyleri, T hücrelerinin CXCL10 sinyallerine doğru hareket ettiğini ve CXCR3’ü devre dışı bırakmanın bu izleme yeteneğini keskin biçimde azalttığını doğruladı; bu da plakla ilişkili interferon sürüklemeli T hücrelerinin ek T hücrelerini beyne çekmesine yardımcı olduğu modelini destekliyor.
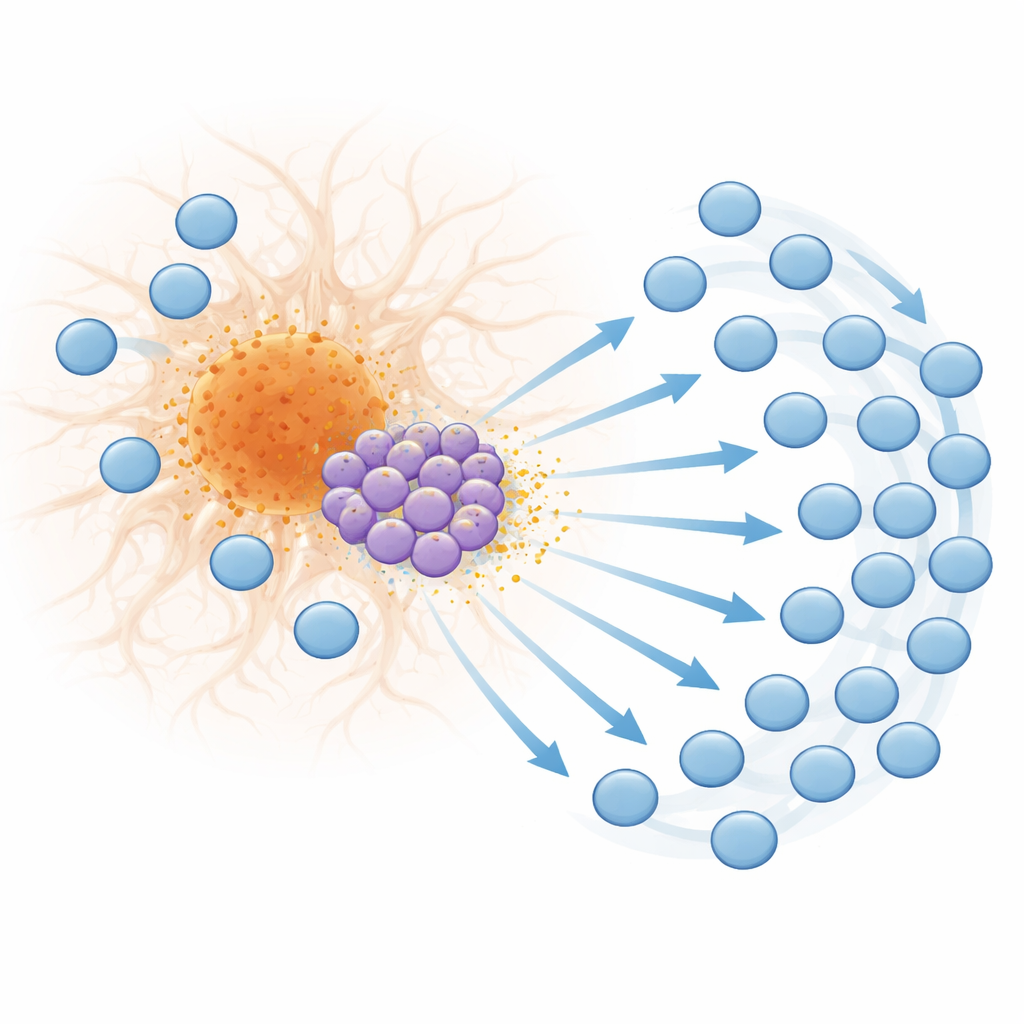
Plak Kenarında Aktivasyondan Tükenmişliğe
T hücrelerinin akını sadece sayı olarak değil, nitelik olarak da değişiklik getirir. Geç evre hastalıkta, plakların etrafındaki birçok CD8 T hücresi yüksek aktivasyon, sitotoksik potansiyel ve klonal genişleme belirteçleri gösterir—bunlar, belirli tetikleyicilere tekrar tekrar yanıt verdiklerinin işaretleridir. Aynı zamanda bu hücreler tükenmişlik belirteçleri taşımaya başlar; kronik uyarılan T hücrelerinin etkinliğini kaybettiği ve PD-1 gibi inhibitör moleküller ifade ettiği bir durum. Mekânsal haritalama, bu tükenmiş T hücrelerin doğrudan plak sınırında biriktiğini ortaya koydu; bu da, plakla ilişkili sinyallerin yoğun, sürekli uyarımının onları yıpranmış bir duruma sürüklediğini düşündürüyor. İnsan Alzheimer beyin dokusunda da plak yakınlarında benzer interferon-yönelimli genler, CXCL10, T hücresi aktivasyon belirteçleri ve PD-1 desenleri bulundu; bu da fare kökenli bu mekanizmanın muhtemelen insanlar için de geçerli olduğunu gösteriyor.
Gelecekteki Alzheimer Tedavileri İçin Ne Anlama Geliyor
Genel olarak çalışma, amiloid hastalığında beyin iltihabının time-lapse (zaman atlamalı) bir resmini çiziyor: erken dönemde mikroglialar yanıtı domine eder, ancak plaklar büyüyüp kalıcı hâle geldikçe, CD8 T hücrelerinin özelleşmiş bir alt kümesi Tip I interferon sinyallemesinin ve T hücresi işe alımının başlıca sürücüsü hâline gelir. Bu evrilen bağışıklık yanıtı sürekli sinir hücresi hasarına katkıda bulunabilir ve plakları uzaklaştıran antikor temelli tedavilerle etkileşime girerek vasküler iltihapla ilişkilendirilen yan etkileri etkileyebilir. Genel okuyucu için kilit mesaj şudur: Alzheimer hastalığında yalnızca plakların kendisi önemli değildir; aynı zamanda bağışıklık sisteminin onlara nasıl—ve ne zaman—yanıt verdiğidir. Interferon yollarını veya CXCL10–CXCR3 sinyal eksenini hastalığın doğru evresinde hedeflemek, beynin savunmasını tamamen susturmadan zararlı iltihabı yatıştırmaya yardımcı olabilir.
Atıf: Michel, J.J., Sanghvi, K., Rosenbauer, J. et al. Type I interferon drives T cell responses to amyloid beta in the central nervous system. Nat Commun 17, 3737 (2026). https://doi.org/10.1038/s41467-026-72262-6
Anahtar kelimeler: Alzheimer hastalığı, amiloid beta, T hücreleri, nöroenflamasyon, interferon sinyalleşmesi