Clear Sky Science · zh
结构分析揭示硫酸盐还原细菌中蛋白酶‑粘附蛋白相互作用及c‑di‑GMP受体调控
黏性细菌为何重要
细菌通常不是以孤立细胞的形式存在,而是以拥挤、粘滑的群体形式生活,称为生物膜。这些群体可以覆盖管道、船体、地下岩石,甚至医疗器械。在像脱硫弧菌(Desulfovibrio vulgaris)这样的硫酸盐还原细菌中,生物膜是一把双刃剑:它们有助于清理受污染的环境,但也会加速金属腐蚀。该研究提出了一个看似简单但影响深远的问题:这些细菌如何决定何时紧紧附着在表面,何时脱落?
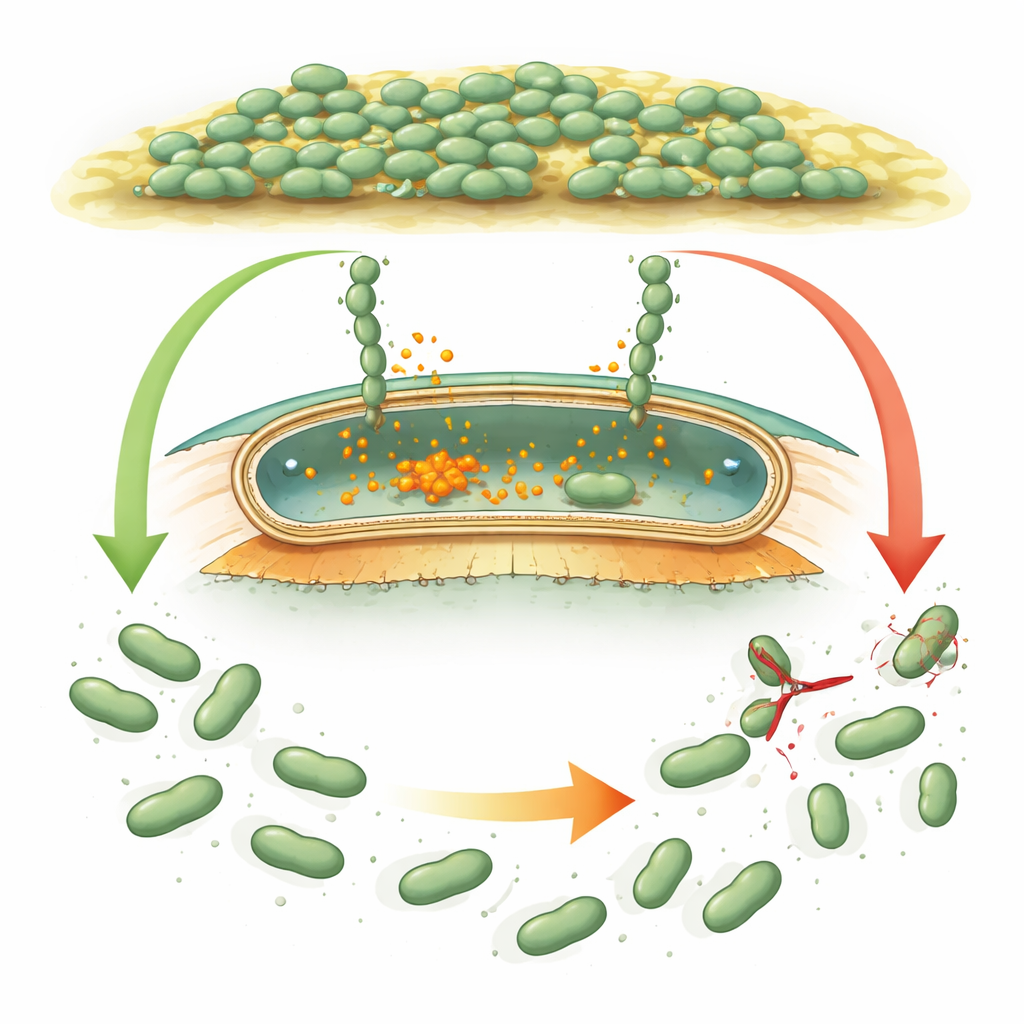
微生物如何抓取与释放
许多细菌使用巨大的“魔术贴式”蛋白——称为粘附蛋白(adhesin)——将细胞粘附到表面或相互之间。在被广泛研究的物种如铜绿假单胞菌中,这些粘附蛋白受一种细胞内化学信号环二鸟苷酸(c‑di‑GMP)的控制:当细菌应形成生物膜时,该信号上升;应解散时则下降。信号高时,粘附蛋白保持锚定在外膜;当信号下降时,一个小型蛋白剪切酶(蛋白酶)在靠近细胞表面的地方切断粘附蛋白,粘性片段随之脱落,帮助细胞分散。脱硫弧菌携带看似相似的遗传工具箱,但其调控蛋白在序列与结构上差异很大,科学家无法判断它是否沿用相同逻辑或采用了全新的策略。
一种专门的分子剪刀
作者首先关注DvhG——脱硫弧菌中负责切割粘附蛋白的蛋白酶版本。通过结构预测和生化测试,他们显示DvhG具有与其他细菌同类蛋白相同的核心折叠和催化机制,并且需要钙才能发挥作用。它在两个大型粘附蛋白上几乎在相同的位置进行精确切割,切点紧跟在使这些蛋白留在外膜中的一段小“滞留”区段之后。有趣的是,研究团队发现DvhG不仅仅识别一段短的靶序列。每个粘附蛋白体积较大的滞留结构与蛋白酶形成广泛接触,构成一个大面积的对接界面,从而提高切割效率。破坏该对接补丁的突变会显著降低DvhG的活性,显示出与相关系统相比额外的一层特异性。
细胞内的信号感受开关
第二个关键分子DvhD位于内膜并伸入细胞内部与膜间空间。研究者解析了DvhD片段的多个三维结构。在细胞外侧,其周质区形成dCache结构域,这是一种常见的感受器构造,常用于结合小分子。在细胞内,DvhD携带HD‑GYP结构域,这个模块通常见于分解环二鸟苷酸的酶。然而在这里,关键的金属结合残基缺失,精细测定表明DvhD并不降解该信号;相反,它与环二鸟苷酸结合得非常紧密。结构快照揭示了两个不同的结合口袋,最多可容纳三分子c‑di‑GMP桥联一对HD‑GYP结构域,并将它们强制置于新的构象,撬开连接至受体其余部分的长螺旋。
从内部信号到表面行为
通过比较“空”态与结合信号态的DvhD,团队揭示了c‑di‑GMP结合如何重塑受体二聚体。这些构象变化预计会穿过内膜并重新定位周质dCache结构域,从而与DvhG发生相互作用。建模显示,当DvhD与DvhG结合时,会阻挡蛋白酶接触粘附蛋白,甚至可能扭曲其钙结合位点,使这把“剪刀”处于关闭状态。当c‑di‑GMP水平下降时,受体的构象放松,释放DvhG,使其能钳住粘附蛋白的滞留区并进行切割,从而允许粘附蛋白的外部部分——以及生物膜基质——从细胞表面滑脱。通过这种方式,脱硫弧菌将其环境的内部化学读数转化为一个机械决策:保持附着或解散。
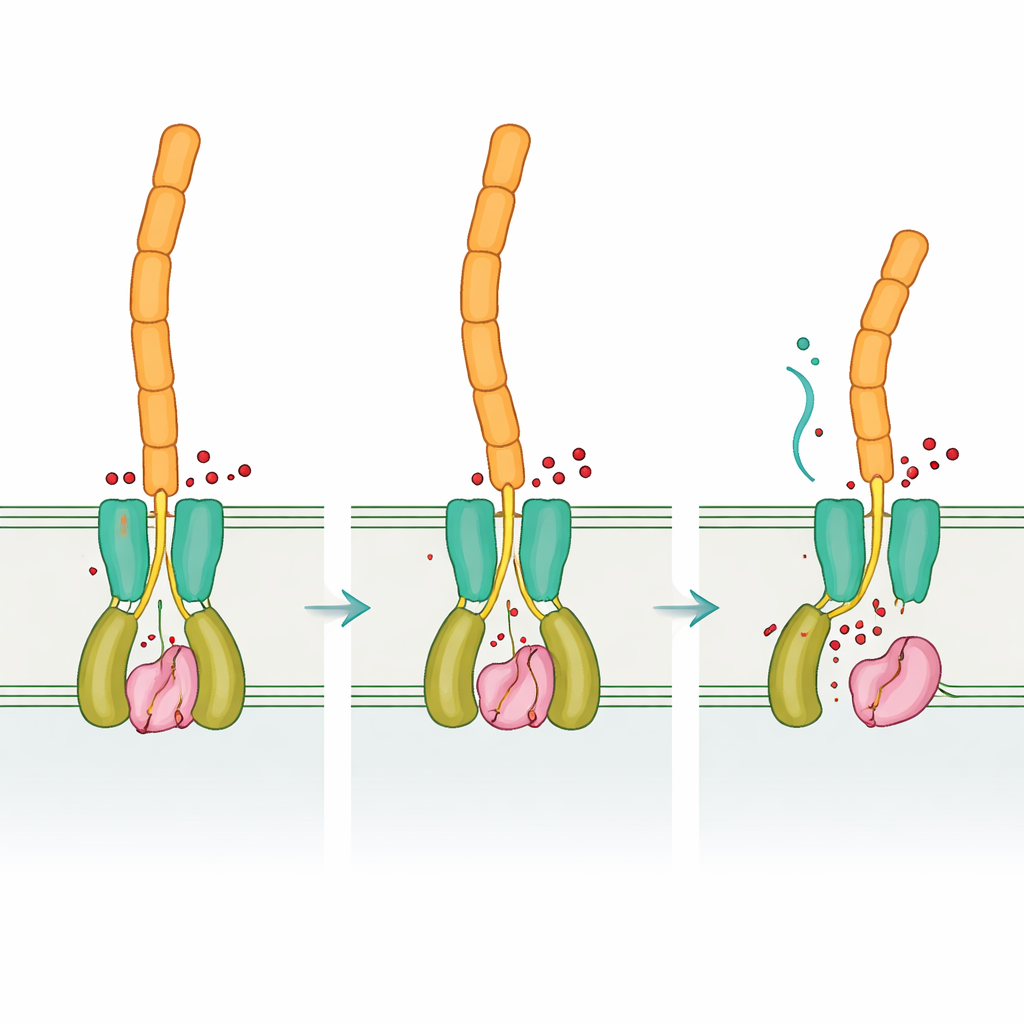
相同逻辑,不同“硬件”
综上所述,结果表明脱硫弧菌使用了与更常见细菌相同的总体调控逻辑——c‑di‑GMP控制一个受体,该受体反过来抑制或释放一个切割表面粘附蛋白的蛋白酶——但它采用了一套非常不同的蛋白“部件”来实现。这种保守性与再造的混合说明了进化如何重用成功的信号理念,同时重塑执行这些功能的分子。理解这种灵活的设计不仅加深了我们对不同细菌群体中生物膜形成与解体机制的认识,也可能为更聪明的策略提供线索,以促进在生物修复中有益的生物膜或破坏导致金属腐蚀和慢性感染的有害生物膜。
引用: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
关键词: 细菌生物膜, 脱硫弧菌(Desulfovibrio vulgaris), 环二鸟苷酸(c‑di‑GMP)信号, 粘附蛋白蛋白酶, 硫酸盐还原细菌