Clear Sky Science · pt
Análises estruturais revelam interações protease-adesina e regulação de receptor de c-di-GMP em bactérias redutoras de sulfato
Por que bactérias pegajosas importam
Bactérias frequentemente não vivem como células isoladas, mas sim como comunidades densas e viscosas chamadas biofilmes. Essas comunidades podem revestir tubos, cascos de navios, rochas subterrâneas e até dispositivos médicos. Em bactérias redutoras de sulfato como Desulfovibrio vulgaris, os biofilmes são uma faca de dois gumes: ajudam a limpar ambientes poluídos, mas também aceleram a corrosão de metais. Este estudo faz uma pergunta simples com grandes implicações: como essas bactérias decidem quando aderir firmemente a uma superfície e quando se soltar?
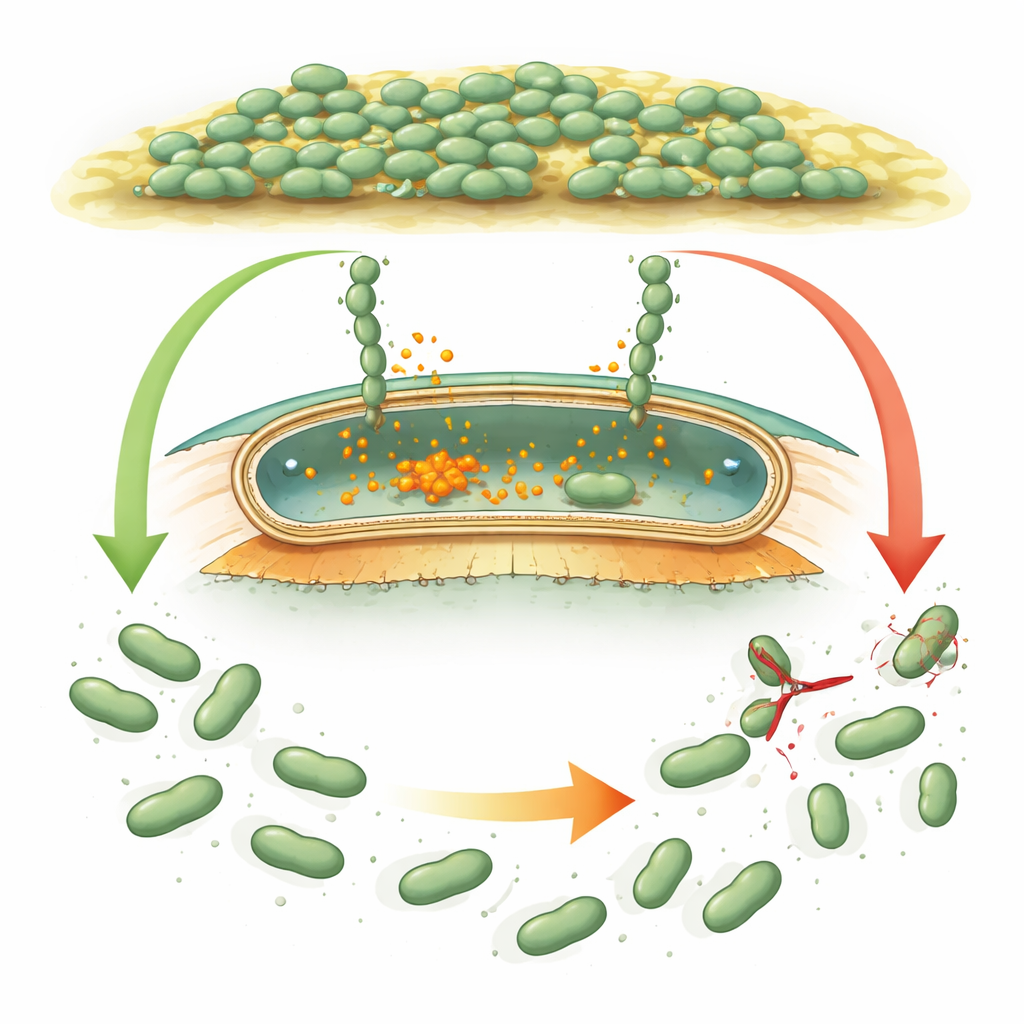
Como micróbios agarram e liberam
Muitas bactérias usam proteínas gigantes “tipo Velcro”, chamadas adesinas, que prendem as células às superfícies e entre si. Em espécies bem estudadas como Pseudomonas, essas adesinas são controladas por um sinal químico interno, o di‑GMP cíclico, que aumenta quando as bactérias devem formar um biofilme e cai quando devem dispersar. Quando o sinal está alto, as adesinas permanecem ancoradas na camada externa da célula. Quando ele diminui, uma pequena tesoura protéica (uma protease) corta a adesina perto da superfície celular, e a porção pegajosa flutua, ajudando as células a se destacarem. Desulfovibrio vulgaris parece carregar um conjunto genético similar, mas suas proteínas regulatórias diferem tanto em sequência e forma que os cientistas não conseguiam dizer se a lógica era a mesma ou se se tratava de uma estratégia totalmente nova.
Uma tesoura molecular especializada
Os autores concentraram‑se primeiro em DvhG, a versão em Desulfovibrio da protease que corta adesinas. Usando predição estrutural e testes bioquímicos, mostraram que DvhG tem o mesmo núcleo dobrado e a mesma maquinaria catalítica que suas contrapartes em outras bactérias e requer cálcio para funcionar. Ela corta com precisão duas grandes adesinas que Desulfovibrio precisa para formar biofilmes, em posições quase idênticas logo após um pequeno segmento de “retenção” que mantém essas proteínas alojadas na membrana externa. Intrigantemente, a equipe descobriu que DvhG faz mais do que simplesmente reconhecer uma sequência curta alvo. O volumoso domínio de retenção de cada adesina estabelece contato extenso com a protease, formando uma grande superfície de encaixe que aumenta a eficiência do corte. Mutações que perturbam essa área de encaixe tornam DvhG muito menos eficaz, revelando uma camada adicional de especificidade em comparação com sistemas relacionados.
Um interruptor sensor de sinal dentro da célula
O segundo ator chave, DvhD, situa‑se na membrana interna e alcança tanto o interior da célula quanto o espaço entre as membranas. Os pesquisadores resolveram várias estruturas tridimensionais de fragmentos de DvhD. Na parte externa da célula, sua região periplásmica forma um domínio dCache, uma arquitetura sensora comum que frequentemente se liga a pequenas moléculas. No interior da célula, DvhD carrega um domínio HD‑GYP, um módulo normalmente encontrado em enzimas que degradam o di‑GMP cíclico. Aqui, no entanto, os resíduos cruciais de ligação a metais estão ausentes, e ensaios cuidadosos mostraram que DvhD não destrói o sinal; em vez disso, liga‑se fortemente ao di‑GMP cíclico. Instantâneos estruturais revelaram dois bolsões de ligação distintos onde até três moléculas de di‑GMP cíclico podem interligar um par de domínios HD‑GYP e forçá‑los a uma nova arrumação, separando longas hélices que se conectam ao restante do receptor.
Do sinal interno ao comportamento na superfície
Ao comparar as formas “vazia” e ligada ao sinal de DvhD, a equipe descobriu como a ligação de di‑GMP cíclico pode remodelar o dímero do receptor. Espera‑se que essas mudanças se propaguem através da membrana interna e reposicionem o domínio periplásmico dCache, que por sua vez interage com DvhG. Modelagem sugere que quando DvhD se liga a DvhG, bloqueia o acesso da protease às adesinas e pode até distorcer seu sítio de ligação ao cálcio, desligando as tesouras. Quando os níveis de di‑GMP cíclico caem, a forma do receptor relaxa, liberando DvhG para que este possa agarrar os domínios de retenção das adesinas e cortá‑los, permitindo que as porções externas das adesinas — e assim a matriz do biofilme — se soltem da superfície celular. Desta forma, Desulfovibrio aplica uma leitura química interna de suas circunstâncias a uma decisão mecânica: permanecer preso ou dispersar.
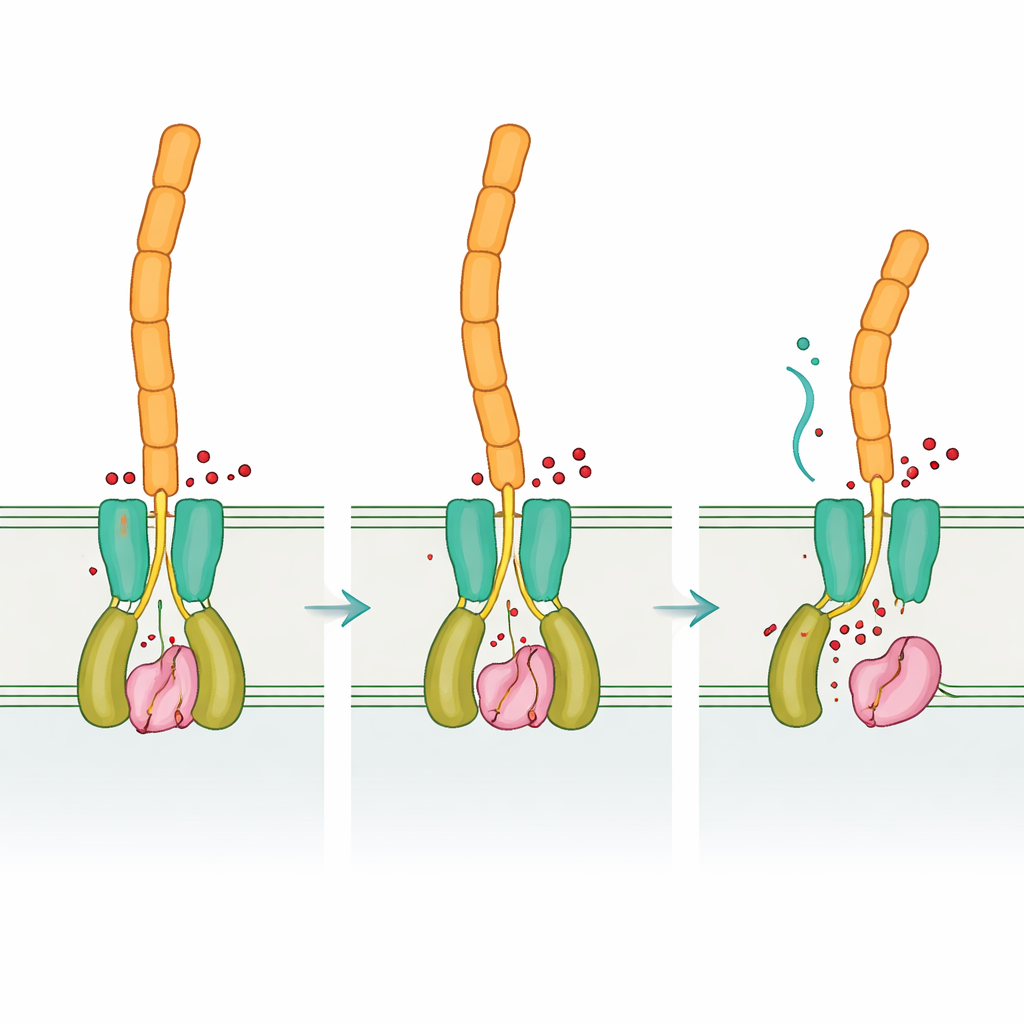
Mesma lógica, hardware diferente
Em conjunto, os resultados mostram que Desulfovibrio vulgaris usa a mesma lógica regulatória geral que bactérias mais familiares — o di‑GMP cíclico controla um receptor, que por sua vez restringe ou libera uma protease que corta adesinas de superfície — mas a implementa com um conjunto muito diferente de “peças” proteicas. Essa mistura de conservação e reinvenção ilustra como a evolução pode reutilizar ideias de sinalização bem‑sucedidas enquanto remodela as moléculas que as executam. Compreender esse design flexível não apenas aprofunda nossa compreensão de como biofilmes se formam e se desfazem em diversos grupos bacterianos, mas também pode apontar caminhos para estratégias mais inteligentes para promover biofilmes benéficos na biorremediação ou interromper os prejudiciais que causam corrosão metálica e infecções crônicas.
Citação: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Palavras-chave: biofilmes bacterianos, Desulfovibrio vulgaris, sinalização por di‑GMP cíclico, protease de adesina, bactérias redutoras de sulfato