Clear Sky Science · es
Análisis estructurales revelan interacciones proteasa‑adhesina y regulación del receptor de c‑di‑GMP en bacterias reductoras de sulfato
Por qué importan las bacterias pegajosas
Las bacterias rara vez viven como células aisladas; suelen formar comunidades densas y viscosas llamadas biopelículas. Estas comunidades pueden recubrir tuberías, cascos de barcos, rocas subterráneas e incluso dispositivos médicos. En bacterias reductoras de sulfato como Desulfovibrio vulgaris, las biopelículas son una espada de doble filo: ayudan a limpiar ambientes contaminados pero también aceleran la corrosión de metales. Este estudio plantea una pregunta simple con grandes implicaciones: ¿cómo deciden estas bacterias cuándo adherirse firmemente a una superficie y cuándo soltarse?
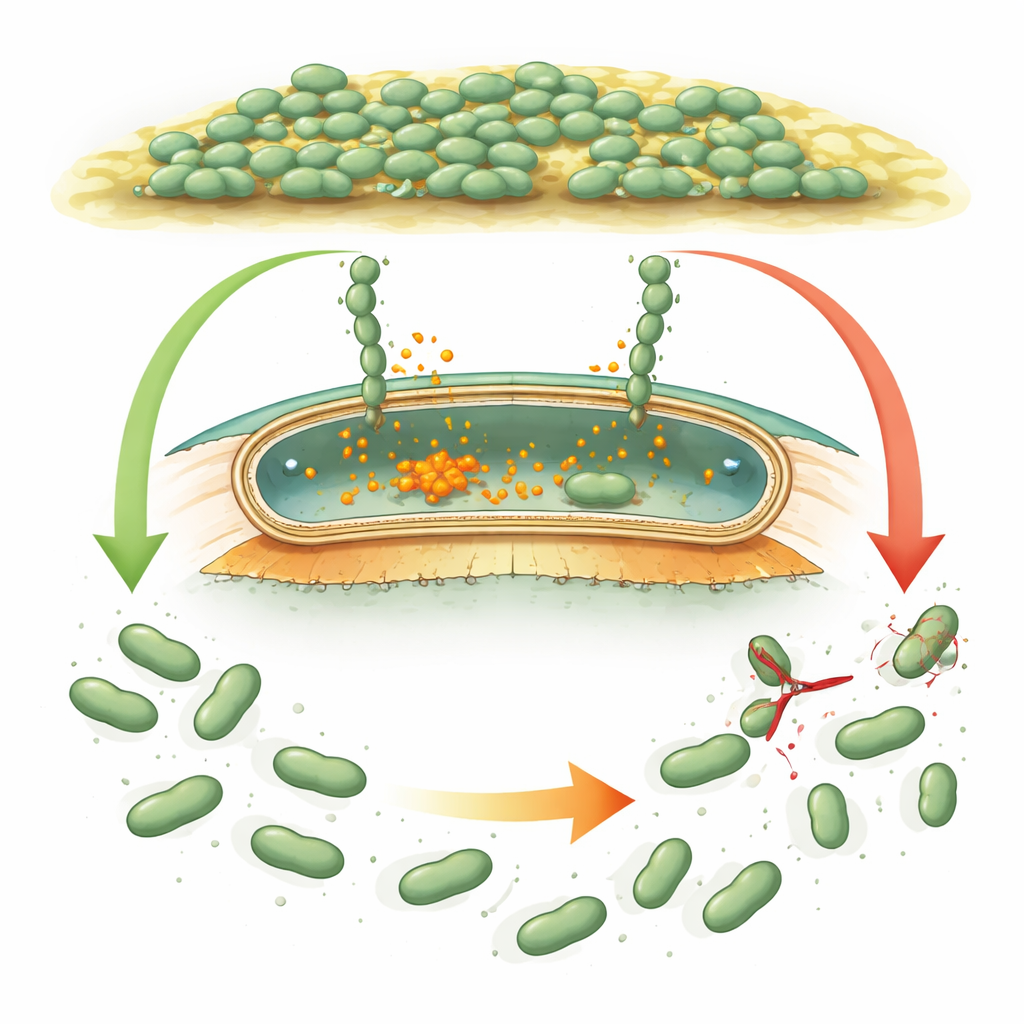
Cómo se agarran y liberan los microbios
Muchas bacterias usan proteínas gigantes tipo “velcro”, llamadas adhesinas, que pegan las células a superficies y entre sí. En especies bien estudiadas como Pseudomonas, estas adhesinas están controladas por una señal química interna, el ciclodi‑GMP, que aumenta cuando las bacterias deben formar una biopelícula y disminuye cuando deben dispersarse. Cuando la señal es alta, las adhesinas permanecen ancladas en la capa externa de la célula. Cuando baja, una pequeña tijera proteica (una proteasa) corta la adhesina cerca de la superficie celular y la porción pegajosa se libera, ayudando a las células a desprenderse. Desulfovibrio vulgaris parece portar un conjunto genético similar, pero sus proteínas regulatorias difieren tanto en secuencia y forma que los científicos no podían determinar si seguía la misma lógica o una estrategia totalmente nueva.
Tijeras moleculares especializadas
Los autores se centraron primero en DvhG, la versión en Desulfovibrio de la proteasa que corta adhesinas. Mediante predicción estructural y ensayos bioquímicos, mostraron que DvhG tiene el mismo plegamiento básico y la maquinaria catalítica que sus homólogos en otras bacterias y que requiere calcio para funcionar. Corta con precisión dos adhesinas grandes que Desulfovibrio necesita para formar biopelículas, en posiciones casi idénticas justo después de un pequeño segmento de “retención” que mantiene estas proteínas alojadas en la membrana externa. De forma intrigante, el equipo encontró que DvhG no se limita a reconocer una secuencia objetivo corta. El voluminoso dominio de retención de cada adhesina establece contactos extensos con la proteasa, formando una gran superficie de acoplamiento que aumenta la eficiencia del corte. Mutaciones que interrumpen este parche de acoplamiento hacen a DvhG mucho menos eficiente, revelando una capa añadida de especificidad en comparación con sistemas afines.
Un interruptor sensor de señales dentro de la célula
El segundo actor clave, DvhD, se encuentra en la membrana interna y alcanza tanto el interior celular como el espacio entre membranas. Los investigadores resolvieron múltiples estructuras tridimensionales de fragmentos de DvhD. En la cara exterior, su región periplásmica forma un dominio dCache, una arquitectura sensora común que suele unirse a moléculas pequeñas. En el interior celular, DvhD porta un dominio HD‑GYP, un módulo que habitualmente aparece en enzimas que degradan ciclodi‑GMP. Aquí, sin embargo, faltan los residuos críticos de unión al metal y ensayos cuidadosos mostraron que DvhD no destruye la señal; en cambio, se une al ciclodi‑GMP con mucha afinidad. Las instantáneas estructurales revelaron dos bolsillos de unión distintos donde hasta tres moléculas de ciclodi‑GMP pueden puentejar un par de dominios HD‑GYP y forzarlos a una nueva disposición, separando largas hélices que conectan con el resto del receptor.
De la señal interna al comportamiento en la superficie
Al comparar las formas “vacía” y ligando‑unida de DvhD, el equipo descubrió cómo la unión de ciclodi‑GMP puede remodelar el dímero del receptor. Se espera que estos cambios se propaguen a través de la membrana interna y reposicionen el dominio periplásmico dCache, que a su vez interactúa con DvhG. Los modelos sugieren que cuando DvhD se acopla a DvhG, bloquea el acceso de la proteasa a las adhesinas e incluso puede distorsionar su sitio de unión al calcio, dejando las tijeras "apagadas". Cuando los niveles de ciclodi‑GMP disminuyen, la conformación del receptor se relaja, liberando a DvhG para que se enganche a los dominios de retención de las adhesinas y las corte, permitiendo que las porciones externas de las adhesinas—y por tanto la matriz de la biopelícula—se deslicen fuera de la superficie celular. De este modo, Desulfovibrio aplica una lectura química interna de sus circunstancias a una decisión mecánica: permanecer adherido o dispersarse.
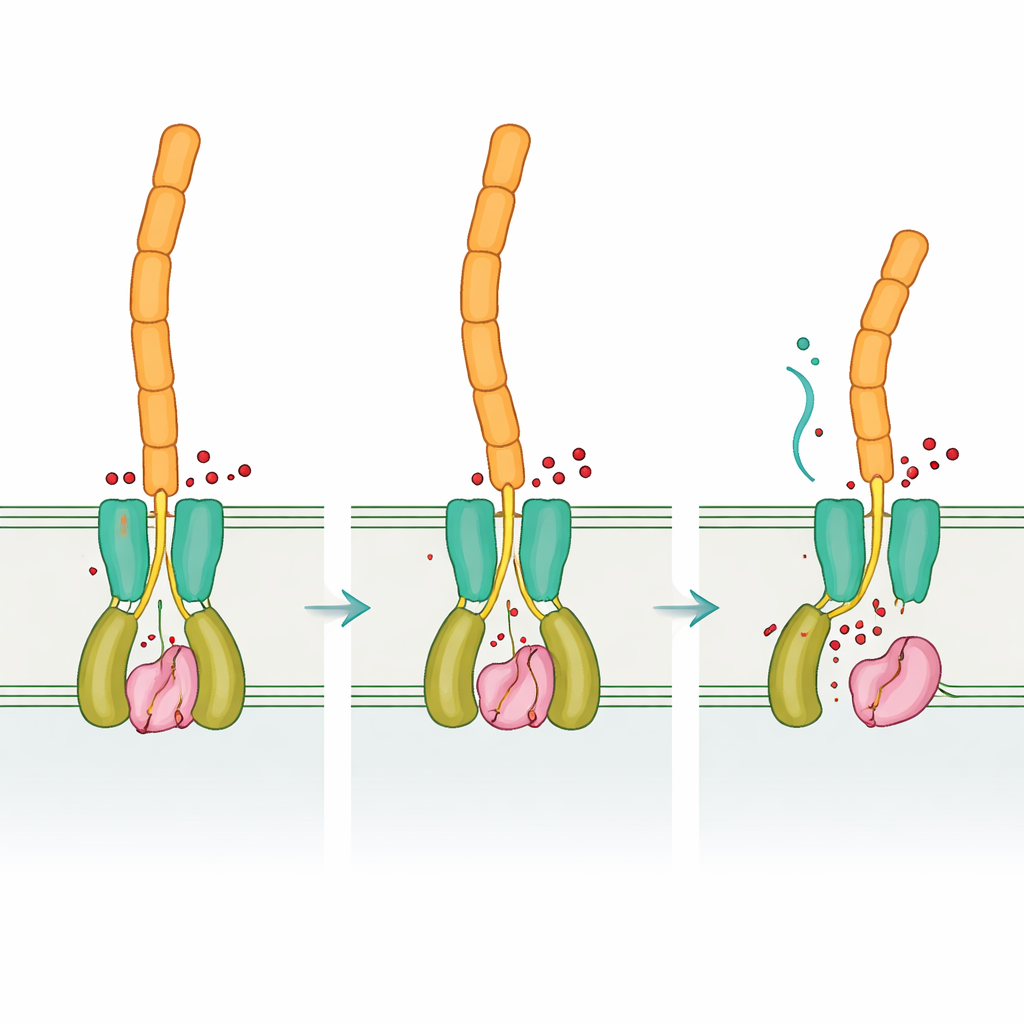
Misma lógica, distinta maquinaria
En conjunto, los resultados muestran que Desulfovibrio vulgaris usa la misma lógica regulatoria general que bacterias más familiares: el ciclodi‑GMP controla un receptor que a su vez restringe o libera a una proteasa que corta adhesinas superficiales, pero lo implementa con un conjunto de “piezas” proteicas muy distinto. Esta mezcla de conservación e reinvención ilustra cómo la evolución puede reutilizar ideas de señalización exitosas mientras remodela las moléculas que las llevan a cabo. Comprender este diseño flexible no solo profundiza nuestra comprensión de cómo se forman y rompen las biopelículas en muchos grupos bacterianos, sino que también puede señalar vías para estrategias más inteligentes, ya sea para promover biopelículas útiles en biorremediación o para interrumpir las dañinas que provocan corrosión metálica e infecciones crónicas.
Cita: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Palabras clave: biopelículas bacterianas, Desulfovibrio vulgaris, señalización por ciclodi‑GMP, proteasa de adhesina, bacterias reductoras de sulfato