Clear Sky Science · ja
構造解析が明らかにした硫酸還元細菌におけるプロテアーゼ–アドヘジン相互作用とc‑di‑GMP受容体の調節
なぜ“粘着性”細菌が重要なのか
細菌は単独の細胞としてではなく、群れになって粘性のある集合体—バイオフィルム—として生活することが多い。これらの集団は配管や船底、地下の岩石、さらには医療機器を覆うことがある。デスルフォビブリオ・バルガリスのような硫酸還元細菌では、バイオフィルムは二面性を持つ:汚染環境の浄化を助ける一方で金属の腐食を促進する。著者らは単純だが重要な問いを投げかける:これらの細菌はいつ表面にしっかりと付着し、いつ離れることを選ぶのか?
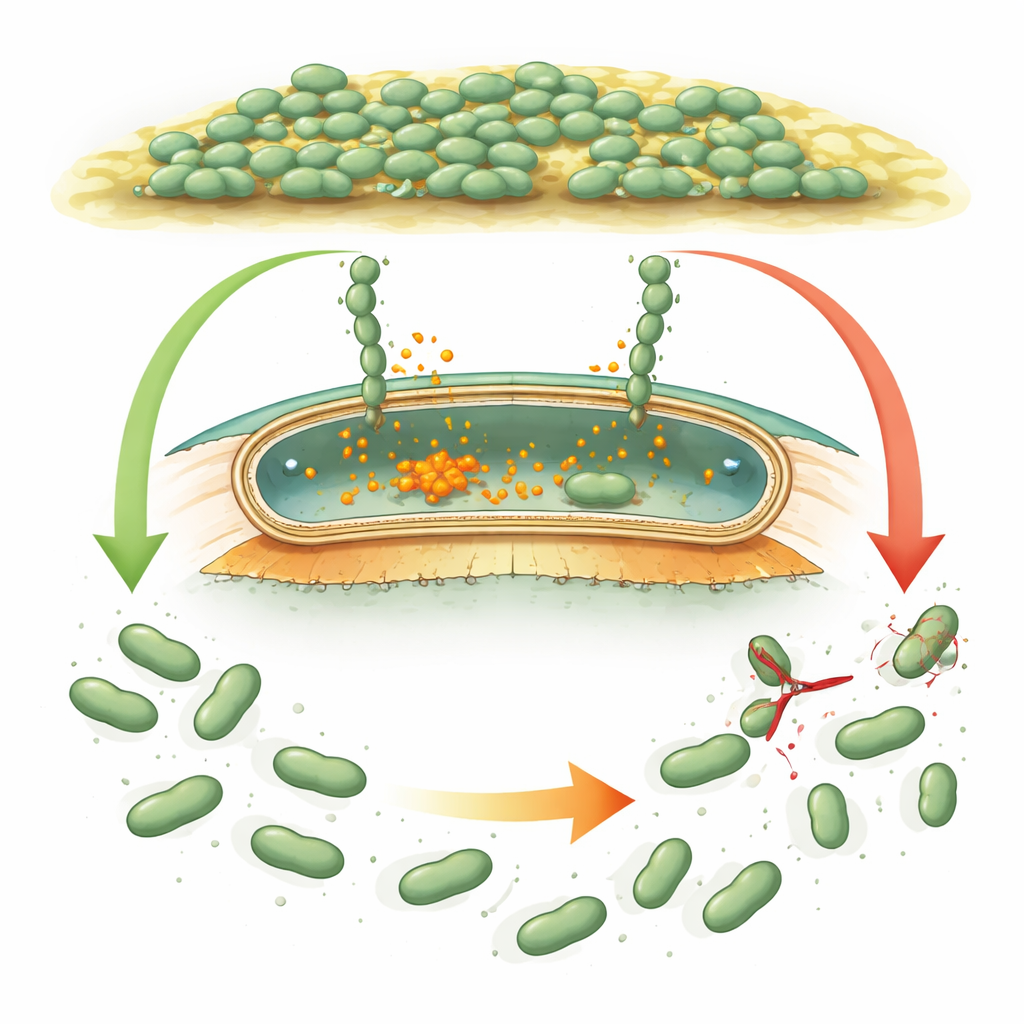
微生物はどうやって掴み、放すのか
多くの細菌は巨大で“ベルクロ様”のタンパク質、アドヘジンを使って細胞を表面や互いに付着させる。シュードモナスなどよく研究された種では、これらのアドヘジンは内部化学シグナルである環状ジグアノシン一リン酸(c‑di‑GMP)によって制御され、バイオフィルムを形成すべきときに上昇し、分散すべきときに低下する。シグナルが高いとき、アドヘジンは外膜に留まり、低下すると小さなタンパク質切断酵素(プロテアーゼ)がアドヘジンを細胞表面近くで切断し、粘着性の部分が流れ去って細胞の離脱を助ける。デスルフォビブリオ・バルガリスも類似の遺伝的装置を持つように見えるが、その調節タンパク質は配列や立体構造が大きく異なるため、同じ論理を用いるのか別の戦略を採るのか判断できなかった。
特化した分子ハサミ
著者らはまずアドヘジンを切断するプロテアーゼのデスルフォビブリオ版であるDvhGに着目した。構造予測と生化学的解析により、DvhGは他細菌の対応酵素と同じ核心の折りたたみと触媒機構を備え、カルシウムを必要とすることが示された。DvhGはバイオフィルム形成に必要な二つの大型アドヘジンを、いずれも小さな“保持”セグメントの直後というほぼ同一の位置で正確に切断するという。興味深いことに、DvhGは短い標的配列を認識するだけでなく、各アドヘジンの大きな保持ドメインがプロテアーゼと広範に接触して大きなドッキング面を形成し、切断効率を高めている。ドッキング面を乱す変異はDvhGの有効性を大きく低下させ、関連する系と比べて特異性の追加層があることを明らかにした。
細胞内にあるシグナル感知スイッチ
第二の主要因子DvhDは内膜に位置し、細胞内と膜間空間の両方に到達する。研究者らはDvhD断片の複数の三次元構造を解いた。細胞外側、すなわちペリプラズム領域ではdCacheドメインを形成しており、これは小分子を結合することの多い一般的なセンサー構造である。細胞内側ではDvhDはHD‑GYPドメインを持ち、通常はc‑di‑GMPを分解する酵素に見られるモジュールだ。しかしここでは重要な金属結合残基が欠損しており、詳細なアッセイによりDvhDはシグナルを破壊せず、むしろc‑di‑GMPを非常に強く結合することが示された。構造のスナップショットは、最大三分子のc‑di‑GMPが二つのHD‑GYPドメインの対を架橋して結合できる二つの異なる結合ポケットを明らかにし、それによって受容体を新しい配列へと押し広げ、受容体に連なる長いヘリックスをこじ開ける様子が示された。
内部シグナルから表面の挙動へ
“空の”形とシグナル結合形のDvhDを比較することで、c‑di‑GMPの結合が受容体ダイマーをどのように再形成するかが明らかになった。これらの変化は内膜を通して伝わり、ペリプラズム側のdCacheドメインの位置を変え、それがさらにDvhGと相互作用することが予想される。モデリングは、DvhDがDvhGに結合するとプロテアーゼのアドヘジンへのアクセスを遮断し、場合によってはカルシウム結合部位を歪めてハサミを“オフ”にする可能性を示唆する。c‑di‑GMP濃度が低下すると受容体の形が緩み、DvhGが解放されてアドヘジンの保持ドメインにしっかり取り付き切断を行い、アドヘジンの外側部分—すなわちバイオフィルム基質—が細胞表面から滑り落ちる。こうしてデスルフォビブリオは周囲の状況を内部化学シグナルで読み取り、それを機械的な決定:付着を続けるか分散するか、に変換している。
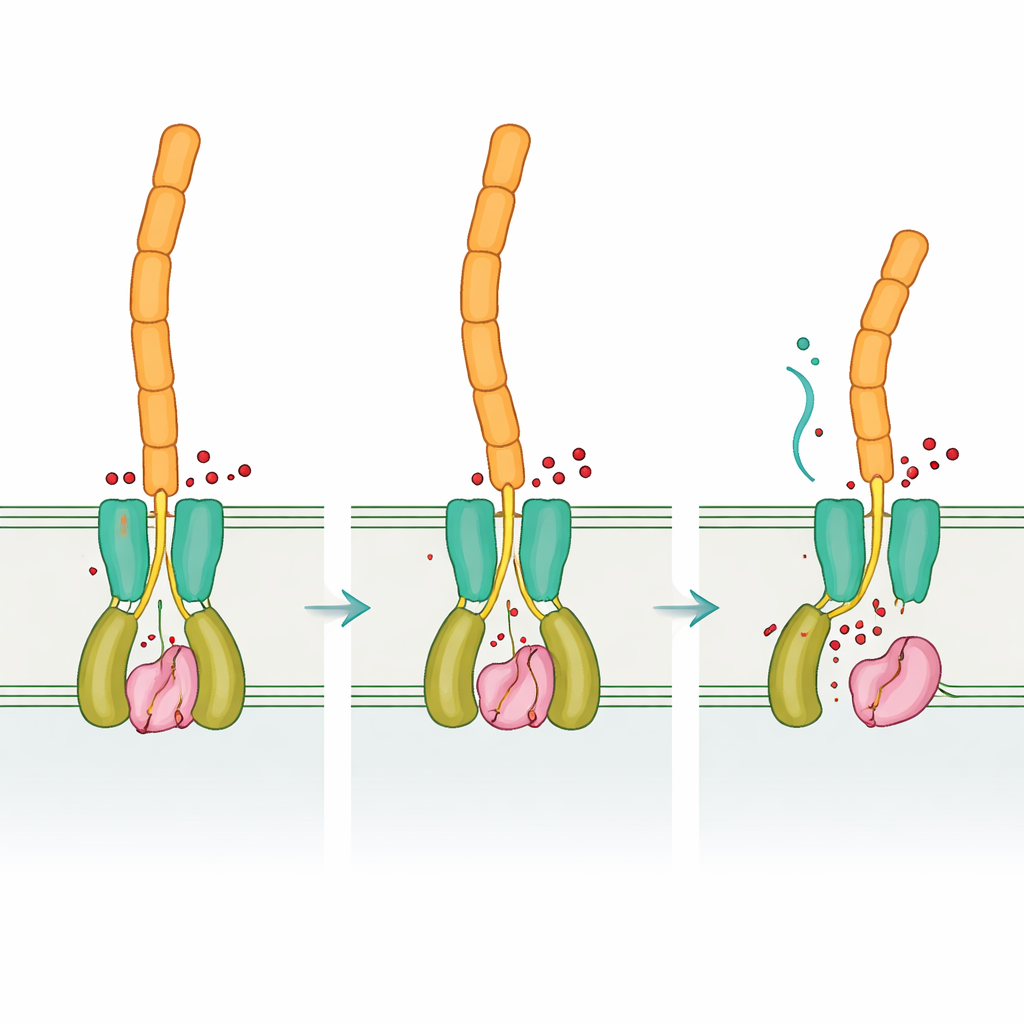
同じ論理、異なるハードウェア
総じて、本研究はデスルフォビブリオ・バルガリスがより馴染みのある細菌と同様の全体的な調節論理を用いることを示している—c‑di‑GMPが受容体を制御し、それがプロテアーゼを抑えたり解放したりして表面アドヘジンを切断する—が、その実装には非常に異なるタンパク質“部品”が使われている。この保存と再発明の混合は、進化が成功したシグナル伝達のアイデアを再利用しつつ、それを担う分子を再構築しうることを示している。この柔軟な設計を理解することは、バイオフィルムが多様な細菌群で形成・解体される仕組みへの理解を深めるだけでなく、環境修復に有用なバイオフィルムを促進したり、金属腐食や慢性感染を引き起こす有害なバイオフィルムを破壊するためのより賢明な戦略を指し示す可能性がある。
引用: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
キーワード: 細菌性バイオフィルム, デスルフォビブリオ・バルガリス, 環状ジグアノシン一リン酸シグナル伝達, アドヘジンプロテアーゼ, 硫酸還元細菌