Clear Sky Science · ru
Структурные анализы выявляют взаимодействия между протеазой и адгезином и регуляцию рецептора c-di-GMP у сульфатредуцирующих бактерий
Почему «липкие» бактерии важны
Бактерии часто живут не поодиночке, а в плотных слизистых сообществах, называемых биоплёнками. Эти сообщества могут покрывать трубы, борта судов, подземные породы и даже медицинские импланты. У сульфатредуцирующих бактерий, таких как Desulfovibrio vulgaris, биоплёнки — палка о двух концах: они помогают очищать загрязнённые среды, но также ускоряют коррозию металлов. В этом исследовании задан простой вопрос с крупными последствиями: как эти бактерии решают, когда прочно прикрепиться к поверхности, а когда — оторваться?
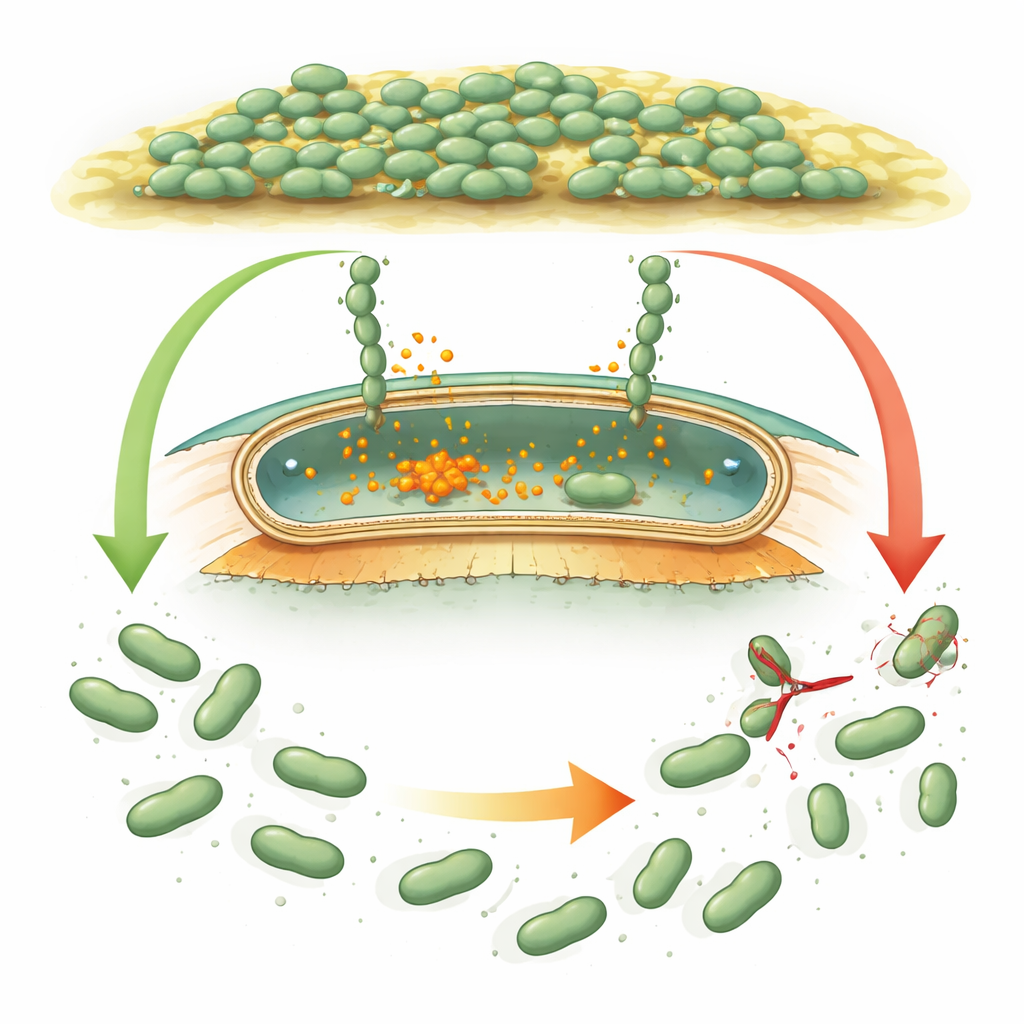
Как микробы цепляются и отпускают
Многие бактерии используют гигантские «велькро‑подобные» белки, называемые адгезинами, которые приклеивают клетки к поверхностям и друг к другу. В хорошо изученных видах, таких как Pseudomonas, адгезины контролируются внутренним химическим сигналом — циклическим ди‑GMP, который повышается, когда нужно формировать биоплёнку, и падает, когда её следует рассредоточить. При высоком уровне сигнала адгезины остаются заякоренными во внешней оболочке клетки. Когда сигнал падает, маленький «резак» — протеаза — отрезает адгезин близко к поверхности клетки, и липкая часть уносится, помогая клеткам отделиться. У Desulfovibrio vulgaris имеется похожий генетический набор, но регуляторные белки настолько отличаются по последовательности и форме, что учёные не могли понять: действует ли там та же логика или полностью новая стратегия.
Специализированные молекулярные ножницы
Авторы сначала сосредоточились на DvhG, версии протеазы Desulfovibrio, расщепляющей адгезины. С помощью предсказания структуры и биохимических тестов они показали, что DvhG имеет ту же основную складку и каталитический аппарат, что и аналоги у других бактерий, и требует кальция для работы. Она точно разрезает два крупных адгезина, необходимых Desulfovibrio для формирования биоплёнки, почти в идентичных позициях сразу за небольшой «удерживающей» секцией, которая фиксирует эти белки в наружной мембране. Любопытно, что команда обнаружила: DvhG делает больше, чем просто распознаёт короткую целевую последовательность. Объёмный удерживающий домен каждого адгезина образует обширный контакт с протеазой, создавая большую «стоянку» для стыковки, которая повышает эффективность разрезания. Мутации, разрушающие эту область стыковки, сильно снижают активность DvhG, что выявляет дополнительный уровень специфичности по сравнению с родственными системами.
Переключатель‑датчик внутри клетки
Второй ключевой участник, DvhD, располагается во внутренней мембране и протягивает домены как в цитоплазму, так и в пространство между мембранами. Исследователи получили несколько трёхмерных структур фрагментов DvhD. Снаружи клетки его периплазматическая часть образует dCache‑домен — распространённую сенсорную архитектуру, часто связывающую малые молекулы. Внутри клетки DvhD несёт домен HD‑GYP, модуль, обычно встречающийся в ферментах, разрушающих циклический ди‑GMP. Однако здесь отсутствуют критические остатки, связывающие металл, и тщательно проведённые анализы показали, что DvhD не разлагает сигнал; вместо этого он очень прочно связывает циклический ди‑GMP. Структурные «моментальные снимки» выявили две различные связующие карманы, где до трёх молекул циклического ди‑GMP могут мостить пару HD‑GYP‑доменов и заставлять их занять новую конфигурацию, расклинивая длинные спирали, которые соединяются с остальной частью рецептора.
От внутреннего сигнала к поведению на поверхности
Сравнивая «пустую» и связанную с сигналом формы DvhD, команда выяснила, как связывание циклического ди‑GMP может перестраивать димер рецептора. Ожидается, что эти изменения передаются через внутреннюю мембрану и перерасполагают периплазматический dCache‑домен, который, в свою очередь, взаимодействует с DvhG. Моделирование указывает на то, что когда DvhD связывается с DvhG, он блокирует доступ протеазы к адгезинам и даже может искажать её кальциевое связующее место, переводя «ножницы» в положение «выключено». Когда уровни циклического ди‑GMP падают, конформация рецептора расслабляется, освобождая DvhG, чтобы тот мог захватить удерживающие домены адгезинов и разрезать их, позволяя наружным частям адгезинов — а значит и матрице биоплёнки — оторваться от поверхности клетки. Таким образом Desulfovibrio превращает внутренний химический отчёт о своих обстоятельствах в механическое решение: оставаться прикреплённым или рассредоточиться.
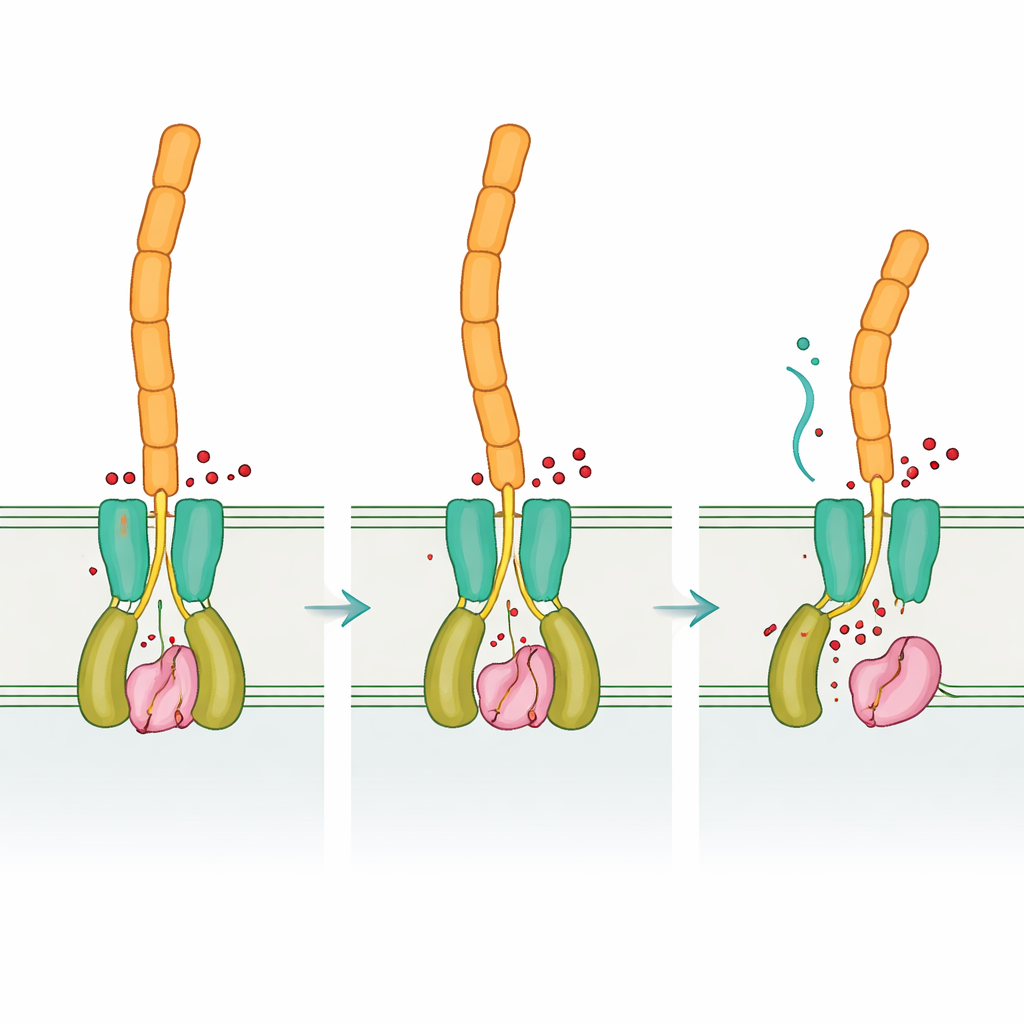
Та же логика, другое «оборудование»
В совокупности результаты показывают, что Desulfovibrio vulgaris использует ту же общую регуляторную логику, что и более знакомые бактерии — циклический ди‑GMP управляет рецептором, который, в свою очередь, сдерживает или отпускает протеазу, обрезающую поверхностные адгезины — но реализует её с совершенно иным набором белковых «деталей». Такое сочетание консервации и переработки иллюстрирует, как эволюция может повторно использовать удачные сигнальные идеи, перестраивая молекулы, которые их воплощают. Понимание этой гибкой архитектуры не только углубляет наше представление о том, как биоплёнки формируются и распадаются у разных групп бактерий, но и может указать путь к более умным стратегиям — либо для поощрения полезных биоплёнок в биоремедиации, либо для разрушения вредных, вызывающих коррозию металлов и хронические инфекции.
Цитирование: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Ключевые слова: бактериальные биоплёнки, Desulfovibrio vulgaris, сигнализация циклическим ди‑GMP, протеаза адгезина, сульфатредуцирующие бактерии