Clear Sky Science · nl
Structurele analyses onthullen interacties tussen protease en adhesine en regulatie door c-di-GMP-receptor in sulfaatreducerende bacteriën
Waarom plakkerige bacteriën ertoe doen
Bacteriën leven vaak niet als losse cellen maar als drukbevolkte, slijmerige gemeenschappen die biofilms worden genoemd. Deze gemeenschappen kunnen pijpleidingen, scheepsrompen, ondergrondse gesteenten en zelfs medische hulpmiddelen bedekken. Bij sulfaatreducerende bacteriën zoals Desulfovibrio vulgaris zijn biofilms een tweesnijdend zwaard: ze helpen vervuilde omgevingen reinigen, maar versnellen ook de aantasting van metalen. Deze studie stelt een eenvoudige vraag met grote gevolgen: hoe beslissen deze bacteriën wanneer ze zich stevig aan een oppervlak vasthechten en wanneer ze loslaten?
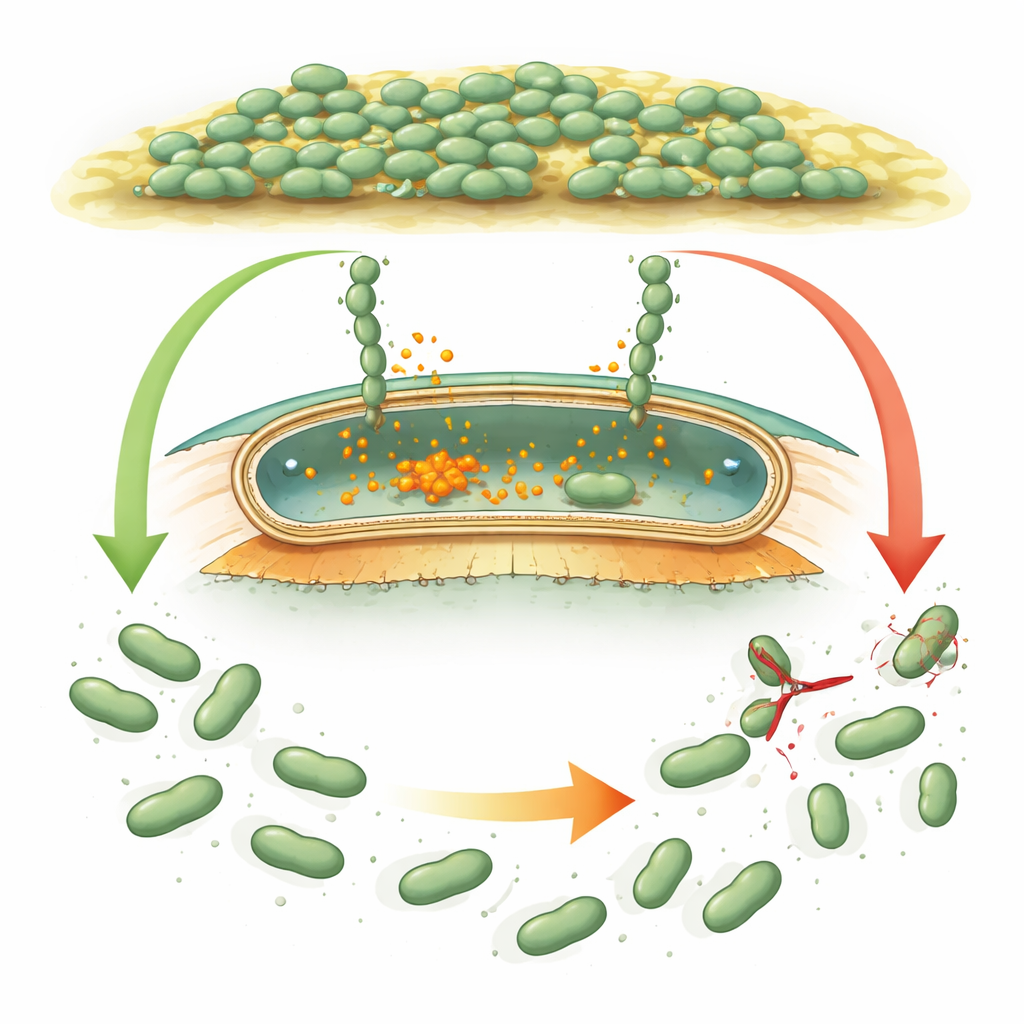
Hoe microben grijpen en loslaten
Veel bacteriën gebruiken reusachtige “klittenband‑achtige” eiwitten, adhesines genoemd, die cellen aan oppervlakken en aan elkaar laten kleven. In goed bestudeerde soorten zoals Pseudomonas worden deze adhesines gereguleerd door een interne chemische signaalstof, cyclisch di‑GMP, die stijgt wanneer bacteriën een biofilm moeten vormen en daalt wanneer ze moeten verspreiden. Wanneer het signaal hoog is, blijven adhesines verankerd in de buitenschil van de cel. Wanneer het daalt, knipt een klein eiwitmesje (een protease) de adhesine vlak bij het celoppervlak door, en het plakkende deel drijft weg, wat helpt de cellen los te laten. Desulfovibrio vulgaris heeft ogenschijnlijk een vergelijkbaar genetisch arsenaal, maar zijn regulerende eiwitten wijken zodanig af in sequentie en vorm dat wetenschappers niet konden vaststellen of het dezelfde logica gebruikt of een geheel nieuwe strategie.
Een gespecialiseerd moleculair schaar
De auteurs richtten zich eerst op DvhG, de Desulfovibrio‑versie van het adhesine‑knippende protease. Met structurele voorspelling en biochemische proeven toonden ze aan dat DvhG dezelfde kernvouwing en katalytische machinerie heeft als tegenhangers in andere bacteriën en calcium nodig heeft om te werken. Het knipt nauwkeurig twee grote adhesines die Desulfovibrio voor biofilmvorming nodig heeft, op nagenoeg identieke posities net na een klein “retentie”segment dat deze eiwitten in de buitenmembraan verankert. Intrigerend genoeg bleek dat DvhG meer doet dan simpelweg een korte doelvolgorde herkennen. Het omvangrijke retentiegebied van elke adhesine maakt uitgebreide contacten met het protease en vormt een groot dokoppervlak dat de knipsnelheid verhoogt. Mutaties die deze docking‑patch verstoren maken DvhG veel minder effectief, wat een extra laag specificiteit onthult vergeleken met verwante systemen.
Een signaal‑gevoelige schakel binnenin de cel
De tweede hoofdrolspeler, DvhD, zit in het binnenmembraan en reikt zowel in het binnenste van de cel als in de ruimte tussen de membranen. De onderzoekers bepaalden meerdere driedimensionale structuren van DvhD‑fragmenten. Buiten de cel vormt het periplasmische deel een dCache‑domein, een veelvoorkomende sensorarchitectuur die vaak kleine moleculen bindt. Binnenin de cel draagt DvhD een HD‑GYP‑domein, een module die gewoonlijk voorkomt in enzymen die cyclisch di‑GMP afbreken. Hier ontbreken echter de cruciale metaalbindende residuen, en zorgvuldige assays toonden aan dat DvhD het signaal niet vernietigt; in plaats daarvan bindt het cyclisch di‑GMP zeer strak. Structurele momentopnamen onthulden twee verschillende bindingspockets waar tot drie cyclisch di‑GMP‑moleculen een paar HD‑GYP‑domeinen kunnen overbruggen en ze in een nieuwe rangschikking dwingen, waardoor lange helices die aan de rest van de receptor verbonden zijn uit elkaar worden gedrukt.
Van intern signaal naar oppervlakgedrag
Door de “lege” en signaalgebonden vormen van DvhD te vergelijken, legde het team bloot hoe binding van cyclisch di‑GMP het receptor‑dimeer kan hervormen. Verwacht wordt dat deze veranderingen door het binnenmembraan reizen en het periplasmische dCache‑domein herpositioneren, dat op zijn beurt met DvhG interageert. Modellering suggereert dat wanneer DvhD DvhG bindt, het de toegang van het protease tot adhesines blokkeert en mogelijk zelfs het calciumbindingsgebied verstoort, waardoor de schaar “uit” staat. Wanneer de cyclisch di‑GMP‑niveaus dalen, ontspant de vorm van de receptor, laat DvhG vrij zodat het zich kan vastklemmen op de retentiegebieden van de adhesines en ze kan doorsnijden, waardoor de buitendelen van de adhesines—en daarmee de biofilmmatrix—van het celoppervlak loslaten. Op deze manier zet Desulfovibrio een interne chemische beoordeling van zijn omstandigheden om in een mechanische keuze: vastzitten of verspreiden.
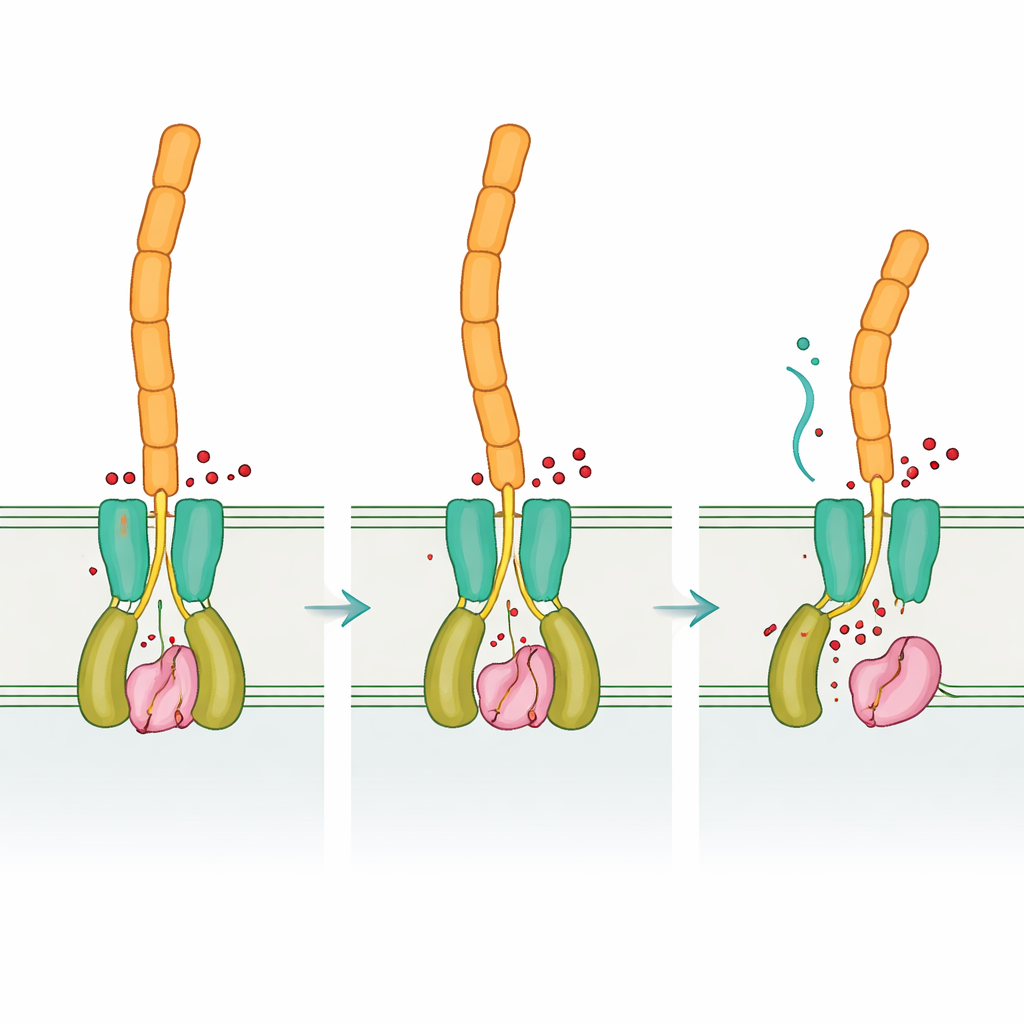
Zelfde logica, andere hardware
Samengevoegd tonen de resultaten dat Desulfovibrio vulgaris dezelfde algemene regelende logica gebruikt als beter bekende bacteriën—cyclisch di‑GMP reguleert een receptor, die op zijn beurt een protease remt of vrijgeeft dat oppervlakte‑adhesines afknipt—maar dit implementeert met een heel andere set eiwit‑“onderdelen.” Deze mix van behoud en heruitvinding illustreert hoe evolutie succesvolle signaalideeën kan hergebruiken terwijl de moleculen die ze uitvoeren worden hervormd. Inzicht in dit flexibele ontwerp verdiept niet alleen ons begrip van hoe biofilms zich vormen en uiteen vallen bij vele bacteriegroepen, maar kan ook wijzen op slimmer strategieën om behulpzame biofilms in bioremediatie te bevorderen of schadelijke biofilms te verstoren die metaalcorrosie en chronische infecties veroorzaken.
Bronvermelding: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Trefwoorden: bacteriële biofilms, Desulfovibrio vulgaris, cyclisch di-GMP-signaal, adhesine-protease, sulfaatreducerende bacteriën