Clear Sky Science · de
Strukturanalysen enthüllen Protease‑Adhäsin‑Interaktionen und c‑di‑GMP‑Rezeptorregulation in sulfatreduzierenden Bakterien
Warum klebrige Bakterien wichtig sind
Bakterien leben häufig nicht als einzelne Zellen, sondern als dichte, schleimige Gemeinschaften, die man Biofilme nennt. Diese Gemeinschaften können Rohrleitungen, Schiffsrümpfe, unterirdische Gesteine und sogar medizinische Geräte überziehen. Bei sulfatreduzierenden Bakterien wie Desulfovibrio vulgaris ist ein Biofilm ein zweischneidiges Schwert: Er hilft bei der Reinigung verschmutzter Umgebungen, beschleunigt aber auch die Korrosion von Metallen. Diese Studie stellt eine einfache Frage mit großen Folgen: Wie entscheiden diese Bakterien, wann sie sich fest an eine Oberfläche heften und wann sie wieder loslassen?
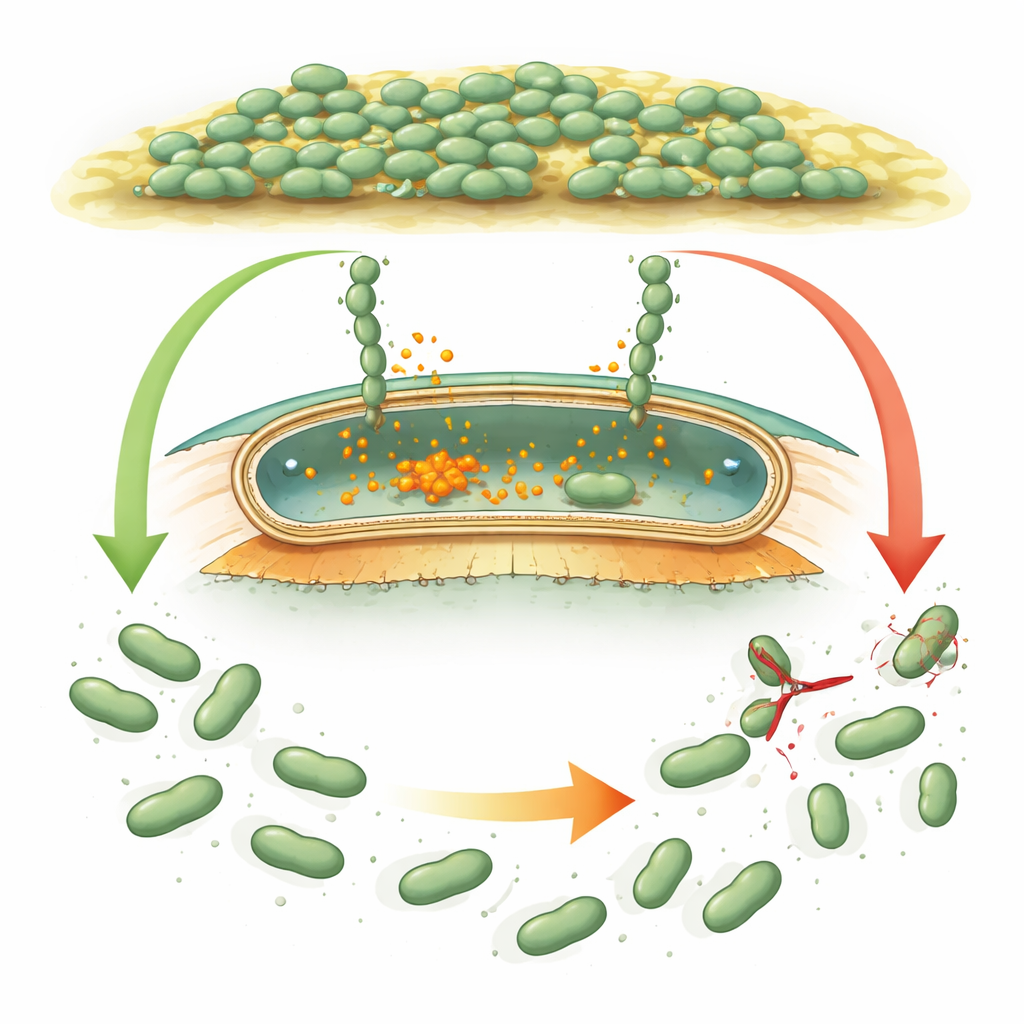
Wie Mikroben greifen und loslassen
Viele Bakterien nutzen riesige „Velcro‑artige“ Proteine, sogenannte Adhäsine, die Zellen an Oberflächen und aneinander haften lassen. In gut untersuchten Arten wie Pseudomonas werden diese Adhäsine durch ein internes chemisches Signal, cyclic di‑GMP, gesteuert, das ansteigt, wenn Bakterien einen Biofilm bilden sollen, und sinkt, wenn sie sich zerstreuen sollen. Bei hohem Signal bleiben Adhäsine in der äußeren Hülle der Zelle verankert. Fällt das Signal, schneidet eine kleine Protease das Adhäsin dicht an der Zelloberfläche ab, und der klebrige Teil treibt weg, wodurch sich die Zellen lösen können. Desulfovibrio vulgaris besitzt offenbar ein ähnliches genetisches Instrumentarium, doch die regulatorischen Proteine unterscheiden sich so stark in Sequenz und Gestalt, dass Forscher nicht sicher waren, ob dieselbe Logik gilt oder eine ganz andere Strategie vorliegt.
Eine spezialisierte molekulare Schere
Die Autoren konzentrierten sich zunächst auf DvhG, die Desulfovibrio‑Variante der Adhäsin‑spaltenden Protease. Anhand struktureller Vorhersage und biochemischer Tests zeigten sie, dass DvhG dieselbe Kernfaltung und katalytische Maschinerie wie entsprechende Proteasen in anderen Bakterien besitzt und Calcium zum Arbeiten benötigt. Sie schneidet präzise zwei große Adhäsine, die Desulfovibrio für die Biofilmbildung benötigt, an nahezu identischen Stellen, jeweils unmittelbar nach einem kleinen „Retention“‑Abschnitt, der diese Proteine in der äußeren Membran verankert. Interessanterweise erkannte das Team, dass DvhG mehr tut, als nur eine kurze Zielsequenz zu erkennen. Die voluminöse Retentionsdomäne jedes Adhäsins tritt in ausgedehnten Kontakt mit der Protease und bildet eine große Andockfläche, die die Schnitteffizienz erhöht. Mutationen, die diese Andockzone stören, machen DvhG deutlich weniger wirksam und offenbaren damit eine zusätzliche Spezifitätsebene im Vergleich zu verwandten Systemen.
Ein signalerkennender Schalter im Inneren der Zelle
Der zweite Schlüsselfaktor, DvhD, sitzt in der inneren Membran und reicht sowohl ins Zellinnere als auch in den Raum zwischen den Membranen hinein. Die Forschenden lösten mehrere dreidimensionale Strukturen von DvhD‑Fragmenten. Außerhalb der Zelle bildet sein periplasmatischer Bereich eine dCache‑Domäne, eine häufige Sensorarchitektur, die oft kleine Moleküle bindet. Im Inneren der Zelle trägt DvhD eine HD‑GYP‑Domäne, ein Modul, das normalerweise in Enzymen vorkommt, die cyclic di‑GMP abbauen. Hier fehlen jedoch die entscheidenden Metall‑bindenden Reste, und sorgfältige Assays zeigten, dass DvhD das Signal nicht zerstört; stattdessen bindet es cyclic di‑GMP sehr fest. Strukturaufnahmen offenbarten zwei verschiedene Bindungstaschen, in denen bis zu drei cyclic di‑GMP‑Moleküle ein Paar von HD‑GYP‑Domänen überbrücken können und diese in eine neue Anordnung zwingen, wodurch lange Helices auseinandergedrängt werden, die an den Rest des Rezeptors anschließen.
Vom internen Signal zum Oberflächenverhalten
Durch den Vergleich der „leeren“ und signalgebundenen Formen von DvhD deckte das Team auf, wie die Bindung von cyclic di‑GMP den Rezeptordimer umformen kann. Diese Veränderungen dürften durch die innere Membran weitergeleitet werden und die periplasmatische dCache‑Domäne neu positionieren, die ihrerseits mit DvhG interagiert. Modellierungen deuten darauf hin, dass DvhD, wenn es DvhG bindet, der Protease den Zugang zu Adhäsinen blockiert und möglicherweise sogar ihre Calcium‑Bindestelle verzerrt, wodurch die Schere „ausgeschaltet“ wird. Fallen die cyclic di‑GMP‑Spiegel, entspannt sich die Form des Rezeptors, gibt DvhG frei, sodass es sich an die Retentionsdomänen der Adhäsine klammern und sie schneiden kann; dadurch können die äußeren Abschnitte der Adhäsine – und damit die Biofilmmatrix – von der Zelloberfläche abgleiten. Auf diese Weise übersetzt Desulfovibrio ein internes chemisches Abbild seiner Lage in eine mechanische Entscheidung: anhaften oder zerstreuen.
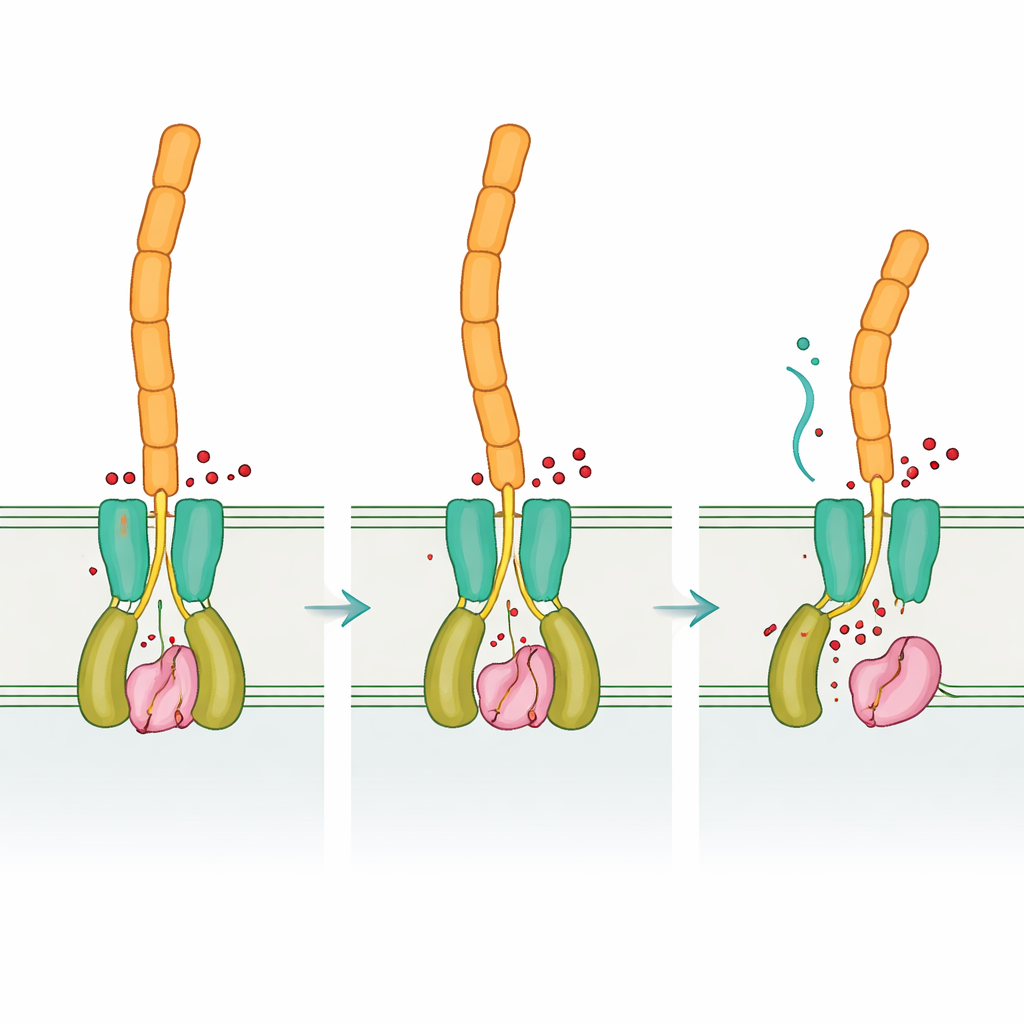
Gleiche Logik, andere Komponenten
Insgesamt zeigen die Ergebnisse, dass Desulfovibrio vulgaris dieselbe übergeordnete Steuerungslogik verwendet wie bekanntere Bakterien – cyclic di‑GMP kontrolliert einen Rezeptor, der wiederum eine Protease zurückhält oder freigibt, die Oberflächenadhäsine abschneidet – jedoch mit einem sehr unterschiedlichen Satz von Protein‑„Bauteilen“. Diese Mischung aus Konservierung und Neuerfindung veranschaulicht, wie die Evolution erfolgreiche Signallösungen wiederverwenden kann und zugleich die Moleküle umgestaltet, die sie ausführen. Das Verständnis dieses flexiblen Designs vertieft nicht nur unser Verständnis davon, wie Biofilme in vielen bakteriellen Gruppen entstehen und sich auflösen, sondern kann auch Hinweise geben für gezieltere Strategien, nützliche Biofilme in der Bioremediation zu fördern oder schädliche zu stören, die Metallkorrosion und chronische Infektionen vorantreiben.
Zitation: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Schlüsselwörter: bakterielle Biofilme, Desulfovibrio vulgaris, cyclidischer di‑GMP‑Signalweg, Adhäsin‑Protease, sulfatreduzierende Bakterien