Clear Sky Science · pl
Analizy strukturalne ujawniają interakcje proteazy z adhezyną oraz regulację receptora c-di-GMP u bakterii redukujących siarczany
Dlaczego „lepkość” bakterii ma znaczenie
Bakterie rzadko żyją jako pojedyncze komórki — częściej tworzą zatłoczone, śliskie społeczności zwane biofilmami. Takie skupiska mogą pokrywać rury, kadłuby statków, skały podziemne, a nawet urządzenia medyczne. W bakteriach redukujących siarczany, takich jak Desulfovibrio vulgaris, biofilmy mają dwie strony medalu: pomagają oczyszczać skażone środowiska, ale także przyspieszają korozję metali. W tej pracy zadano proste pytanie o dalekosiężnych konsekwencjach: jak te bakterie decydują, kiedy mocno przylegać do powierzchni, a kiedy się uwolnić?
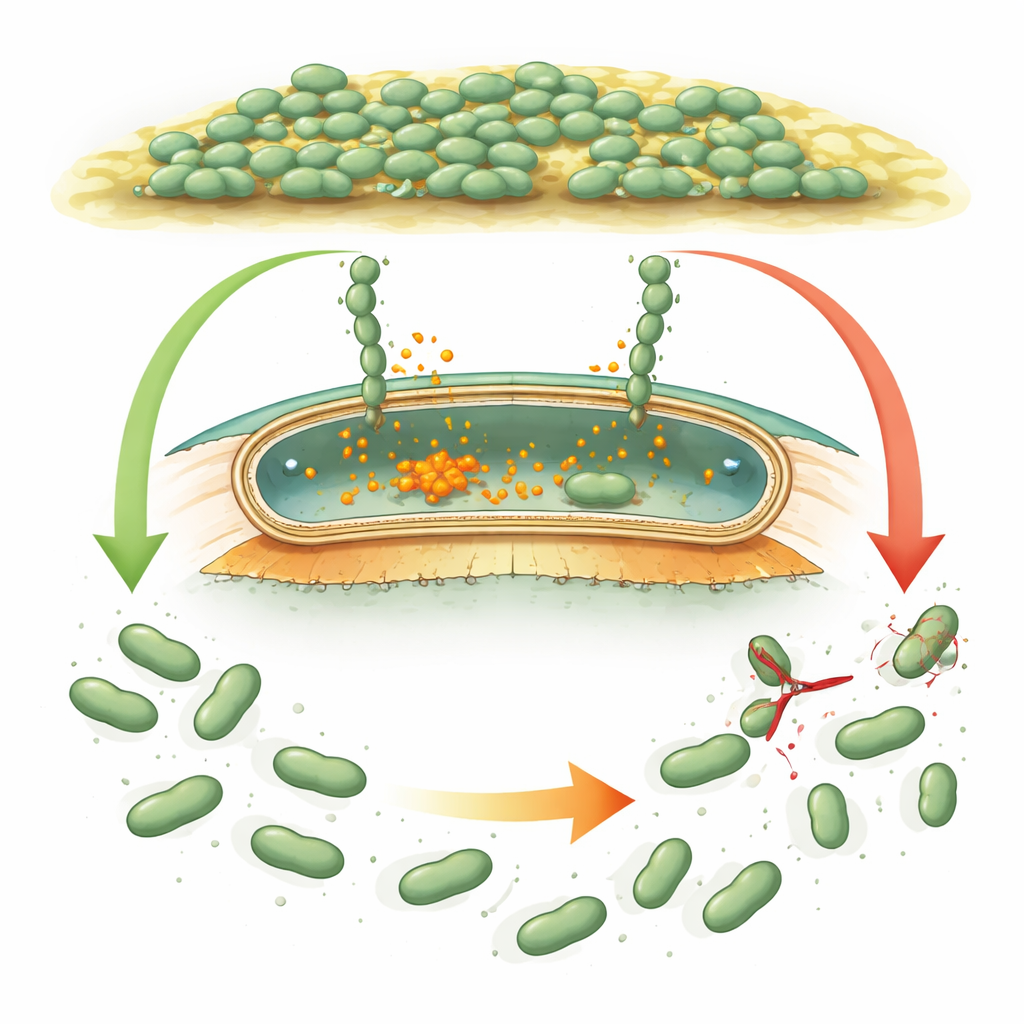
Jak mikroby chwycają i puszczają
Wiele bakterii korzysta z gigantycznych białek przypominających rzep, zwanych adhezynami, które przyklejają komórki do powierzchni i do siebie nawzajem. W dobrze zbadanych gatunkach, takich jak Pseudomonas, adhezyny kontrolowane są przez wewnętrzny sygnał chemiczny — cykliczny di‑GMP — którego poziom rośnie, gdy bakterie powinny tworzyć biofilm, i spada, gdy mają się rozproszyć. Przy wysokim poziomie sygnału adhezyny pozostają zakotwiczone w zewnętrznej powłoce komórki. Gdy sygnał maleje, mały „nożyk” białkowy (proteaza) odcina adhezynę blisko powierzchni komórki, a lepka część odpływa, ułatwiając odłączenie komórek. Desulfovibrio vulgaris ma zestaw genów wyglądający na podobny, ale jego białka regulacyjne różnią się sekwencją i kształtem na tyle, że naukowcy nie mogli stwierdzić, czy działa według tej samej logiki, czy według zupełnie nowej strategii.
Specjalistyczne nożyce molekularne
Autorzy najpierw skupili się na DvhG, desulfowibryjskiej wersji proteazy tnącej adhezyny. Dzięki predykcji strukturalnej i testom biochemicznym wykazali, że DvhG ma tę samą podstawową fałdową architekturę i mechanizm katalityczny co jej odpowiedniki w innych bakteriach i wymaga wapnia do działania. Precyzyjnie tnie dwie duże adhezyny, które Desulfovibrio wykorzystuje do tworzenia biofilmu, w niemal identycznych miejscach tuż za krótkim „segmentem retencyjnym”, który utrzymuje te białka osadzone w zewnętrznej błonie. Co ciekawe, zespół odkrył, że DvhG robi coś więcej niż rozpoznaje krótką sekwencję docelową. Masywna domena retencyjna każdej adhezyny nawiązuje szerokie kontakty z proteazą, tworząc dużą powierzchnię dokującą, która zwiększa skuteczność cięcia. Mutacje zakłócające ten obszar dokowania znacznie osłabiają aktywność DvhG, ujawniając dodatkową warstwę swoistości w porównaniu z pokrewnymi systemami.
Wewnętrzny przełącznik reagujący na sygnał
Drugi kluczowy element, DvhD, osadzony jest w błonie wewnętrznej i sięga zarówno do wnętrza komórki, jak i przestrzeni międzybłonowej. Badacze rozwiązywali kilka strukturalnych trójwymiarowych modeli fragmentów DvhD. Na zewnątrz komórki jego periplazmatyczny obszar tworzy domenę dCache, powszechną architekturę sensoryczną często wiążącą małe cząsteczki. Wnętrze komórki zawiera domenę HD‑GYP, moduł zwykle spotykany w enzymach rozkładających cykliczny di‑GMP. Tutaj jednak brakowało krytycznych reszt wiążących metale, a precyzyjne testy wykazały, że DvhD nie rozkłada sygnału; zamiast tego wiąże cykliczny di‑GMP bardzo mocno. Migawki strukturalne ujawniły dwa odmienne kieszonki wiążące, w których do trzech cząsteczek cyklicznego di‑GMP może mostkować parę domen HD‑GYP i przestawić je w nowe ułożenie, rozdzierając długie helisy łączące się z resztą receptora.
Od wewnętrznego sygnału do zachowania na powierzchni
Porównując formy DvhD „pustą” i związaną z ligandem, zespół odsłonił, jak wiązanie cyklicznego di‑GMP może przekształcić dimer receptora. Oczekuje się, że te zmiany przekażą sygnał przez błonę wewnętrzną i przesuną domenę periplazmatyczną dCache, która z kolei wchodzi w interakcję z DvhG. Modele sugerują, że gdy DvhD angażuje DvhG, blokuje dostęp proteazy do adhezyn i może nawet zaburzać miejsce wiążące wapń, wyłączając tym samym „nożyce”. Gdy poziomy cyklicznego di‑GMP spadają, kształt receptora relaksuje się, uwalniając DvhG, który może chwycić domeny retencyjne adhezyn i je przeciąć, pozwalając zewnętrznym częściom adhezyn — a więc macierzowi biofilmu — odsunąć się od powierzchni komórki. W ten sposób Desulfovibrio przekłada wewnętrzny odczyt chemiczny swoich warunków na decyzję mechaniczną: pozostać przytwierdzonym albo się rozproszyć.
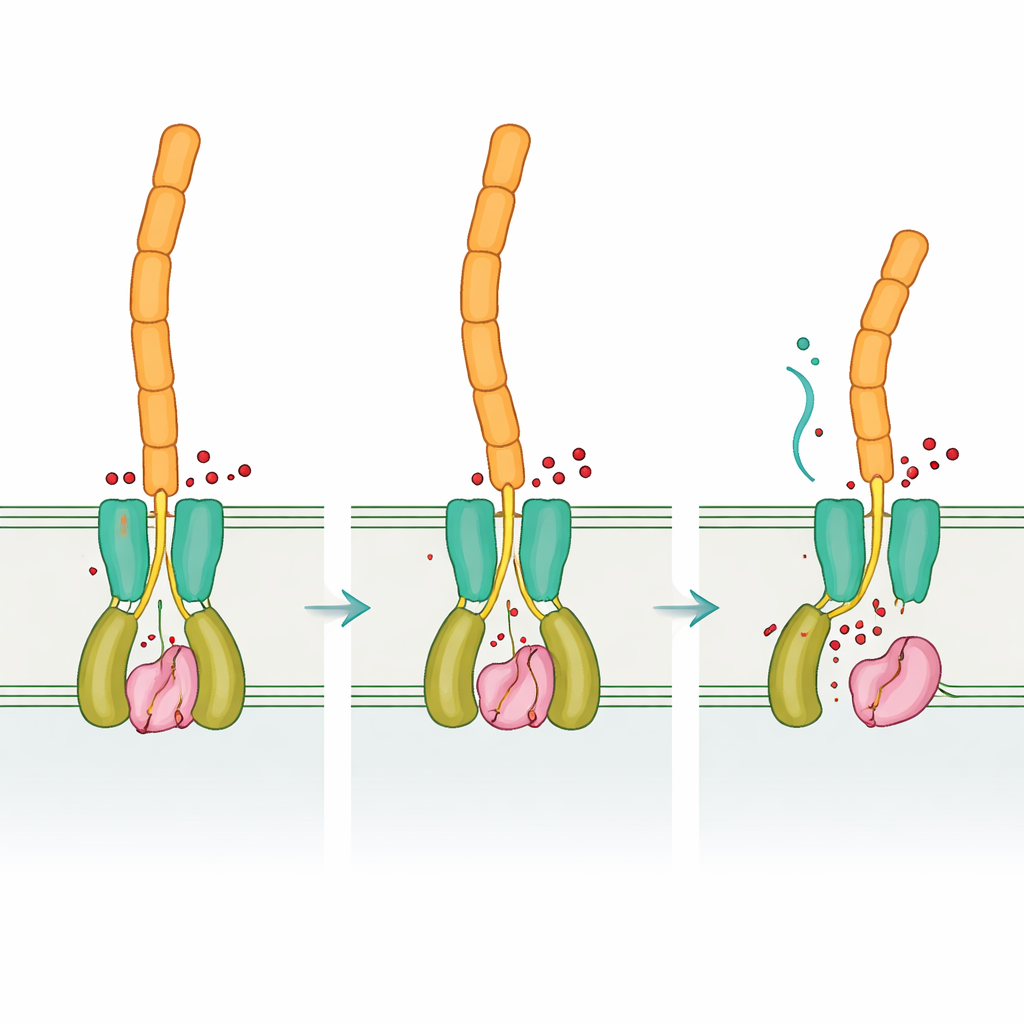
Ta sama logika, inne podzespoły
Podsumowując, wyniki pokazują, że Desulfovibrio vulgaris stosuje tę samą ogólną logikę regulacyjną co bardziej znane bakterie — cykliczny di‑GMP kontroluje receptor, który z kolei powstrzymuje lub uwalnia proteazę tnącą powierzchniowe adhezyny — ale realizuje ją przy użyciu bardzo innego zestawu białkowych „części”. To połączenie zachowania i wynalazczości ilustruje, jak ewolucja może ponownie wykorzystywać udane pomysły sygnalizacyjne, jednocześnie przeobrażając molekuły, które je realizują. Zrozumienie tej elastycznej konstrukcji pogłębia wiedzę o tym, jak biofilmy powstają i się rozpadają w różnych grupach bakterii, i może wskazywać drogę do mądrzejszych strategii — zarówno sprzyjających korzystnym biofilmom w bioremediacji, jak i zakłócających szkodliwe, które prowadzą do korozji metali i przewlekłych zakażeń.
Cytowanie: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Słowa kluczowe: biofilmy bakteryjne, Desulfovibrio vulgaris, sygnalizacja cyklicznym di-GMP, proteaza adhezyny, bakterie redukujące siarczany