Clear Sky Science · it
Analisi strutturali rivelano interazioni proteasi‑adesina e regolazione del recettore c‑di‑GMP in batteri riduttori di solfato
Perché i batteri “appiccicosi” sono importanti
I batteri spesso non vivono come cellule isolate ma come comunità affollate e viscide chiamate biofilm. Queste comunità possono rivestire tubazioni, carene di navi, rocce sotterranee e persino dispositivi medici. Nei batteri riduttori di solfato come Desulfovibrio vulgaris, i biofilm sono una lama a doppio taglio: aiutano a depurare ambienti inquinati ma accelerano anche la corrosione dei metalli. Questo studio pone una domanda semplice ma dalle grandi implicazioni: come fanno questi batteri a decidere quando aggrapparsi saldamente a una superficie e quando staccarsi?
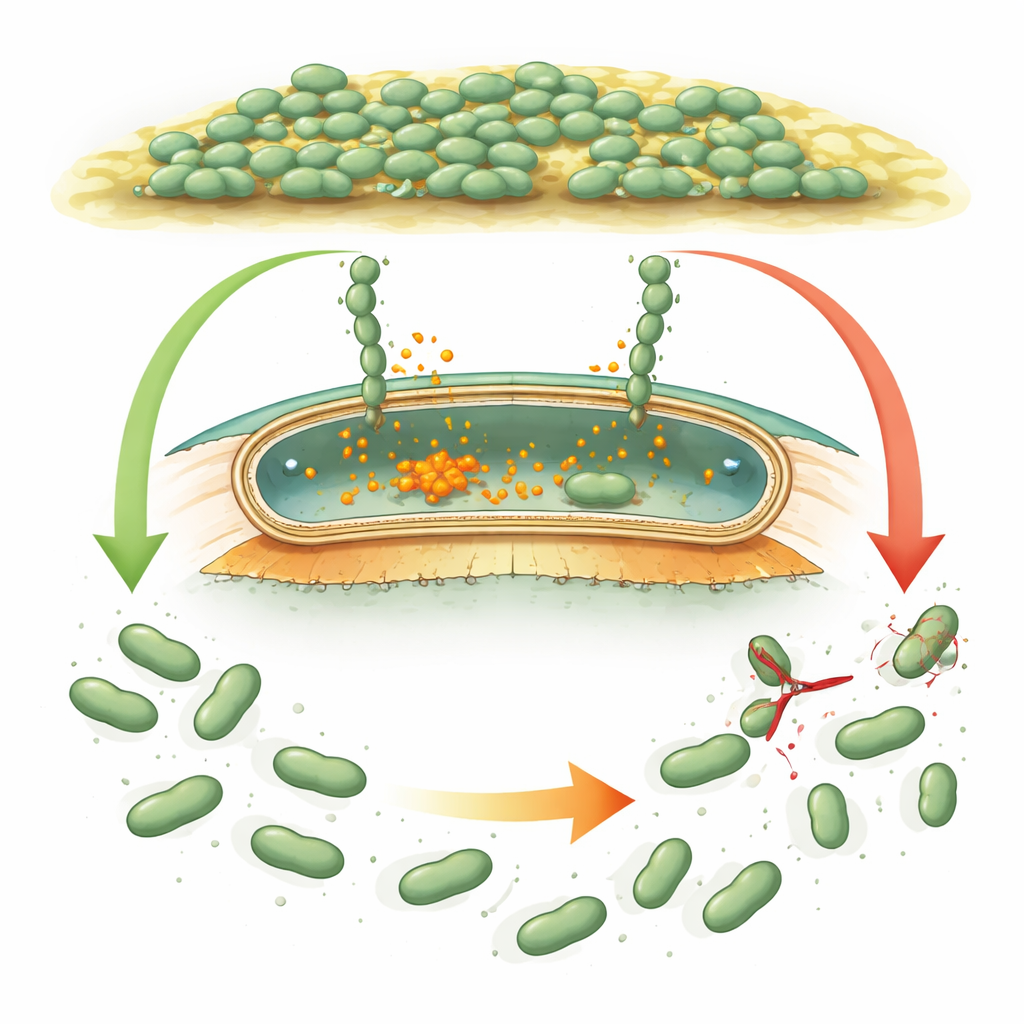
Come i microrganismi si attaccano e si staccano
Molti batteri usano proteine gigantesche “simili al Velcro”, chiamate adesine, che fissano le cellule alle superfici e tra loro. In specie ben studiate come Pseudomonas, queste adesine sono regolate da un segnale chimico interno, il cico‑di‑GMP, che aumenta quando i batteri devono formare un biofilm e diminuisce quando devono disperdersi. Quando il segnale è alto, le adesine restano ancorate allo strato esterno della cellula. Quando scende, una piccola cesoia proteica (una proteasi) taglia l’adesina vicino alla superficie cellulare e la porzione appiccicosa si allontana, aiutando le cellule a staccarsi. Desulfovibrio vulgaris possiede quello che sembra uno strumento genetico simile, ma le sue proteine regolatorie differiscono così tanto nella sequenza e nella forma che gli scienziati non potevano dire se usasse la stessa logica o una strategia completamente nuova.
Una forbice molecolare specializzata
Gli autori si sono prima concentrati su DvhG, la versione di Desulfovibrio della proteasi che taglia le adesine. Attraverso predizioni strutturali e test biochimici, hanno mostrato che DvhG possiede lo stesso ripiegamento di base e la stessa macchina catalitica dei suoi omologhi in altri batteri e richiede calcio per funzionare. Taglia con precisione due grandi adesine di cui Desulfovibrio ha bisogno per formare biofilm, in posizioni quasi identiche subito dopo un piccolo segmento di “ritenzione” che mantiene queste proteine inserite nella membrana esterna. In modo intrigante, il gruppo ha scoperto che DvhG fa più che riconoscere una breve sequenza bersaglio. Il voluminoso dominio di ritenzione di ciascuna adesina stabilisce ampi contatti con la proteasi, formando una grande superficie di docking che aumenta l’efficienza del taglio. Mutazioni che interrompono questa patch di docking rendono DvhG molto meno efficace, rivelando uno strato aggiuntivo di specificità rispetto a sistemi correlati.
Un interruttore sensibile al segnale all’interno della cellula
Il secondo protagonista, DvhD, è situato nella membrana interna e si estende sia nell’interno della cellula sia nello spazio tra le membrane. I ricercatori hanno risolto più strutture tridimensionali di frammenti di DvhD. All’esterno della cellula, la sua regione periplasmatica forma un dominio dCache, un’architettura sensoriale comune che spesso lega piccole molecole. All’interno della cellula, DvhD porta un dominio HD‑GYP, un modulo solitamente presente in enzimi che degradano il cico‑di‑GMP. Qui, tuttavia, i residui cruciali per il legame dei metalli sono assenti e saggi accurati hanno mostrato che DvhD non distrugge il segnale; al contrario, lega il cico‑di‑GMP in modo molto stretto. Fotogrammi strutturali hanno rivelato due tasche di legame distinte dove fino a tre molecole di cico‑di‑GMP possono collegare una coppia di domini HD‑GYP e costringerli in un nuovo assetto, separando lunghe eliche che si collegano al resto del recettore.
Dal segnale interno al comportamento di superficie
Confrontando le forme “vuote” e quelle legate al segnale di DvhD, il team ha scoperto come il legame del cico‑di‑GMP possa rimodellare il dimerio del recettore. Si prevede che questi cambiamenti si propaghino attraverso la membrana interna e riposizionino il dominio periplasmatico dCache, che a sua volta interagisce con DvhG. La modellizzazione suggerisce che quando DvhD interagisce con DvhG, blocca l’accesso della proteasi alle adesine e può perfino alterare il sito di legame del calcio, mettendo le forbici “off”. Quando i livelli di cico‑di‑GMP calano, la forma del recettore si rilassa, rilasciando DvhG in modo che possa agganciarsi ai domini di ritenzione delle adesine e tagliarli, permettendo alle porzioni esterne delle adesine — e quindi alla matrice del biofilm — di scivolare via dalla superficie cellulare. In questo modo, Desulfovibrio applica una lettura chimica interna delle proprie condizioni a una decisione meccanica: restare attaccato o disperdersi.
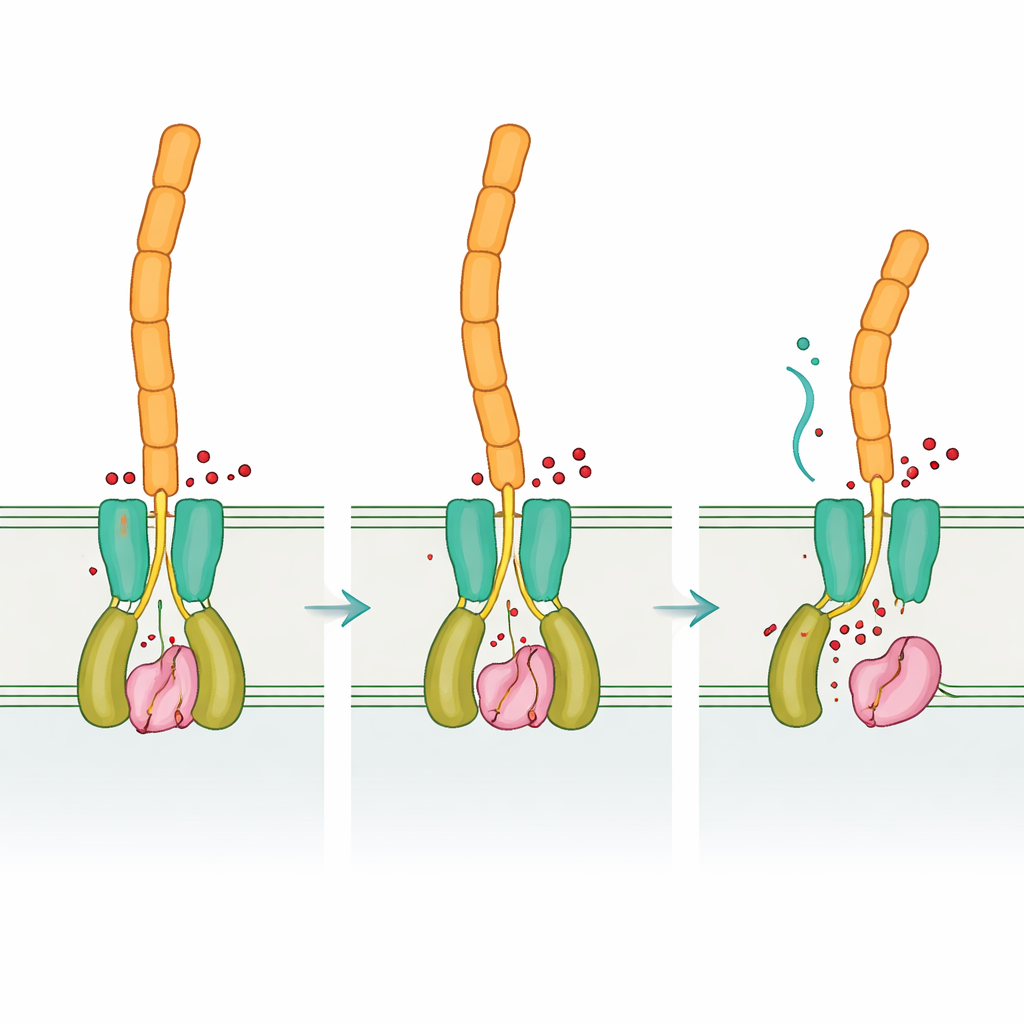
Stessa logica, componenti diversi
Nel loro complesso, i risultati mostrano che Desulfovibrio vulgaris usa la stessa logica regolatoria generale di batteri più familiari — il cico‑di‑GMP controlla un recettore che a sua volta trattiene o libera una proteasi che taglia le adesine di superficie — ma la implementa con un insieme molto diverso di “pezzi” proteici. Questa mescolanza di conservazione e reinvenzione illustra come l’evoluzione possa riutilizzare idee di segnalazione efficaci rimodellando le molecole che le eseguono. Comprendere questo progetto flessibile non solo approfondisce la nostra comprensione di come i biofilm si formano e si dissolvono in molti gruppi batterici, ma può anche indicare strategie più intelligenti per promuovere biofilm utili nella biorisanamento o interrompere quelli dannosi che provocano corrosione dei metalli e infezioni croniche.
Citazione: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Parole chiave: biofilm batterici, Desulfovibrio vulgaris, segnalazione ciclica di-GMP, proteasi dell’adesina, batteri riduttori di solfato