Clear Sky Science · fr
Des analyses structurelles dévoilent les interactions protéase‑adhésine et la régulation du récepteur c‑di‑GMP chez les bactéries réductrices de sulfate
Pourquoi les bactéries « collantes » comptent
Les bactéries vivent souvent non pas comme des cellules isolées mais en communautés denses et visqueuses appelées biofilms. Ces communautés peuvent enrober des canalisations, des coques de navires, des roches souterraines et même des dispositifs médicaux. Chez les bactéries réductrices de sulfate comme Desulfovibrio vulgaris, les biofilms sont à la fois utiles et problématiques : ils aident à dépolluer des environnements contaminés mais accélèrent aussi la corrosion des métaux. Cette étude pose une question simple aux implications importantes : comment ces bactéries décident‑elles de s’accrocher fermement à une surface ou de s’en détacher ?
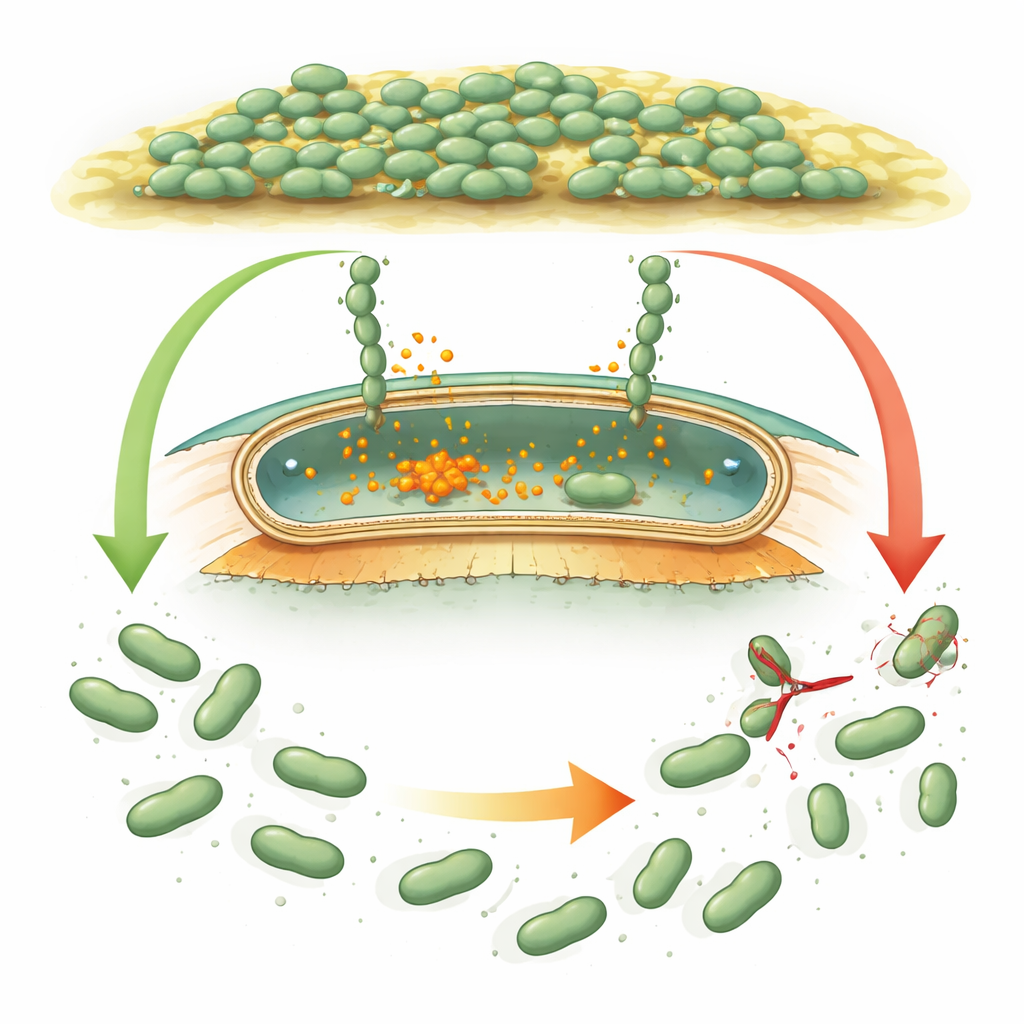
Comment les microbes s’accrochent et se détachent
Beaucoup de bactéries utilisent de très grosses protéines « type Velcro », appelées adhésines, qui collent les cellules aux surfaces et entre elles. Chez des espèces bien étudiées comme Pseudomonas, ces adhésines sont contrôlées par un signal chimique interne, le cyclique di‑GMP, qui augmente lorsque les bactéries doivent former un biofilm et diminue lorsqu’elles doivent se disperser. Quand le signal est élevé, les adhésines restent ancrées dans l’enveloppe externe de la cellule. Quand il baisse, une petite cisaille protéique (une protéase) coupe l’adhésine près de la surface cellulaire, et la portion collante s’échappe, facilitant le détachement. Desulfovibrio vulgaris possède ce qui ressemble à un dispositif génétique similaire, mais ses protéines régulatrices diffèrent tellement par leur séquence et leur forme que les chercheurs ne pouvaient pas dire s’il suivait la même logique ou une stratégie entièrement nouvelle.
Des ciseaux moléculaires spécialisés
Les auteurs se sont d’abord concentrés sur DvhG, la version de Desulfovibrio de la protéase qui clive les adhésines. Grâce à la prédiction structurale et à des tests biochimiques, ils ont montré que DvhG possède le même repli fondamental et l’appareil catalytique que ses homologues chez d’autres bactéries et nécessite du calcium pour fonctionner. Elle coupe précisément deux grandes adhésines dont Desulfovibrio a besoin pour former des biofilms, à des positions presque identiques juste après un petit segment de « rétention » qui maintient ces protéines logées dans la membrane externe. Fait intrigant, l’équipe a constaté que DvhG fait plus que reconnaître une courte séquence cible : le volumineux domaine de rétention de chaque adhésine établit des contacts étendus avec la protéase, formant une large surface d’amarrage qui augmente l’efficacité de la coupure. Des mutations perturbant cette zone d’amarrage rendent DvhG beaucoup moins efficace, révélant un niveau supplémentaire de spécificité par rapport aux systèmes apparentés.
Un commutateur sensoriel à l’intérieur de la cellule
Le second acteur clé, DvhD, est ancré dans la membrane interne et s’étend à la fois à l’intérieur de la cellule et dans l’espace périplasmique. Les chercheurs ont résolu plusieurs structures tridimensionnelles de fragments de DvhD. À l’extérieur de la cellule, sa région périplasmique forme un domaine dCache, une architecture sensorielle courante qui lie souvent de petites molécules. À l’intérieur de la cellule, DvhD porte un domaine HD‑GYP, un module habituellement présent dans des enzymes qui dégradent le cyclique di‑GMP. Ici, toutefois, les résidus cruciaux de liaison au métal sont absents, et des essais attentifs ont montré que DvhD ne détruit pas le signal ; au contraire, il se lie très fortement au cyclique di‑GMP. Des instantanés structuraux ont révélé deux poches de liaison distinctes où jusqu’à trois molécules de cyclique di‑GMP peuvent faire le pont entre une paire de domaines HD‑GYP et les forcer à adopter une nouvelle configuration, écartant de longues hélices qui relient le reste du récepteur.
Du signal interne au comportement de surface
En comparant les formes « vides » et liées au signal de DvhD, l’équipe a découvert comment la liaison du cyclique di‑GMP peut remodeler le dimère du récepteur. On s’attend à ce que ces changements se propagent à travers la membrane interne et repositionnent le domaine périplasmique dCache, qui interagit à son tour avec DvhG. La modélisation suggère que lorsque DvhD engage DvhG, il bloque l’accès de la protéase aux adhésines et peut même déformer son site de liaison au calcium, mettant les ciseaux « en position off ». Quand les niveaux de cyclique di‑GMP chutent, la conformation du récepteur se relâche, libérant DvhG afin qu’il puisse se fixer aux domaines de rétention des adhésines et les couper, permettant aux parties externes des adhésines — et donc à la matrice du biofilm — de se détacher de la surface cellulaire. De cette manière, Desulfovibrio transpose une lecture chimique interne de son environnement en une décision mécanique : rester attaché ou se disperser.
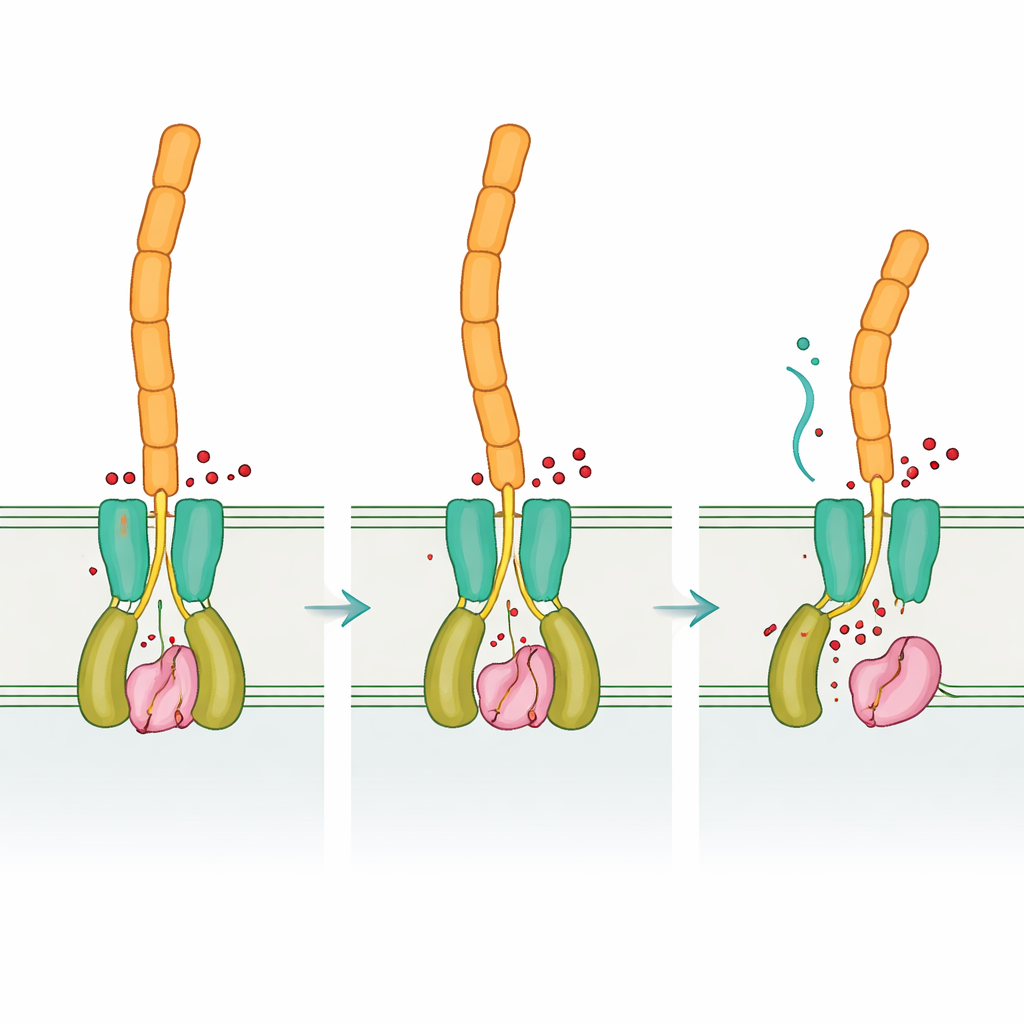
Même logique, matériel différent
Dans l’ensemble, les résultats montrent que Desulfovibrio vulgaris utilise la même logique régulatrice globale que des bactéries mieux connues : le cyclique di‑GMP contrôle un récepteur qui, à son tour, retient ou libère une protéase qui découpe les adhésines de surface — mais l’implémente avec un ensemble de « pièces » protéiques très différent. Ce mélange de conservation et de réinvention illustre comment l’évolution peut réutiliser des idées de signalisation efficaces tout en remodelant les molécules qui les mettent en œuvre. Comprendre cette conception flexible approfondit non seulement notre compréhension de la formation et de la dissociation des biofilms à travers de nombreux groupes bactériens, mais peut aussi indiquer des voies vers des stratégies plus intelligentes pour favoriser des biofilms utiles en bioremédiation ou perturber ceux nuisibles qui provoquent la corrosion des métaux et des infections chroniques.
Citation: Font, M.E., Karbelkar, A.A., Lormand, J.D. et al. Structural analyses uncover protease-adhesin interactions and c-di-GMP receptor regulation in sulfate-reducing bacteria. Nat Commun 17, 3564 (2026). https://doi.org/10.1038/s41467-026-71936-5
Mots-clés: biofilms bactériens, Desulfovibrio vulgaris, signalisation cyclique di‑GMP, protéase d'adhésine, bactéries réductrices de sulfate